Электролиз водных растворов электролитов
Для проведения электролиза приготовлены стандартные водные растворы трех различных электролитов, формулы которых приведены в вашем варианте задания в таблице 16. Используя эти данные, выполните следующие задания:
а) рассмотрите электролиз водных растворов электролита 1, электролита 2 и электролита 3 на инертных электродах (предложите варианты инертных электродов) при стандартных условиях; напишите уравнения катодного, анодного и суммарного процессов (или объясните, почему невозможно написать уравнение суммарного процесса электролиза);
г) рассмотрите электролиз водного раствора электролита 3 с активным анодом (предложите вариант активного анода для данного электролита) при стандартных условиях; напишите уравнения протекающих процессов.
Варианты задания 8.4 приведены в таблице 16.
Таблица 16
| № вар. | Электролиты | № вар. | Электролиты | ||||
| LiOH | K2SO4 | CuCl2 | Mg(NO3)2 | AlCl3 | AgF | ||
| KCl | HF | AgNO3 | Al(NO3)3 | CaI2 | HgCl2 | ||
| CsBr | LiNO3 | Hg(NO3)2 | H2SO4 | Na2S | Au(NO3)3 | ||
| BaI2 | Cs2SO4 | AuCl3 | CsOH | Li2SO4 | PbCl2 | ||
| Na2S | Ba(OH)2 | Pb(NO3)2 | LiCl | K3PO4 | NiBr2 | ||
| MgCl2 | Ca(NO3)2 | NiSO4 | KBr | HNO3 | SnSO4 | ||
| AlBr3 | Na3PO4 | SnCl2 | BaCl2 | CsOH | CoSO4 | ||
| CaCl2 | MgSO4 | AgF | Na2S | Ba(NO3)2 | CdCl2 | ||
| HI | Al(NO3)3 | CoI2 | MgBr2 | Ca(NO3)2 | FeCl2 | ||
| Li2SO4 | KOH | Cd(NO3)2 | AlCl3 | NaF | Cr(NO3)3 | ||
| KF | LiCl | FeSO4 | CaI2 | Mg(NO3)2 | ZnI2 | ||
| CsNO3 | CsI | CrCl3 | HBr | Al2(SO4)3 | MnSO4 | ||
| Ba(OH)2 | BaBr2 | ZnSO4 | BeCl2 | NaOH | Pt(NO3)2 | ||
| Ca(ClO4)2 | HCl | MnBr2 | LiOH | K2SO4 | MnSO4 | ||
| Na2CO3 | MgBr2 | CuSO4 | KCl | HF | ZnI2 |
Справочные данные
Приложение А.
Термодинамические свойства некоторых веществ.
| Формула вещества | ∆Нfo,298, кДж*моль-1 | So298, Дж*моль-1*K-1 | ∆Gfo,298, кДж*моль-1 |
| Al(к.) Al2O3(к.) Al2(SO4)3(к.) B(к.) B2O3(к.) Br2(г.) C(графит) CH3OH(ж.) CH4(г.) C2H2(г.) C2H4(г.) CO(г.) COCl2(г.) CO2(г.) Ca(к.) CaO(к.) Cl2(г.) Cu(к.) CuO(к.) Fe(к.) FeO(к.) FeS2(к.) Fe2O3(к.) Fe3O4(к.) H2(г.) HBr(г.) HCl(г.) HI(г.) H2O(ж.) H2O(г.) H2S(г.) I2(г.) Mg(к.) MgCl2(к.) MgO(к.) Mn(к.) MnO2(к.) N2(г.) NH3(г.) NH4NO3(к.) NO(г.) NOCl(г.) NO2(г.) N2O(г.) N2O4(г.) NaAlO2(к.) Na2O(к.) O2(г.) PCl3(г.) PCl5(г.) Pb(к.) PbO(к.) Sромб. SO2(г.) SO2Cl2(г.) SO3(г.) Si(к.) SiC(к.) SiCl4(г.) SiO2(к.) Ti(к.) TiCl4(ж.) TiO2(к.) W(к.) WO3(к.) Zn(к.) ZnO(к.) | -1675,69 -3441,80 -1270,43 30,91 -238,57 -74,85 226,75 52,30 -110,53 -219,50 -393,51 -635,09 -162,00 -264,85 -177,40 -822,16 -1117,13 -36,38 -92,31 26,36 -285,83 -241,81 -20,60 62,43 -644,80 -601,49 -521,49 -45,94 -365,43 91,26 52,59 34,19 82,01 11,11 -1133,03 -417,98 -287,02 -374,89 -219,28 -296,90 -363,17 -395,85 -66,10 -657,52 -910,94 -804,16 -944,75 -842,91 -348,11 | 28,33 50,92 239,20 5,86 53,84 245,37 5,74 126,78 186,27 200,82 219,45 197,55 283,64 213,66 41,63 38,07 222,98 33,14 42,63 27,15 60,75 52,93 87,45 146,19 130,52 198,58 186,79 206,48 69,95 188,72 205,70 260,60 32,68 89,54 27,07 32,01 53,14 191,50 192,66 151,04 210,64 263,50 240,06 219,83 304,35 70,29 75,06 205,04 311,71 364,47 64,81 66,11 31,92 248,07 311,29 256,69 18,83 16,61 330,95 41,84 30,63 252,40 50,33 32,64 75,90 41,63 43,51 | -1582,27 -3100,87 -1191,29 3,14 -166,27 -50,85 209,21 68,14 -137,15 -205,31 -394,37 -603,46 -134,26 -244,30 -166,05 -740,34 -1014,17 -53,43 -95,30 1,58 -237,23 -228,61 -33,50 19,39 -595,30 -569,27 -466,68 -16,48 -183,93 87,58 66,37 52,29 104,12 99,68 -1069,20 -379,26 -267,98 -305,10 -189,10 -300,21 -318,85 -371,17 -67,7 -617,62 -856,67 -737,32 -889,49 -764,11 -318,10 |
Приложение Б.
Константы диссоциации некоторых слабых электролитов в водных растворах при 25°С.
| Кислота | Кк | Основание | Ко |
| HF | 6,67*10-4 | NH4OH | 1,76*10-5 |
| HCN | 4,93*10-10 | Al(OH)3 K3 | 1,38*10-9 |
| HAsO2 | 6,03*10-10 | Cd(OH)2 K2 | 4,20*10-7 |
| HBrO | 2,06*10-9 | Co(OH)2 K2 | 7,90*10-6 |
| HClO | 2,82*10-8 | Cr(OH)3 K2 K3 | 3,50*10-9 8,90*10-11 |
| HIO | 2,29*10-11 | Cu(OH)2 K2 | 2,20*10-7 |
| HNO2 | 5,13*10-4 | Fe(OH)2 K2 | 5,50*10-8 |
| H2O2 | 2,40*10-12 | Mg(OH)2 K2 | 2,60*10-3 |
| H3PO2 | 7,94*10-2 | Mn(OH)2 K2 | 3,90*10-4 |
| HCOOH | 1,78*10-4 | Ni(OH)2 K2 | 8,30*10-4 |
| CH3COOH | 1,74*10-5 | Pb(OH)2 K1 K2 | 5,00*10-4 1,40*10-8 |
| H2S K1 K2 | 1,05*10-7 1,23*10-13 | Zn(OH)2 K1 K2 | 1,30*10-5 4,90*10-7 |
| H2Se K1 K2 | 1,55*10-4 1,00*10-11 | ||
| H2B4O7 K1 K2 | 1,80*10-4 2,00*10-8 | ||
| H2CO3 K1 K2 | 4,27*10-7 4,68*10-11 | ||
| H2C2O4 K1 K2 | 6,46*10-2 6,17*10-5 | ||
| H2CrO4 K2 | 3,16*10-7 | ||
| H2MoO4 K2 | 1,00*10-6 * | ||
| H3PO3 K1 K2 | 1,00*10-2 2,57*10-7 | ||
| H2SO3 K1 K2 | 1,58*10-2 6,31*10-8 | ||
| H2SeO3 K1 K2 | 2,45*10-3 4,79*10-9 | ||
| H2SiO3 K1 K2 | 2,20*10-10 * 1,60*10-12 * | ||
| H2WO4 K2 | 2,19*10-4 | ||
| H3AsO4 K1 K2 K3 | 5,50*10-3 1,07*10-7 3,02*10-12 | ||
| H3PO4 K1 K2 K3 | 7,24*10-3 6,17*10-8 4,57*10-13 |
Примечание:
Значения констант диссоциации, отмеченные астериксом (*), отвечают температуре 18°С.
Приложение В.
Произведение растворимости
некоторых малорастворимых электролитов при 25°С.
| Электролит | ПР | Электролит | ПР |
| Ag2CO3 Ag2C2O4 AgCl Ag2CrO4 AgI AgIO3 Ag2S Ag2SO4 Al(OH)3 AlPO4 BaCO3 BaC2O4 BaCrO4 BaF2 BaSO3 BaSO4 CaCO3 CaC2O4 CaF2 CaMoO4 CaSO3 CaSO4 CaWO4 CdCO3 CdC2O4 Cd(OH)2 CdS | 8,7*10-12 1,1*10-11 1,8*10-10 1,2*10-12 2,3*10-16 3,2*10-8 7,2*10-50 1,2*10-5 5,7*10-32 1,7*10-19 4,9*10-9 1,1*10-7 1,1*10-10 1,7*10-6 8,0*10-7 * 1,8*10-10 4,4*10-9 2,3*10-9 * 4,0*10-11 3,2*10-9 3,2*10-7 * 3,7*10-5 1,6*10-9 2,5*10-14 1,5*10-8 * 4,3*10-15 6,5*10-28 | CoCO3 CuS FeCO3 FeO(OH) FeS HgO HgS Li3PO4 MgF2 MnCO3 MnS NiCO3 PbCrO4 PbS PbWO4 RaSO4 SrCO3 SrCrO4 SrF2 Sr3(PO4)2 SrSO4 Tl2CrO4 ZnCO3 ZnC2O4 Zn(OH)2 ZnS(кубич.) | 1,5*10-10 1,4*10-36 2,9*10-11 2,2*10-42 3,4*10-17 3,3*10-26 1,4*10-45 3,2*10-9 * 6,4*10-9 4,9*10-11 1,1*10-13 1,3*10-7 2,8*10-13 8,7*10-29 4,5*10-12 4,3*10-11 5,3*10-10 2,7*10-5 2,5*10-9 1,0*10-31 * 2,1*10-7 1,0*10-12 5,3*10-11 1,5*10-9 * 3,0*10-16 1,2*10-25 |
Примечание:
Значения произведений растворимости, отмеченные астериксом (*), отвечают комнатной температуре (18 – 25°С).
Приложение С.
Стандартные электродные потенциалы 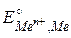 некоторых металлов
некоторых металлов
