Решение экспериментальных задач
ПО ТЕМЕ «МЕТАЛЛЫ»
Цель: закрепить знания о свойствах металлов, развивать умения применять полученные знания на практике, работать с химическим оборудованием и реактивами.
Оборудование: пробирки, стеклянная палочка, спиртовка.
Реактивы:медная проволока, цинк, алюминий; растворы карбоната натрия, хлорида натрия, гидроксида кальция, серной кислоты, гидроксида натрия, сульфата натрия, хлорида бария, хлорида цинка, алюминия, сульфат кальция.
G Соблюдайте правила техники безопасности!
Ход работы
Задача 1
В выданных вам пробирках находятся растворы гидроксида натрия, хлорида кальция, сульфат натрия. Определите опытным путем, какое вещество находится в каждой пробирке.
Для распознавания выданных веществ проведите качественные реакции на содержащиеся в растворах катионы и анионы.
Составьте соответствующие уравнения реакций в молекулярном и ионном виде.
Результаты исследований занесите в таблицу 1.
Задача 2
Из кусочка медной проволоки сделайте маленькую спираль и закрепите ее в держателе. Прокалите спираль в пламени спиртовки и отметьте произошедшие изменения.
Составьте уравнение химической реакции, уравняйте его с помощью метода электронного баланса, укажите окислитель и восстановитель.
Внесите прокаленную, еще теплую спираль в раствор серной кислоты. Отметьте признаки химической реакции.
Составьте уравнение химической реакции в молекулярном и ионном виде.
По результатам проведенных исследований заполните таблицу 2.
| Реактив | Номер пробирки, где произошли изменения | Наблюдения | Уравнение реакции |
| Задание | Наблюдения | Уравнение реакции |
| 1.Нагревание медной спирали в пламени спиртовки | ||
| 2. Взаимо-действие прокаленной медной проволоки с раствором серной кислоты |
| Задание | Наблюдения | Уравнение реакции |
| 1. Получение гидроксида алюминия | ||
| 2. Взаимодействие гидро-ксида алюминия с гидро-ксидом натрия | ||
| 3. Взаимодействие гидро-ксида алюминия с соляной кислотой |
Таблица 1
| (в молекулярном и ионном виде) | Вывод |
Таблица 2
| (в молекулярном и ионном виде) | Вывод |
Таблица 3
| (в молекулярном и ионном виде) | Вывод |
Задача 3
Из хлорида алюминия получите гидроксид алюминия и докажите его амфотерность.
1. Получение гидроксида алюминия.
К раствору хлорида алюминия по каплям добавьте раствор гидроксида натрия до появления белого осадка.
Составьте уравнения соответствующих реакций в молекулярном и ионном виде.
2. Доказательство амфотерного характера гидроксида алюминия.
Разделите осадок на две части.
а) К осадку гидроксида алюминия в пробирке 1 приливаем раствор гидроксида натрия до растворения осадка.
Составьте соответствующее уравнение реакции в молекулярном и ионном виде.
б) К осадку гидроксида алюминия в пробирке 2 приливаем раствор соляной кислоты до растворения осадка.
Составьте соответствующее уравнение реакции в молекулярном и ионном виде.
Заполните таблицу 3.
Сделайте вывод о свойствах металлов.
__________
Практическая работа № 5 «____»_____________________20____ г.
ПОЛУЧЕНИЕ ЭТИЛЕНА И ИЗУЧЕНИЕ ЕГО СВОЙСТВ
Цель: получить лабораторным способом этилен и исследовать его свойства.
Оборудование: лабораторный штатив, штатив с пробирками, пробка с газоотводной трубкой, спиртовка.
Реактивы: смесь этанола и концентрированной серной кислоты, иодная вода (с массовой долей 1 – 3%), раствор перманганата калия (с массовой долей 1 – 3%), центры кипения (кисочки фарфора или пемзы).
G Соблюдайте правила техники безопасности!
Ход работы
Прежде чем приступить к выполнению первого опыта, налейте в одну из пробирок на ¼ объема раствора иодной воды, а в другую – столько же раствора перманганата калия. Поставьте обе пробирки в штатив для пробирок. К оформлению отчета приступайте только после выполнения второго опыта (изучение химических свойств этилена)
Задание 1. Получение этилена
1. Поместите в пробирку с заранее приготовленной преподавателем смесью этилового спирта и концентрированной серной кислоты несколько крупинок фарфора для равномерного кипения смеси при нагреванию
2. Соберите прибор для получения этилена как показано на рисунке.
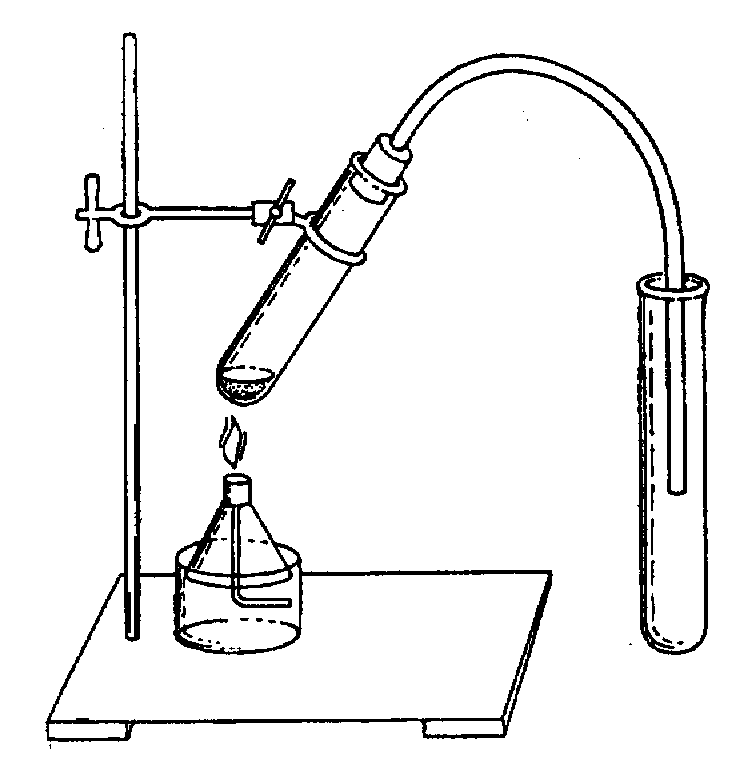
3. Нагревайте пробирку со смесью в пламени спиртовки до появления пузырьков газа в пробирке с иодной водой.
