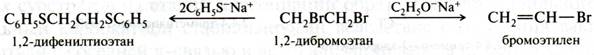Направление элиминирования: правила Зайцева и Гофмана
В большинстве реакций дегидрогалогенирования атома водорода отщепляется преимущественно от соседнего наименее гидрогенизированного атома углерода:
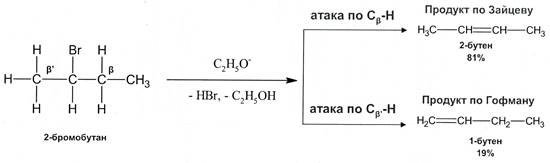
Рис. 19.9. Схема реакции элименирования по Зайцеву
1. Увеличение числа алкильных групп при двойной связи повышает её стабильность.
2. Как следствие, в тех случаях, когда выполняется правило Зайцева, следует ожидать образования наиболее замещенного алкена.
Правило Зайцева выполняется не всегда, т.е. атом водорода может отщепляться от соседнего более гидрогенезированного атома углерода с образованием менее замещенного алкена:
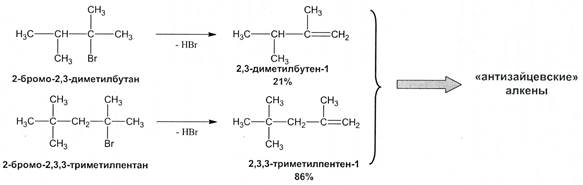
Рис. 19.10. Схема реакций дегалогенирования галогеналканов «вопреки правилу Зайцева»
Аналогичным образом протекает реакция разложения гидроксидов четвертичных аммониевых солей. Алкильные заместители аммониевых солей содержат атом водорода в β-положении к аммонийному азоту. В результате разложения образуются алкены, третичные амины и вода:
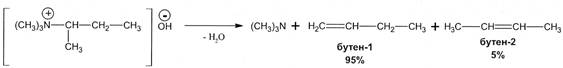
Рис. 19.11. Схема реакции разложения гидроксидов четвертичных аммониевых солей (по Гофману)
Элиминирование происходит по бимолекулярному механизму (E2).
Основание атакует наиболее доступный атом водорода (кинетический контроль):
- вызывая β-анти-элиминирование триалкиламинной группы;
- приводя к образованию наименее замещенного алкена:
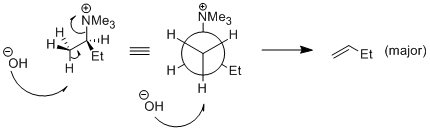
Особенности элиминирования по Гофману:
1. При разложении аммониевых, сульфониевых, фосфониевых и т. д. солей с наибольшим выходом образуется наименее замещенный алкен:
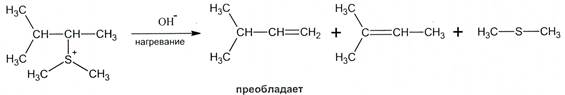
Рис. 19.12. Схема реакции разложения сульфониевых солей (по Гофману)
2. Реакция протекает по правилу Гофмана с соединениями, в которых уходящая группа положительно заряжена (-N+R3, -S+R2).
3. Правило Гофмана никогда не соблюдается абсолютно, всегда образуется некоторое количество продукта по правилу Зайцева (рис. 19.11).
4. Использование стерически объемных оснований (t-BuOK, Et3COK) способствует протеканию элиминирования по правилу Гофмана:

Рис. 19.13. Влияние стерически объемных оснований на протекание реакций элиминирования галогеналканов (правило Гофмана)
Конкурентность реакций нуклеофильного замещения и элиминирования
Конкуренция бимолекулярных реакций нуклеофильного замещения и элиминирования
Конкурентность РНЗ и РЭ обусловлена тем, что данные реакции осуществляются для одних и тех же субстратов и под влиянием одних и тех же реагентов.
В бимолекулярных процессах решающее воздействие на направление реакции (замещение или элиминирование) оказывает:
- относительная нуклеофильность;
и основность реагента. Что можно представить следующей схемой:
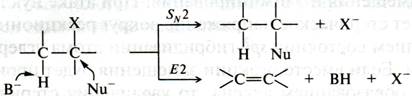
Рис. 19.14. Влияние относительной нуклеофильности и основности реагента на направление реакции
!!! Уже отмечалось ранее, что понятие «нуклеофил» и «основание» не тождественны и хороший нуклеофил необязательно будет сильным основанием, и наоборот.
1. Конкурентность РДмЗ и РДмЭ зависит от природы реагента. В связи с этим возможны два варианта:
- при использовании реагентов - сильных оснований - преимущественно протекает реакция элиминирования;
при использовании реагентов сильных как нуклеофил, но слабых как основание, преимущественно протекает реакция нуклеофильного замещения: