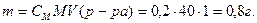Методика проведения опытов. 7.2.1 Опыт 1 Приготовление раствора с заданной массовой долей соли
7.2.1 Опыт 1 Приготовление раствора с заданной массовой долей соли
Получите у преподавателя задание и рассчитайте, сколько граммов соли и миллилитров воды потребуется для приготовления раствора заданной концентрации.
Покажите расчеты преподавателю и получите разрешение на проведение опыта.
Взвесьте на технохимических весах нужную массу соли и высыпьте ее в коническую колбу на 250 мл. Отмерьте цилиндром необходимый объем воды и влейте его в колбу с солью. Перемешивайте содержимое колбы до полного растворения соли.
Перелейте в цилиндр приготовленный раствор. При помощи ареометра измерьте его плотность рэксп.. Найдите по табл. 1 плотность раствора ртабл., соответствующую заданной концентрации.
Вычислите относительную ошибку опыта:
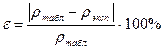
Рассчитайте молярную концентрацию, молярную концентрацию эквивалента, моляльную концентрацию и титр приготовленного раствора. Результаты опыта и расчетов сведите в табл. 7.2.
Таблица 7.2 - Результаты опыта 1
| Формула соли | Масса соли, г | V раствора, мл | V воды, мл | ртабл., г/см3 | рэксп., г/см3 | ω% | СМ | CН | Сb | Т |
7.2.2 Опыт 2 Приготовление раствора с заданной массовой долей из более
концентрированного раствора
В качестве более концентрированного раствора используется раствор, приготовленный в опыте 1.
Получите у преподавателя задание. Определите плотность заданного раствора по табл. 7.1. Рассчитайте объем более концентрированного раствора соли и объем воды, необходимые для приготовления раствора заданной концентрации.
Покажите расчеты преподавателю и получите разрешение на выполнение опыта.
Отмерьте цилиндром рассчитанный объем более концентрированного раствора соли и долейте водой до необходимого объема. Приготовленный раствор тщательно перемешайте, переливая из цилиндра в колбу и обратно. При помощи ареометра измерьте плотность раствора рэксп.. Вычислите относительную ошибку опыта аналогично опыту 1. Результаты опыта сведите в табл.7.3
Таблица 7.3 – Результаты опыта 2
| ω% | V, мл | р, г/см3 | |||||
| Исходного раствора | Заданного раствора | Исходного раствора | Заданного раствора | Воды | Исходного раствора | Заданного раствора | |
| Ртабл. | Рэксп. | ||||||
Примеры решения задач
Пример 1 Массовая доля растворенного вещества.
Определите массовую долю в (%) хлорида калия в растворе, содержащем 0,053 кг KCI в 0,5 л раствора, плотность которого 1063 кг/м3.
Решение
Массовую долю вещества находим по формуле
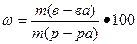 %
%
где m(в-ва), масса вещества, г ;
m(р-ра), масса раствора, г.
Масса раствора равна произведению объема раствора V на его плотность ρ
m=Vρ, тогда 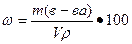
массовая доля хлорида калия в растворе равна:
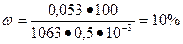 .
.
Пример 2 Молярная концентрация раствора.
Какова масса NaOH, содержащегося в 0,2 л раствора, если молярная концентрация раствора 0,2 моль/л?
Решение
Молярную концентрацию вещества находят по формуле
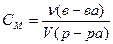
где ν(в-ва), количество вещества, моль;
V(р-ра), объем раствора, л.
Количество вещества ν вычисляют по формуле
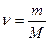
где m, масса вещества, г;
М, молярная масса вещества, г/моль.
Тогда масса NaOH, содержащегося в растворе, равна