Классификация химических соединений ,закномоерность протекания химических реакций
Билет 1
1.1Атом - наименьшая, химически неделимая часть химического элемента. Атом состоит из атомного ядра и электронов. Ядро атома состоит из положительно заряженныхпротонов и незаряженных нейтронов.
Атомы классифицируются по количеству протонов и нейтронов в ядре: количество протонов определяет принадлежность атома некоторому химическому элементу, а число нейтронов — изотопу этого элемента.
Материя не может существовать вне движения, она всегда находится в состоянии движения, изменения и развития. При уничтожении движения объект прекращает свое существование, переходит в другие объекты, которым характерно движение покоя – состояния движений, обеспечивающих стабильность предмета, сохраняя его качества. Покой относителен, а движение абсолютно – это неотъемлемое свойство материи.
Материя не существует без движения, так же как движение не существует без материи.
Движение материи– постоянное ее взаимодействие, а также изменения состояния объектов, вызванные этими взаимодействиями. Формы движения материи различны. Пример формы движения материи: нагревание и охлаждение тел, излучение света, электрический ток, химические и физические превращения, жизненные процессы. Классификация форм движения материи :
1) неживая природа;
2) живая природа;
3) общество.
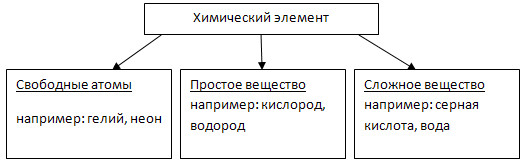
Свободными называют атомы, которые не имеют химической связи с другими атомами. Большинство простых веществ, образованных одним химическим элементом, состоят из химически связанных, т. е. не свободных атомов.
Пример свободных атомов, которые могут существовать сколько угодно долго - это благородные газы гелий, неон, аргон, криптон, ксенон. Отдельные атомы других химических элементов в свободном состоянии не могут существовать долго из за высокой реакционной способности.
Простые вещества – это вещества, образованные атомами одного и того же химического элемента.
Вещества, образованные из двух и более химических элементов, называются сложными.
Химическая промышленность преследует цель снабдить народное хозяйство различными веществами, материалами, продуктами, получаемыми ею путем изменения состава или структуры исходных веществ, т. е. химическими способами.
Химизация народного хозяйства — это внедрение химических методов обработки материалов и продуктов химической промышленности во все отрасли производства, культуры и быта.
1.2
1) CaCO3+2HCl=CaCl2+H2O+CO2 (мрамор или известняк + кислота)
2) CO2+Ca(OH)2=CaCO3+H2O (известковая вода - раствор гидроксида кальция)
3) CO2+CaCO3+H2O=Ca(HCO3)2 (гидрокарбонат кальция - заметно растворимая соль)
4) Ca(HCO3)2 ---> CaCO3+H2O+CO2 (гидрокарбонат кальция - очень неустойчива, как все гиддрокарбонаты, и легко распадается при нагревании на основную соль и CO2, CaCO3 вновь выпадает в осадок)
1.3 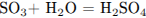
Рассчитаем массу серной кислоты, находившейся в исходном растворе и получившейся из х моль
оксида серы (VI):
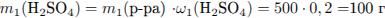
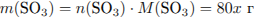 (где х - число молей оксида серы)
(где х - число молей оксида серы)
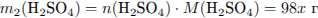
Рассчитаем массу раствора и суммарную массу серной кислоты в нём:
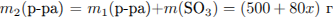
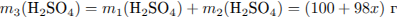
Найдем массу 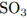 , необходимую для растворения:
, необходимую для растворения:
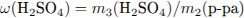
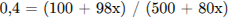
Откуда 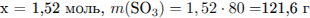
Билет 2
2.1
Квантовые числа –энергетические параметры, определяющие состояние электрона и тип атомной орбитали, на которой он находится.
Главное квантовое число(n)определяет общую энергию электрона и степень его удаления от ядра (номер энергетического уровня); оно принимает любые целочисленные значения, начинаю с 1 (n= 1, 2, 3…).
Орбитальное квантовое число (l) характеризует геометрическую форму орбитали. Принимает значение целых чисел от 0 до (n - 1). Независимо от номера энергетического уровня, каждому значению орбитального квантового числа соответствует орбиталь особой формы. Набор орбиталей с одинаковыми значениями n называется энергетическим уровнем, c одинаковыми n и l - подуровнем.
Магнитное квантовое число(m) характеризует положение электроннойорбитали в пространстве и принимает целочисленные значения от -I до +I, включая 0. Это означает, что для каждой формы орбитали существует (2l + 1) энергетически равноценных ориентации в пространстве.
Для s- орбитали (l = 0) такое положение одно и соответствует m = 0. Сфера не может иметь разные ориентации в пространстве.
Для p- орбитали (l = 1) - три равноценные ориентации в пространстве (2l + 1 = 3): m = -1, 0, +1.
Для d- орбитали (l = 2) - пять равноценных ориентаций в пространстве (2l + 1 = 5): m = -2, -1, 0, +1, +2.
Таким образом, на s- подуровне - одна, на p- подуровне - три, на d- подуровне - пять, на f- подуровне - 7 орбиталей.
Спиновое квантовое число (s) характеризует магнитный момент, возникающий при вращении электрона вокруг своей оси. Принимает только два значения +1/2 и –1/2 соответствующие противоположным направлениям вращения.
Энергетический уровень — это совокупность орбиталей, которые имеют одинаковые значения главного квантового числа. Число энергетических уровней атома равно номеру периода, в котором он расположен. Например,калий(К) -элемент четвертого периода, имеет 4 энергетических уровня (n = 4).
Энергетический подуровень — совокупность орбиталей с одинаковыми значениями главного и орбитального квантовых чисел. Энергетический подуровень обозначается латинскими буквами: s, p, d, f и т. д. Например, n = 2,1 = 0,1. Значит, на 2 уровне есть подуровень s (1 = 0) и подуровень р (1 = 1).
1. Принцип Паули. В атоме не может быть двух электронов, у которых значения всех квантовых чисел (n, l, m, s) были бы одинаковы, т.е. на каждой орбитали может находиться не более двух электронов (c противоположными спинами).
2. Правило Клечковского (принцип наименьшей энергии). В основном состоянии каждый электрон располагается так, чтобы его энергия была минимальной. Чем меньше сумма (n + l), тем меньше энергия орбитали. При заданном значении (n + l) наименьшую энергию имеет орбитальс меньшим n. Энергия орбиталей возрастает в ряду:
1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 5d > 4f < 6p < 7s.
3. Правило Хунда. Атом в основном состоянии должен иметь максимально возможное число неспаренных электронов в пределах определенного подуровня.
Запись, отражающая распределение электронов в атоме химического элемента по энергетическим уровням и подуровням, называется электронной конфигурацией этого атома. В основном (невозбужденном) состоянии атома все электроны удовлетворяют принципу минимальной энергии. Это значит, что сначала заполняются подуровни, для которых:
1) Главное квантовое число n минимально;
2) Внутри уровня сначала заполняется s- подуровень, затем p- и лишь затем d-подуровень;
3) Заполнение происходит так, чтобы (n + l) было минимально (правило Клечковского);
4) В пределах одного подуровня электроны располагаются таким образом, чтобы их суммарный спин был максимален, т.е. содержал наибольшее число неспаренных электронов (правило Хунда).
5) При заполнении атомныхорбиталей выполняется принцип Паули. Его следствием является, что энергетическому уровню с номером n может принадлежать не более чем 2n 2 электронов, расположенных на n 2 подуровнях.
2.2
При электролизе расплава соли на катоде выделяется металл (уравнение 1). При горении натрия преимущественно образуется пероксид натрия (уравнение 2), который реагируете углекислым газом с выделением кислорода (уравнение 3). При нагревании раствора, содержащего NH4Cl (соль, образованная слабым основанием и сильной кислотой) и Na2C03 (соль, образованная сильным основанием и слабой кислотой), будет происходить гидролиз (уравнение 4).

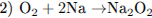
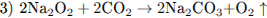
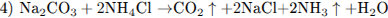
2.3
Билет 3.1. 
3.2
1) P₄ + 3KOH (конц.) + 3H₂O = 3KH₂PO₂ + PH₃ (газ)
2) 2PH₃ + 4O₂ = P₂O₅ + 3H₂O
3) P₂O₅ + 4NaOH = 2NaHPO₄ + H₂O
4) 2Na₂HPO₄ = Na₄P₂O₇ + H₂O
3.3
CaCO3 + 2HNO3 =Ca(NO3)2 + H2O + CO2
Состав конечного раствора после добавления CaCO3:
1. Н2О - она будет состоять из воды начального раствора азотной кислоты + вода образовавшияся в результате реакции
2. Ca(NO3)2 - образовавшийся в результате реакции
3. HNO3 - количество уменьшится на количество прореагировавшей с CaCO3 кислоты
Обозначим количество моль прореагировавшей кислоты через Х, концентрация кислоты в конечном растворе составляет 10/2=5%
4. Масса 1 моль HNO3=1+14+3*16=63 г
Масса 1 моль Ca(NO3)2=40+(14+3*16)*2=164 г
Масса 1 моль воды = 2*1+16=18 г
Масса 1 моль CaCO3= 40+12+3*16=100 г
5. Составим уравнение
(250*0,1-63*х) /(250+164*х/2+18*х/2-63*х=0,05
Решая уравнение получим 64,4*х=12,5, т. е. х=0,1941 моль HNO3 прореагировали в результате реакции.
По уравнению реакции количество моль CaCO3 реагирущее с 2 моль HNO3 равно 1, следовательно масса карбоната кальция, которое необходимо для получения 5% конечноного раствора азотной кислоты= 0,1941/2*100=9,705 г
Билет 4
Классификация химических соединений ,закномоерность протекания химических реакций
Тепловой эффект
Химическая реакция-разрыв связи продуктов реакции и образование новых связей в продуктах реакции
Химическая реакция- процесс превращения веществ связанных с превращением энергии, сопровождающейся образованиями новых веществ с другими свойствами
Признаки классификации
1.Число и состав исходных и образующих веществ
· Соединение
· Разложение
· Замещение
· Обмен
2. Тепловой эффект реакции
· Экзотермический (выделение теплоты)
· Эндотермический (поглащение теплоты
3. По степени окисления
· ОВР
· Не ОВР
4. Обратимость
· Обратимые
· Не обратимые
5.Наличие катализатора
· Каталитические
· Не каталитические
6. По агрегатному состоянию
· Гомогенные
· Гетерогенные
