Последовательность протекания электродных процессов
При электролизе
Характер процессов, происходящих при электролизе, зависит от многих факторов, важнейшими из которых являются природа электролита, материал анода, концентрация раствора электролита и режим электролиза (температура, напряжение, плотность тока и др.).
Учитывая влияние природы электролита на характер процессов электролиза, рассмотрим два принципиально различных варианта: электролиз расплава и электролиз раствора электролита.
9.2.1. Электролиз расплава электролита
При прохождении тока через расплав соли на катоде восстанавливаются катионы металла, на аноде окисляются анионы кислотного остатка соли.
Электролизом расплавов солей и гидроксидов получают металлы, имеющие сильно отрицательные значения Ео 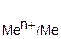 (Na, Al,Mg, Ca, Ni, Be и др.).
(Na, Al,Mg, Ca, Ni, Be и др.).
Например, при электролизе расплавов NaCl и NaОН протекают следующие процессы:
2NaCl расплав
↑↓
(−) K (Pt) 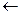 2Na+ + 2Cl
2Na+ + 2Cl 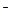
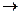 (Pt) А (+);
(Pt) А (+);
(−) K: 2Na+ + 2 
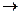 2Na (+) A: 2Cl
2Na (+) A: 2Cl 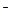
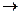 Cl2 + 2
Cl2 + 2  ;
;

2Na++2Cl 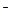 ↔ 2Na+Cl2.
↔ 2Na+Cl2.
4NaОНрасплав
↑↓
(−) K (Pt)  4Na+ + 4ОН
4Na+ + 4ОН 
 (Pt) А (+);
(Pt) А (+);
(−) K: 4Na+ + 4 
 4Na (+) A: 4OH- ↔ 2Н2О + O2
4Na (+) A: 4OH- ↔ 2Н2О + O2  + 4
+ 4  ;
;
 |
4Na+ + 4ОН 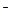 ↔ 4Na + 2Н2О + О2.
↔ 4Na + 2Н2О + О2.
Если расплав состоит из нескольких солей, очередность разрядки катионов и анионов определяется значениями их стандартных электродных потенциалов (см. прил., табл. 13). Чем больше величина стандартного электродного потенциала металла, тем выше окислительная способность ионов этого металла, тем легче разряжаются катионы. Например, при одновременном присутствии в расплаве катионов Zn2+, Pb2+, Cu2+ в равных концентрациях на катоде в соответствии со значениями их стандартных электродных потенциалов (ЕоZn2+/Zn =−0,76 B; ЕоPb2+/Pb =−0,13 B; ЕоCu2+/Cu = +0,34 B) сначала выделится медь, затем – свинец и в конце процесса – цинк.
Окисление на аноде протекает тем легче, чем ниже значение стандартного электродного потенциала аниона. Например, при одновременном присутствии в расплаве анионов Cl-, J-, SO 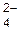 в равных концентрациях (стандартные электродные потенциалы которых соответственно равны +1,36 В; +0,53 В; +2,05 В) первоначально будут окисляться анионы J-, затем – Cl- и наконец – SO
в равных концентрациях (стандартные электродные потенциалы которых соответственно равны +1,36 В; +0,53 В; +2,05 В) первоначально будут окисляться анионы J-, затем – Cl- и наконец – SO 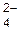 .
.
9.2.2. Электролиз раствора электролита
При электролизе водных растворов электролитов в процессе принимают участие не только молекулы электролитов, но и молекулы растворителя – воды.
Протекание того или иного электрохимического процесса у электродов при электролизе прежде всего будет зависеть от относительных значений электродных потенциалов соответствующих электрохимических систем. Из нескольких возможных процессов преимуществом обладает тот, осуществление которого сопряжено с минимальной затратой энергии. Это означает, что на катоде будут восстанавливаться окисленные формы электрохимических систем с наибольшим значением электродного потенциала, а на аноде будут окисляться восстановленные формы систем с наименьшим значением электродного потенциала.
Катодные процессы. При электролизе водного раствора электролита на катоде протекают два взаимно конкурирующих процесса:
1. Восстановление катионов металла:
Меn+ + n  ↔ продукты.
↔ продукты.
2. Электрохимическое разложение воды в соответствии с уравнением
2H2O + 2  ↔ H2
↔ H2  + 2OH
+ 2OH 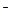 (рН
(рН 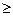 7), Е
7), Е 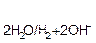 =−0,059рН.
=−0,059рН.
Электрохимическое выделение водорода происходит из кислотных растворов (рН<7) вследствие разряда ионов водорода в соответствии с уравнением
2Н+ + 2  ↔ H2
↔ H2  , Е
, Е 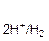 =−0,059рН.
=−0,059рН.
Вопрос о том, какой из катодных процессов обладает преимуществом, определяется величинами стандартных электродных потенциалов окисленных форм электрохимических систем, концентрацией раствора электролита, условиями электролиза (плотность тока, температура).
Все окислители, которые восстанавливаются на катоде при электролизе, по величине их стандартных потенциалов подразделяются на три группы:
I группа – окислители, стандартный потенциал которых более положителен, чем потенциал стандартного водородного электрода (Cu2+, Ag+, Hg2+, Au3+, O2, J2, Br2, Cl2, PbO2, MnO4- и др.). Они восстанавливаютсяна катоде в первую очередь в порядке уменьшения электродного потенциала. Восстановление ионов водорода или молекул воды не происходит.
II группа – окислители от (от Li+ до Al3+ включительно), стандартный потенциал которых более отрицателен, чем потенциал стандартного водородного электрода, не могут быть восстановлены электролизом из растворов солей, на катоде в этом случае восстанавливается водород в кислотной среде, а в водных растворах в первую очередь восстанавливаются молекулы воды.
III группа – окислители, имеющие стандартный электродный потенциал меньший, чем у водорода, но больший чем у алюминия (Mn2+, Zn2+, Cr3+, Fe2+, Cd2+, Co2+, Ni2+, Sn2+, Pb2+). В зависимости от условий проведения электролиза (рН раствора, плотности тока, перенапряжения и др.) возможно преимущественное восстановление молекул воды (в кислотных растворах ионов водорода) или этих окислителей, в противном случае протекает их одновременное восстановление на катоде.
III группа – окислители, имеющие стандартный электродный потенциал меньший, чем у водорода, но больший чем у алюминия (Mn2+, Zn2+, Cr3+, Fe2+, Cd2+, Co2+, Ni2+, Sn2+, Pb2+). В зависимости от условий проведения электролиза (рН раствора, плотности тока, перенапряжения и др.) возможно преимущественное восстановление молекул воды (в кислотных растворах ионов водорода) или этих окислителей, в противном случае протекает их одновременное восстановление на катоде.
| Катодные процессы | ||
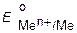 < < 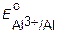 | 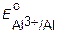 < <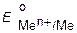 < < 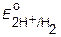 | 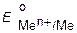 > > 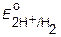 |
| Li+, K+, Na+, Mg2+, Al3+ и др. | Mn2+, Zn2+, Cr 3+, Fe2+, Cd2+, Co2+, Ni2+, Sn2+, Pb2+ | Cu2+, Ag+ …Au3+, O2, J2 , Br2, MnO4- |
2Н2О +2 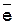 ↔H2↑+2OН- (рН ↔H2↑+2OН- (рН 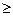 7); 2H+ + 2 7); 2H+ + 2 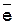 ↔ H2↑ (рН < 7) ↔ H2↑ (рН < 7) | Ме ↔ Men+ + n 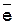 2Н2О +2 2Н2О +2 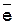 ↔H2↑+2OН- (рН ↔H2↑+2OН- (рН 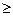 7); 2H++2 7); 2H++2 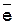 ↔ H2↑(рН < 7) ↔ H2↑(рН < 7) | Ме ↔ Men+ + n 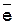 Ox + n Ox + n 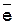 ↔ Red ↔ Red |
Если водный раствор содержит катионы различных металлов в равных концентрациях, то при электролизе выделение их на катоде будет протекать в порядке уменьшения величины стандартного электродного потенциала соответствующего металла. Так, из смеси катионов Ag+, Cu2+, Fe2+ сначала будут восстанавливаться катионы Ag+(ЕO 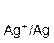 =+0,80 B), затем Cu2+(ЕO
=+0,80 B), затем Cu2+(ЕO 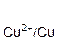 = +0,34 B) и Fe2+ (ЕO
= +0,34 B) и Fe2+ (ЕO 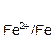 =−0,44 B) .
=−0,44 B) .
Анодные процессыпри электролизе растворов в значительной мере зависят от материала анода. При этом возможны два принципиально различных случая: первый – анод выполнен из инертных материалов (уголь, графит, платина) – электролиз с нерастворимым анодом и второй – анод выполнен из материала, окисляющегося в ходе электролиза, – электролиз с растворимым анодом.
| Анодные процессы | |
| Нерастворимый (инертный) анод | Растворимый анод |
| 1. Окисление бескислородных анионов J-, Br-, Cl- | 1. Растворение анода Ме ↔ Men+ + n 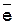 |
2. Электрохимическое окисление воды в зависимости от характера среды 4ОН- ↔ 2 Н2О + О2↑ + 4 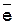 (рН (рН 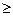 7) 2 Н2О ↔ О2 ↑+ 4Н+ + 4 7) 2 Н2О ↔ О2 ↑+ 4Н+ + 4 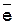 (рН < 7) (рН < 7) | 2. Электрохимическое окисление воды в зависимости от характера среды 4ОН- ↔ 2 Н2О + О2↑ + 4 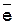 (рН (рН 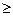 7) 2 Н2О ↔ О2 ↑+ 4Н+ + 4 7) 2 Н2О ↔ О2 ↑+ 4Н+ + 4 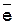 (рН < 7) (рН < 7) |
| 3. Окисление бескислородных анионов в порядке возрастания Ео - J-, Br-, Cl- | |
4. Окисление анионов SO 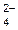 , NO , NO 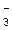 , СO , СO 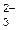 |
Электролиз с нерастворимым анодом.При электролизе водных растворов электролитов с нерастворимым анодом характер
анодного процесса определяется исходя из значений стандартных электродных потенциалов анионов солей и электрохимического окисления воды с выделением кислорода.
Электрохимическое окисление воды зависит от характера среды и протекает в соответствии с уравнениями:
2H2O ↔ O2 + 4H+ + 4  , (рН
, (рН 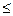 7); Е
7); Е 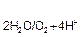 =1,23−0,59рН В.
=1,23−0,59рН В.
4ОН 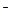 ↔ O2 + 2H2O + 4
↔ O2 + 2H2O + 4  , (рН > 7); Е
, (рН > 7); Е 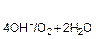 =1,23−0,59рН В.
=1,23−0,59рН В.
Из сопоставления величин электродных потенциалов соответствующих электрохимических систем становится очевидным
процесс электрохимического разложения воды.
Рассмотрим некоторые примеры электролиза водных растворов с нерастворимым анодом.
Пример 1.
2NaCl + 2Н2О
↑↓
(−) K (Pt)  2Na+ + 2Cl
2Na+ + 2Cl 
 (Pt) А (+);
(Pt) А (+);
(−) К: 2Н2О + 2  ↔ Н2
↔ Н2  +2ОН- (+) А: 2Cl
+2ОН- (+) А: 2Cl  ↔Cl2 +2
↔Cl2 +2  ;
;

2NaCl + 2Н2О ↔ Н2  + Cl2 + 2NaОН.
+ Cl2 + 2NaОН.
Пример 2.
К2SO4 + Н2О
↑↓
(−) K (Pt)  2K+ + SO42
2K+ + SO42 
 (Pt) А (+);
(Pt) А (+);
(−) К: 2Н2О +2  ↔ Н2
↔ Н2  + 2ОН- (+) А: 2Н2О ↔ O2
+ 2ОН- (+) А: 2Н2О ↔ O2  + 4H++ 4
+ 4H++ 4  ;
;

2Н2О ↔ 2Н2  + O2
+ O2  .
.
Пример 3.
4КOH + Н2О
↑↓
(−)K (Pt)  4K+ + 4OH
4K+ + 4OH 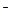
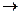 (Pt) А (+);
(Pt) А (+);
(−) К: 4Н2О + 4  ↔ Н2
↔ Н2  +4ОН- (+) А: 4OH- ↔2Н2О + O2
+4ОН- (+) А: 4OH- ↔2Н2О + O2  + 4
+ 4  ;
;

2Н2О ↔ 2Н2  + O2
+ O2  .
.
Аналогично происходит электролиз водных растворов NaOH, Na2SO4, NaNO3 и кислородосодержащих кислот. При электролизе разлагается вода:
2Н2О ↔ 2Н2  + O2
+ O2  .
.
Пример 4.
Н2SO4 + Н2О
↑↓
(−) K (Pt) 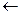 2Н+ + SO
2Н+ + SO 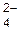
 (Pt) А (+);
(Pt) А (+);
(−) К: 4Н+ + 4  ↔ 2Н2
↔ 2Н2  (+) А: 2Н2О ↔ O2
(+) А: 2Н2О ↔ O2  + 4H++ 4
+ 4H++ 4  ;
;

2Н2О ↔ 2Н2  + O2
+ O2  .
.
Пример 5.
ZnSO4 + Н2О
↑↓
(−) K (Pt)  Zn2+ + SO
Zn2+ + SO 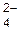
 (Pt) А (+);
(Pt) А (+);
(−) К: Zn2+ + 2  ↔ Zn (+) А: 2Н2О ↔O2
↔ Zn (+) А: 2Н2О ↔O2  +4H++ 4
+4H++ 4  ;
;
2Н2О + 2  ↔ Н2
↔ Н2  + 2ОН-
+ 2ОН-

ZnSO4 + 2Н2О ↔ Zn + 2Н2  + O2
+ O2  + H2SO4.
+ H2SO4.
Пример 6.
CuSO4 + Н2О
↑↓
(−) K (Pt)  Cu2+ + SO
Cu2+ + SO 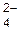
 (Pt) А (+);
(Pt) А (+);
(−) К: Cu2+ + 2  ↔Cu (+) А: 2Н2О ↔O2
↔Cu (+) А: 2Н2О ↔O2  + 4H++ 4
+ 4H++ 4  ;
;

2CuSO4 + 2Н2О ↔ 2Cu + O2  + 2H2SO4.
+ 2H2SO4.
Пример 7.
HCl + Н2О
↑↓
(−) K (Pt)  H+ + Cl
H+ + Cl 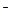
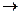 (Pt) А (+);
(Pt) А (+);
(−) К: 2Н++ 2  ↔ Н2
↔ Н2  (+) А: 2Cl
(+) А: 2Cl 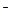 ↔ Cl2 +2
↔ Cl2 +2  ;
;

2HCl ↔ Н2  + Cl2.
+ Cl2.
При высоких плотностях тока на катоде идет выделение Cl2, при малых – О2↑.
Электролиз с растворимым анодом. В этом случае источником электронов, поступающих с анода во внешнюю цепь, может быть металл, из которого выполнен анод.
Переход электронов с анода во внешнюю цепь смещает вправо равновесие, существующее между металлом – электродом и раствором:
Мео электрод 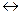 Меn+раствор + n
Меn+раствор + n  внешняя цепь,
внешняя цепь,
благодаря чему анод растворяется.
Таким образом, число конкурирующих окислительных процессов возрастает до трех:
1) электрохимическое окисление воды с выделением кислорода;
2) окисление аниона электролита;
3) электрохимическое окисление металла − материала анода (анодное растворение металла).
Из этих возможных процессов будет осуществляться энергетически наиболее выгодный.
Например, в случае электролиза раствора хлорида меди, осуществляемого с медным анодом, возможны следующие процессы:
2Сl 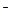
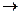 Cl
Cl 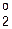 + 2
+ 2  ; Ео =+1,36 В,
; Ео =+1,36 В,
2H2O 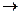 O2 + 4H+ + 4
O2 + 4H+ + 4  ; Ео =+1,23 В,
; Ео =+1,23 В,
Сuо 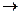 Сu2+ + 2
Сu2+ + 2  ; Ео =+0,34 В.
; Ео =+0,34 В.
Из сопоставления величин электродных потенциалов соответствующих электрохимических систем можно сделать вывод о преимущественном протекании процесса окисления меди из общего числа рассматриваемых. Таким образом, при электролизе раствора хлорида меди, проводимом с медным анодом, происходит растворение меди на аноде и выделение ее на катоде:
CuCl2 + Н2О
↑↓
(−) K (Cu) 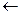 Cu2+ + 2 Cl
Cu2+ + 2 Cl 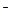
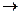 (Cu) A (+);
(Cu) A (+);
(−) К: Cu2+ + 2  ↔ Cu (+) А: Cu ↔ Cu2+ + 2
↔ Cu (+) А: Cu ↔ Cu2+ + 2  .
.
