К выполнению контрольной работы №1
по дисциплине «Материаловедение»
| т,°с |
А) Вычертить диаграмму состояния сплавов системы «свинец Pb – олово Sn» (рис. П.5). Указать основные линии, точки, а также структурно-фазовый состав всех областей диаграммы. Для сплава, содержащего 20% олова Sn, построить кривую охлаждения и описать происходящие при охлаждении фазовые превращения. Для данного сплава определить количественное соотношение структурно-фазовых составляющих и их состав при температуре 250ºC и схематично изобразить его структуру.
| 327°С |
10 20 30 40 50 60 70 80 90 100% Sn
РЬ 100% 90 80 70 60 50 40 30 20 10 0
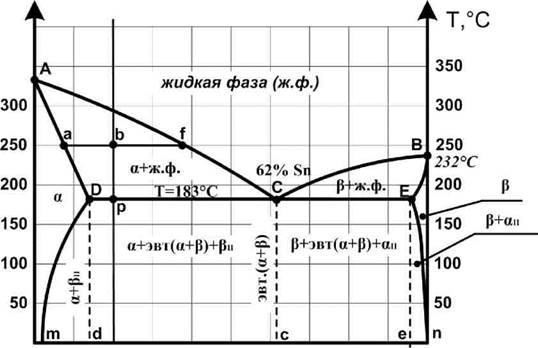
Рис. 1. Диаграмма состояния сплавов системы «свинец Pb - олово Sn»
Диаграмма состояния сплавов системы «свинец Pb - олово Sn» (рис. 1) относится к разновидности диаграмм состояния двойных сплавов III типа, является диаграммой состояния сплавов, испытывающих фазовые превращения в твёрдом состоянии (диаграмма состояния сплавов с переменной растворимостью компонентов в твёрдом состоянии). По внешнему виду диаграмма похожа на диаграмму состояния сплавов с ограниченной растворимостью компонентов в твёрдом состоянии. Отличие только состоит в том, что линии предельной растворимости компонентов не перпендикулярны оси концентрации. На диаграмме имеются области, в которых из однородных твёрдых растворов при понижении температуры выделяются вторичные фазы. Поэтому данный тип диаграммы характерен для сплавов, образующих при сплавлении компонентов твёрдые растворы, имеющих ограниченную взаимную растворимость друг в друге, изменяющуюся с изменением температуры.
Основные линии диаграммы:
ACB — линия ликвидус, линия начала процесса кристаллизации;
ADCEB — линия солидус, линия конца процесса кристаллизации;
Dm — линия переменной предельной растворимости олова Sn в свинце Pb;
En — линия переменной предельной растворимости свинца Pb в олове Sn;
DCE — линия кристаллизации эвтектики (T = 183ºC).
Основные точки диаграммы:
A — температура кристаллизации чистого свинца Pb (T = 327ºC);
B — температура кристаллизации чистого олова Sn (T = 232ºC);
C — температура кристаллизации эвтектического сплава 62% Sn + 38% Pb (T = 183ºC);
D — максимальная предельная растворимость олова Sn в свинце Pb (13% олова Sn в 87% свинца Pb при T = 183ºC);
E — максимальная предельная растворимость свинца Pb в олове Sn (4% свинца Pb в 96% олова Sn при T = 183ºC).
На диаграмме условно обозначены следующие фазы:
α — твёрдый раствор олова Sn в основном компоненте-растворителе свинце Pb;
β — твёрдый раствор свинца Pb в основном компоненте-растворителе олове Sn.
Из данной диаграммы видно, что с понижением температуры растворимость олова Sn в свинце Pb и, соответственно, свинца Pb в олове Sn (линии Dm и En соответственно) уменьшаются. Вследствие этого из твёрдых растворов выделяются избыточные фазы, то есть в сплаве образуются равномерно распределённые зоны, содержащие избыточное количество растворённого компонента. Таким образом, из α-твёрдого раствора, например, выделяются вторичные кристаллы β-твёрдого раствора (β II) переменного состава; из β-твёрдого раствора — вторичные кристаллы α-твёрдого раствора (αII). Составы этих вторичных кристаллов определяются соответственно линиями Dm и En.
Причинами выделения вторичных фаз (αII и βII) в сплавах в твёрдом состоянии при понижении температуры являются:
1) изменение параметров кристаллических решёток основных компонентов-растворителей;
2) изменение типов кристаллических решёток сплавляемых компонентов при понижении температуры (полиморфное превращение), что приводит к изменению растворяющей способности.
Сплавы составов левее точки m состоят из однородного α-твёрдого раствора — твёрдого раствора олова Sn в основном компоненте-растворителе свинце Pb, а сплавы стоящие правее точки n — из однородного β-твёрдого раствора — твёрдого раствора свинца Pb в основном компоненте-растворителе олове Sn.
Сплавы составов от точки m до точки d имеют микроструктуру, состоящую из кристаллов α-твёрдого раствора переменного состава и вторичных кристаллов β II-твёрдого раствора, а от точки e до точки n — из кристаллов β-твёрдого раствора переменною состава и вторичных кристаллов α II-твёрдого раствора.
На диаграмме также можно выделить следующие сплавы:
Эвтектический сплав (эвтектика). На диаграмме данный сплав соответствует проекции точки С на ось концентраций, содержит 62% олова Sn и 38% свинца Pb. Этот сплав начинает кристаллизоваться при самой низкой температуре 183ºC среди всех сплавов рассматриваемой системы; имеет при понижении температуры постоянный количественный состав компонентов; структура его в твёрдом состоянии представляет собой мелкодисперсную механическую смесь кристаллов α- и β-твёрдых растворов переменного состава.
Доэвтектические сплавы, имеющие состав от точки d до точки c состоят из первичных кристаллов α-твёрдого раствора, эвтектики (α + β) и мелких вторичных кристаллов β II-твёрдого раствора, выделившихся из твёрдой фазы при понижении температуры. Первичные кристаллы α-твёрдого раствора равномерно распределены в эвтектике (α + β). Доэвтектические сплавы начинают кристаллизоваться с выделения из жидкой фазы кристаллов α-твёрдого раствора переменного состава (область диаграммы ADC, лежащая между линиями ликвидус и солидус).
Заэвтектические сплавы, имеющие состав от точки c до точки e, состоят из первичных кристаллов β-твёрдого раствора, эвтектики (а + β) и мелких вторичных кристаллов α II-твёрдого раствора, выделившихся из твёрдой фазы при понижении температуры. Первичные кристаллы β-твёрдого раствора равномерно распределены в эвтектике (α + β). Заэвтектические сплавы начинают кристаллизоваться с выделения из жидкой фазы кристаллов β-твёрдого раствора переменного состава (область диаграммы CEB, лежащая между линиями ликвидус и солидус).
Таким образом, в структурно-фазовом составе сплавов рассматриваемой системы важное место занимает эвтектика, представляющая собой смесь мелкодисперсных фаз α и β. Она имеет постоянный количественный состав компонентов (Pb и Sn) и кристаллизуется при наименьшей для данной системы сплавов температуре tэ = 183ºC, т. е. температуре, соответствующей линии DCE. Ниже этой линии находится область двухфазных сплавов.
Выше линии ликвидус (линии ACB) сплавы представляют собой жидкие фазы — неограниченные растворы компонентов (свинца Pb и олова Sn) друг в друге в жидком состоянии.
Для диаграмм состояния сплавов III типа характерно то, что кристаллы сплавляемых компонентов в чистом виде ни в одном из сплавов системы не присутствуют.
Рассмотрим процесс кристаллизации сплава, содержащего 80% Pb и 20% Sn (рис. 2, 3).
| Т,°С |
| 327°С |
 0 10 20 30 40 50 60 70 80 90 100% Sn РЬ 100% 90 80 70 60 50 40 30 20 10 0 Кривая охлаждения двойного t, МИН
0 10 20 30 40 50 60 70 80 90 100% Sn РЬ 100% 90 80 70 60 50 40 30 20 10 0 Кривая охлаждения двойного t, МИН
сплавa «80%Pb+20%Sn»
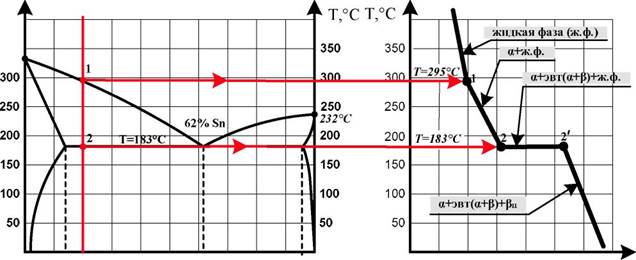
Рис. 2. Построение кривой охлаждения сплава «80% Pb + 20% Sn»
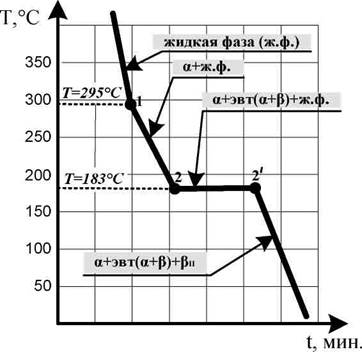
Рис. 3. Кривая охлаждения сплава «80% Pb + 20% Sn»
Построение кривой охлаждения сплава «80% Pb + 20%Sn» проводится в следующей последовательности:
а) через точку оси абсцисс, соответствующую составу сплава «80% Pb + 20%Sn», проводится вертикаль — линия сплава (рис. 1, 2);
б) точки пересечения линии сплава с линиями диаграммы обозначаются цифрами (рис. 2). Это — критические точки, указывающие критические температуры начала и конца процесса кристаллизации, перекристаллизации (если она имеется) данного сплава;
в) в соответствии с выявленными критическими температурами строится кривая охлаждения сплава в координатах «температура - время» (рис. 2, 3).
Согласно представленной на рис. 3 кривой охлаждения при кристаллизации сплава «80% Pb + 20%Sn» происходят следующие структурно-фазовые превращения.
При температуре выше точки 1 (T = 295ºC) сплав находится в жидком состоянии (жидкая фаза) и представляется собой неограниченный раствор компонентов (Pb и Sn) друг в друге. Соответственно, точка 1, лежащая на линии ликвидус A C, — температура начала кристаллизации данного сплава.
При охлаждении сплава ниже температуры точки 1 из жидкой фазы начинают выделяться кристаллы α-твёрдого раствора — кристаллы твёрдого раствора олова Sn в основном компоненте-растворителе свинце Pb состава, соответствующему абсциссе точки a, лежащей на линии солидус (линии ADCEB) диаграммы. Таким образом, при понижении температуры количественный состав выделяющихся из жидкой фазы первичных кристаллов α-твёрдого раствора изменяется по линии AD от точки A до D. При этом характер хода кривой охлаждения изменяется, процесс охлаждения замедляется, что вызвано выделением скрытой теплоты кристаллизации при образовании кристаллов α-твёрдого раствора из жидкой фазы. Поэтому на кривой охлаждения наблюдается излом (участок 1 - 2). Фазовый состав сплава на участке 1 - 2 кривой охлаждения — жидкая фаза + первичные кристаллы α-твёрдого раствора.
При достижении температуры точки 2 (T = 183ºC, линия DCE диаграммы) возникает нонвариантная система (количество степеней свободы системы C = 0). То есть количество независимых внутренних и внешних параметров системы (температура, давление, концентрация), которые можно произвольно изменять без изменения количества фаз (равновесия) в системе, равно нулю. В данном случае при T = 183ºC (точка 2) в равновесии находятся одновременно три фазы:
1) жидкая фаза, соответствующая количественному составу точки C диаграммы (62% Sn + 38% Pb);
2) кристаллы α-твёрдого раствора, количественного состава, соответствующего точке D диаграммы (13% Sn + 87% Pb);
3) кристаллы β-твёрдого раствора, количественного состава, соответствующего точке E диаграммы (96% Sn + 4% Pb)
При температуре, соответствующей линии DCE — линии кристаллизации эвтектики (T = 183ºC), возникает эвтектическое превращение
LC → α d + βE .
Трём фазам соответствуют определённые количественные составы компонентов, характеризующиеся проекциями точек D, C и E, хотя температура их превращения постоянна.
При кристаллизации сплава между точками 2 и 2′ (T = 183ºC) кроме первичных кристаллов α-твёрдого раствора, образуется также эвтектика (α + β) — мелкодисперсная механическая смесь кристаллов α- и β-твёрдого раствора, количественного состава (62%Sn + 38% Pb). Температура кристаллизации эвтектики постоянна, независимо оттого, что дополнительной теплоты от внешней среды не поступает. Причиной постоянства температуры кристаллизации эвтектики также является выделение скрытой теплоты кристаллизации. В точке 2 эвтектика полностью находится ещё в жидком состоянии, между точками 2 и 2′ — в жидком и твёрдом состояниях, в точке 2′ — полностью в твёрдом состоянии. На участке 2 - 2′ кривой охлаждения фазовый состав сплава — первичные кристаллы α-твёрдого раствора, эвтектика (α + β) и жидкая фаза. В точке 2′ сплав полностью переходит в твёрдое состояние.
При дальнейшем охлаждении сплава ниже точки 2′ из первичных кристаллов α-твёрдого раствора выделяются вторичные кристаллы βII-твёрдого раствора. При обычных температурах кристаллы α-твёрдого раствора сплава имеют количественный состав компонентов, соответствующий точке m диаграммы (2,5%Sn + 97,5% Pb), а кристаллы βII-твёрдого раствора — соответствующий точке n диаграммы (99%Sn + 1% Pb). Причиной выделения вторичных кристаллов βII-твёрдого раствора из α-твёрдого раствора являются: 1) изменение параметров кристаллической решётки компонента-растворителя (свинца Pb), что приводит к снижению его растворяющей способности; 2) структурно-фазовые (полиморфные) превращения кристаллических решёток сплавляемых компонентов, что также приводит к снижению их взаимной растворимости друг в друге.
Окончательно охлаждённый сплав содержит только две фазы — кристаллы
α-твёрдого раствора и кристаллы β-твёрдого раствора. Каждый из этих видов кристаллов содержится как в мелкодисперсном состоянии в составе эвтектики (α + β), так и в виде более крупных фаз — α и β, равномерно распределённых по объёму сплава.
Для определения количественного соотношения структурно-фазовых составляющих при температуре 250ºC для сплава, содержащего 20% Sn и 80%
Pb, надо воспользоваться «правилом отрезков».
Для этого в замкнутой области ADC диаграммы на уровне температуры 250ºC проведём горизонтальную линию — коноду abf (рис. 1). Данная линия пересекает вертикальную линию, характеризующую состав сплава (линию сплава), в точке b.
Количество твёрдой фазы Qтв. (количество выпавших кристаллов α-твёрдого раствора) при T = 250ºC определим из соотношения:
Q me = (bf/ af) х100% =58,06% .
Таким образом, количество твёрдой фазы Qтв. определяется отношением длины отрезка горизонтали (коноды), прилегающего к линии ликвидус ACB, ко всей длине горизонтали.
Количество жидкой фазы Qж при T = 250ºC определим из соотношения:
Qж = (af/аf) х 100% = 41,94%.
Количество жидкой фазы Qж определяется отношением длины отрезка горизонтали (коноды), прилегающего к линии солидус ADCEB, ко всей длине горизонтали.
Количественный состав выделяющихся при кристаллизации сплава первичных кристаллов α-твёрдого раствора при T = 250ºC определяется абсциссой точки a — 8% Sn + 92% Pb.
Количественный состав жидкой фазы при T = 250ºC определяется абсциссой точки f — 38% Sn + 62% Pb.
Количество образующейся эвтектики при T = 183ºC в точке 2′ составит:
Qэвт = (Dp/ DC) х 100% = 14,3%
Количество образующихся первичных кристаллов α-твёрдого раствора при T = 183ºC составит:
Qтв.= (pC / DC ) х 100% = 85,7%
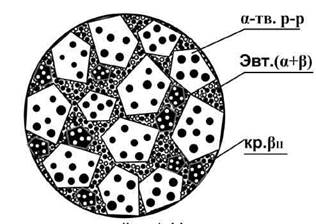 |

Рис. 4. Микроструктура сплава «80% Pb + 20% Sn»
Б) Вычертить диаграмму состояния сплавов системы «железо Fe-углерод C» (рис. П.7). Указать основные линии, точки и структурно-фазовый состав всех областей диаграммы. Для сплава, содержащего 1,2% углерода C, построить кривую охлаждения и описать происходящие при охлаждении структурно-фазовые превращения. Схематично изобразить и описать структуру заданного сплава.
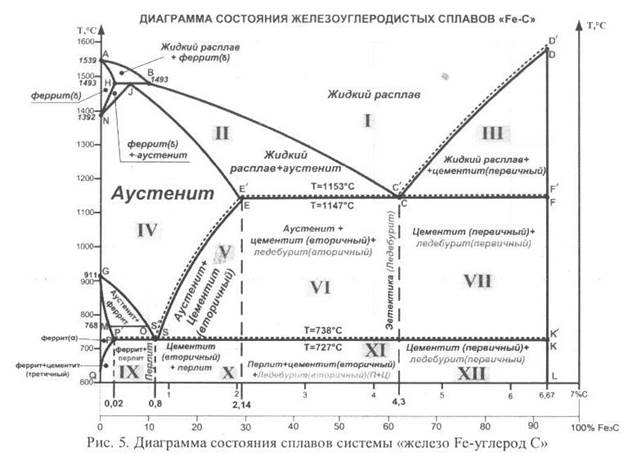
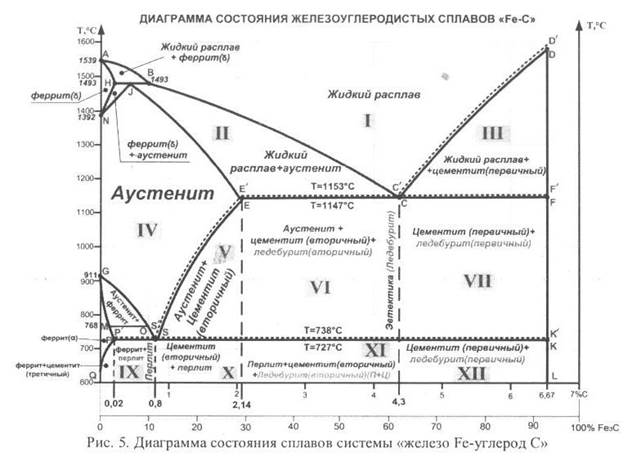
На диаграмме железоуглеродистых сплавов (рис. 5) нанесены сплошные и пунктирные линии. Это связано с тем, что углерод в сплавах может находиться как в свободном виде (в виде графита), так и в виде химического соединения (цементита Fe3C). Поэтому, диаграмма состояния железоуглеродистых сплавов может быть:
1) система «Fe-Fe3C» (метастабильная);
2) система «Fe-C» (стабильная).
Характерные точки диаграммы:
А (Т= 1539ºC) — температура плавления чистого железа Fe;
В (Т= 1493ºC; 0,5%С) — состав жидкой фазы при перитектической реакции;
J (Т= 1493ºC; 0,18%С) — состав аустенита при перитектической реакции;
Н (Т= 1493ºC; 0,1%С) — состав феррита при перитектической реакции;
N (Т= 1392ºC) — температура полиморфного превращения железа Feα ↔ Feγ;
С (Т= 1147ºC; 4,3%С) — состав эвтектики (ледебурит = аустенит + цементит);
D (Т= 1600ºC; 6,67%С) — условная температура плавления цементита Fe3С;
Е (Т= 1147ºC; 2,14%С) — предельная растворимость углерода в γ-железе Fe;
G (Т= 911ºC) — температура полиморфного превращения железа Feγ ↔ Feα;
S (Т= 727ºC; 0,80%С) — состав эвтектоидного сплава (перлит = феррит + цементит);
Р (Т= 727ºC; 0,02%С) — предельная растворимость углерода в α-железе Feα;
К (Т= 727ºC; 6,67%С) — состав цементита;
Q (Т= 20ºC; 0,006%С) — минимальная растворимость углерода в железе.
