При постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в степенях их стехиометрических коэффициентов
Химическая кинетика
Химическая кинетика – раздел химии, который изучает скорость и механизм химических реакций.
Основные задачи химической кинетики:
- выяснение факторов, влияющих на реакционную способность химических соединений;
- установление связи между свойствами химических соединений и их активностью в химических реакциях;
- описание механизма протекания химических реакций;
Предсказание скоростей химических реакций.
Скорость химической реакции - изменение концентрации реагирующих веществ в единицу времени в единице реакционного пространства.
Скорость химической реакции представляет собой число элементарных актов этой реакции в единицу времени в единице объёма для гомогенных реакций или на единице площади поверхности раздела фаз для гетерогенных реакций.
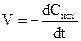 Выражения для скорости реакции:
Выражения для скорости реакции:
Сисх – концентрация исходных реагентов
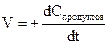 |
Спрод – концентрация продуктов реакции
Размерность скорости V - [моль/л×сек].
Знак минус связан с тем, что С для исходного реагента уменьшается во времени, а скорость реакции должна быть величиной положительной.
Факторы, влияющие на скорость химической реакции.
- Концентрация реагирующих веществ (закон действующих масс).
- Температура (правило Вант-Гоффа, уравнение Аррениуса).
- Природа реагирующих веществ.
- Катализатор.
- Площадь поверхности соприкосновения реагирующих веществ.
Зависимость скорости реакции от концентрации реагирующих веществ.
Закон действующих масс (К. Гульдберг-Вааге, 1867 г):
При постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в степенях их стехиометрических коэффициентов
Для реакции
А(г) + В(г) = АВ(г)
Кинетическое уравнение имеет вид:
V = k · CA · CB
V – скорость химической реакции
CA, CB –концентрации реагентов А и В
В общем случае для реакции:
a A + b B = cC + dD
Кинетическое уравнение имеет вид:
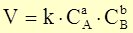 |
k – константа скорости реакции.
При этом концентрации твёрдых веществ считаются практически неизменными и в явном виде не включаются в выражение для скорости. Например, скорость реакции железа с соляной кислотой
Fe (тв) + 2HCl (р-р) = FeCl2 (р-р) + H2 (г)
выражается только через концентрацию кислоты:
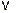 = k [HCl]2.
= k [HCl]2.
Величина k зависит от природы реагирующих веществ, от температуры, не зависит от концентрации реагентов.
Порядок реакции (n) – это эмпирическая величина, равная сумме показателей степеней, с которыми концентрации реагентов входят в выражение для скорости реакции:
n = a + b
Пример
1. В реакции, уравнение которой
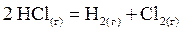 |
давление увеличили в 3 раза.
Во сколько раз возросла при этом скорость реакции?
Решение.
Кинетическое уравнение данной реакции:
V = k · C2 (HCl)
Обозначим: C (HCl) = х (начальная концентрация HCl),
скорость реакции: V1 = k·x 2.
При увеличении давления в 3 раза концентрация реагирующего вещества увеличилась тоже в 3 раза и составила 3x.
Скорость реакции при этом
V2 = k·(3x)2 = 9·k·x2 = 9· V1
Т.е. при увеличении давления в 3 раза скорость увеличилась в 9 раз.
Кинетическая классификация химических реакций.
* 1. По величине молекулярности
Молекулярность реакции- число молекул, участвующих в элементарном акте.
Реакции бывают мономолекулярные (одномолекулярные), бимолекулярные, тримолекулярные.
* 2. По величине порядка реакции:
- Реакции 1 порядка.
- Реакции 2 порядка.
- Реакции 3 порядка
Зависимость скорости реакции от температуры (правило Вант-Гоффа):
При увеличении температуры на 10 градусов скорость простой реакции возрастает в 2 – 4 раза.
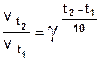
где 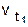 - скорость реакции при температуре t1,
- скорость реакции при температуре t1,
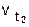 - скорость реакции при температуре t2 ,
- скорость реакции при температуре t2 ,
g - температурный коэффициент реакции.
Например, при повышении температуры от 20° до 60° скорость реакции, температурный коэффициент которой равен 3, возрастает в 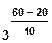 = 34 = 81 раз.
= 34 = 81 раз.
Пример (test)
Температурный коэффициент реакции = 2.
Как изменится скорость химической реакции при повышении температуры с 40 до 80 0С?
Решение:
По уравнению Вант-Гоффа:
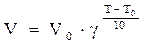 |
T-T0 = 80 – 40 = 40
V = V0 · 24 = V0 · 16.
Ответ: скорость реакции увеличится в 16 раз.
Из множества молекул при столкновении химически взаимодействуют только те, энергия которых не ниже энергии активации. Доля таких молекул, они называются активными, а также величина энергии активации (высота активационного барьера) определяют величину скорости химической реакции.
Уравнение Аррениуса:
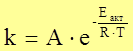 |
k – константа скорости химической реакции
Еакт – энергия активации
А – предэкспоненциальный множитель (частотный фактор).
Обратимые химические реакции. Химическое равновесие.
Химические реакции, которые в одних и тех же условиях могут идти в противоположных направлениях, называются обратимыми.
k1

 А + В D + E
А + В D + E
k 2
Реакция, протекающая слева направо – прямая (константа скорости - k1) ,
Реакция, протекающая справа налево – обратная (константа скорости – k2)
Протекание обратимых реакций завершается установлением химического равновесия.
В состоянии химического равновесия скорости прямой и обратной реакций равны
(V1 = V2), при этом концентрации компонентов будут постоянными.
Закон действующих масс для химического равновесия:
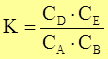 |
К – константа химического равновесия
Константа равновесия К – отношение произведения равновесных концентраций продуктов реакции в степенях, равных стехиометрическим коэффициентам, к произведению равновесных концентраций исходных веществ в степенях, равных стехиометрическим коэффициентам.
Например, для реакции в газовой фазе
2SO2 (г) + O2 (г) = 2SO3 (г)
константа равновесия имеет вид
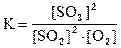 .
.
Следует учесть, что в случае гетерогенных равновесий, например,
MgSО3 (тв) = MgО (тв) + SО2 (г)
концентрации твёрдых веществ в явном виде не записывают в выражении для константы химического равновесия:
К = [SO2].
Смещение равновесия определяется принципом Ле Шателье:
Если на систему, находящуюся в равновесии, оказать внешнее воздействие, то равновесие смещается в таком направлении, которое ослабляет внешнее воздействие.
Так, нагревание смещает равновесие в сторону эндотермической реакции, происходящей с поглощением тепла. Охлаждение - в сторону экзотермической реакции, сопровождающейся выделением тепла.
Повышение давления вызывает смещение равновесия в сторону реакции, протекающей с уменьшением объёма или числа молей газообразных веществ. Напротив, понижение давления – в сторону реакции с увеличением объёма (числа молей газообразных веществ).
Увеличение концентрации исходных веществ сдвигает равновесие вправо, а увеличение концентрации продуктов взаимодействия – влево. В общем случае повышение концентрации какого-либо компонента реакционной системы смещает равновесие в сторону той реакции, в которой этот компонент расходуется.
Например, в системе
2SO2 (г) + O2 (г) = 2SO3 (г)
прямая реакция экзотермична, протекает с уменьшением числа молей газообразных веществ, из трёх молей исходных газов образуются два моля газообразного продукта. Поэтому для смещения равновесия слева направо, в сторону прямой реакции, необходимо понизить температуру по сравнению с равновесной, повысить давление и концентрации SO2 и О2 или понизить концентрацию SO3 (отводить его из сферы реакции по мере образования).
Примеры, иллюстрирующие принцип Ле-Шателье.
1. Для реакции, уравнение которой
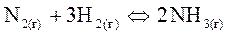 |
равновесие сместится вправо при увеличении давления, т.к. реакция протекает с уменьшением объёма или числа молей газообразных веществ (из 4 молей газообразных веществ образуется 2 моля).
В реакционной системе, уравнение которой
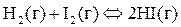 |
равновесие сместится вправо при увеличении концентрации иода
