Типы химических реакций. Составление уравнений реакций. 5 страница
В 1913 г. Бор предложил теорию строения водородного атома. Основными отличиями от предыдущей теории были следующие: электроны двигаются по строго определенным орбитам, до тех пор пока электрон находится на этой орбите, он не излучает. При переходе электрона с одной орбиты на другую выделяется энергия, что объясняет происхождение атомных спектров. Однако, теория Бора не пригодна к описанию строения сложных атомов.
Современная теория строения атома включает в себя квантово-механические представления: наличие у электрона свойств волны и частицы, невозможность одновременного определения координаты и импульса микрочастицы, применение волновой функции ψ для описания свойств электрона.
365. Атомная масса химического элемента рассчитывается как сумма вкладов атомных масс изотопов. Атомная масса хлора равна А(Cl) = 35*75.53%/100% + 37*24.47%/100% = 35.49 а.е.м.
366. Атомная масса химического элемента рассчитывается как сумма вкладов атомных масс изотопов. Атомная масса меди равна А(Cu) = 63*73%/100% + 65*27%/100% = 63.54 а.е.м. Результат не совпадает с табличным значением из-за т.н. «дефекта массы»: несовпадение значения суммы масс нуклонов и массы ядра, которое они составляют вследствие потери энергии.
367. Атомная масса химического элемента рассчитывается как сумма вкладов атомных масс изотопов. Атомная масса урана равна А(U) = 234*0.0058%/100% + 235*0.715%/100% + 238*99.28%/100% = 237.98 а.е.м. Результат не совпадает с табличным значением из-за т.н. «дефекта массы»: несовпадение значения суммы масс нуклонов и массы ядра, которое они составляют вследствие потери энергии.
368. Процессы взаимодействия ядер одних элементов с ядрами других элементов или с элементарными частицами, при которых образуются ядра новых элементов, получили название ядерных реакций. Ядерные реакции отличаются от химических тем, что в химических реакциях не происходит изменения ядерного состава. На Солнце протекает много ядерных реакций по суммарной схеме: 4р = α + 2е+ + 565 млн. ккал. Искусственно впервые осуществил ядерную реакцию Резерфорд (1919): 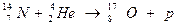 . В 1933 году Ирен и Фредерик Жолио-Кюри осуществили ядерную реакцию:
. В 1933 году Ирен и Фредерик Жолио-Кюри осуществили ядерную реакцию: 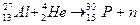
369. 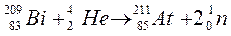
370. 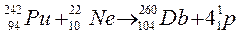
371. Спектры химических элементов получают путем сообщения атомам энергии, например в виде квантов света. При этом происходит возбуждение и переход электронов на более удаленные орбитали, возвращаясь с которых, они излучают. Таким образом получается линейчатый спектр испускания. Спектры имеют линейчатый вид, поскольку все переходы электронов дискретны, т.е. прерывисты. Спектр водорода состоит из трех серий: УФ - серии, серии Бальмера (видимый спектр) и ИК - серии. Перескокам с удаленных орбит на орбиту с n=1 соответствуют линии серии, лежащей в УФ-области, перескокам на орбиту с n=2 - линии серии Бальмера, перескокам на орбиты с n=3, 4, 5
              |
372.
              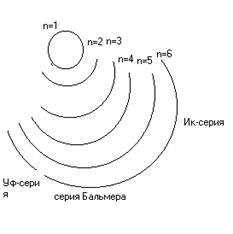 | Серим Лаймана соответствуют переходы с более удаленных орбиталей на орбиту с n=1. Серии Бальмера - переходы на n=2. Серии Пашена - переходы на орбиты с n=3,4,5. |
373. Для расчета энергии возбуждения электрона с одного уровня на другой используется уравнение: 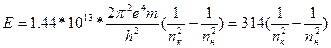 . Энергия перехода с 1 на 2 уровень равна 44 ккал/г-атом, Энергия перехода с 1 на 5 уровень равна 70 ккал/г-атом.
. Энергия перехода с 1 на 2 уровень равна 44 ккал/г-атом, Энергия перехода с 1 на 5 уровень равна 70 ккал/г-атом.
374. а) Принцип квантования и дискретности энергии: электрон не изменяет энергию непрерывно, переходя с одной орбиты на другую, изменение энергии электрона происходит скачкообразно. Т.е. энергетические состояния электрона в атоме дискретны.
б) Корпускулярно-волновая двойственность: электрон имеет свойства как частицы, так и волны.
в) Принцип неопределенности: нельзя одновременно и точно определить скорость электрона и его координаты.
Таким образом, электрон в атоме вращается по определенным орбитам с дискретной энергией. Поглощение или выделение энергии происходит только при переходе электрона с одной орбиты на другую.
375. Квантовая механика изучает движения и взаимодействия микрочастиц. Она основывается на представлении о квантовании энергии, волновом характере движения микрочастиц и вероятностном методе описания микрообъектов. Основным уравнением квантовой механики является волновое уравнение Шредингера, которое связывает волновую функцию с потенциальной полной энергией электрона. Волновые функции, получаемые решением этого уравнения, описывают орбитали.
376. Совокупность положений электрона в атоме, характеризуемых определенными значениями квантовых чисел называют атомной орбиталью.
377. а) Главное квантовое число (n) соответствует номеру энергетического слоя, в котором находится электрон.
б) Орбитальное квантовое число (l) определяет форму орбитали, форму электронного облака.
в) Магнитное квантовое число (m) определяет пространственную ориентацию орбиталей.
г) Спиновое квантовое число (s) определяет направление собственного вращения электрона.
378. Энергию электрона определяют главное, спиновое и магнитное квантовые числа. Наиболее существенно зависит энергия электрона от главного квантового числа, наименее - от магнитного. Магнитное квантовое число влияет на энергию электронов в пределах одного подуровня.
379. Энергетический уровень - набор атомных орбиталей с одинаковым значением главного квантового числа (n). Энергетический подуровень - набор атомных орбиталей с одинаковым значением орбитального квантового числа (l) внутри данного энергетического уровня. Число энергетических подуровней для данного энергетического уровня равно 2n2. Если энергетический уровень расщеплен на 4 подуровня, то n=2.
380.Электронный слой - это совокупность электронов с одинаковым значением главного квантового числа n. В электронном слое с n = 1 наибольшее количество содержащихся электронов - 2, в n = 2 - 8 электронов, в n = 3 - 18 электронов, в n = 4 - 32 электрона, в n = 5 - 50, в n = 6 - 72, в n = 7 - 98. Максимально теоретически допустимое количество электронов в слое равно 2n2.
381. Форму орбитали в пространстве определяет побочное квантовое число L. L принимает значения от 0 до (n - 1). Значению L=0 отвечает сферическая форма орбитали:  . Значению L=1 отвечает гантелеобразная форма орбитали:
. Значению L=1 отвечает гантелеобразная форма орбитали: 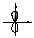 . Расположение орбиталей в пространстве определяет магнитное квантовое число ML. Например: гантелеобразные р-облака могут располагаться в пространстве тремя видами:
. Расположение орбиталей в пространстве определяет магнитное квантовое число ML. Например: гантелеобразные р-облака могут располагаться в пространстве тремя видами: 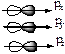
 . Размер орбиталей определяется главным квантовым числом n. Чем больше n, тем дальше внешние электроны находятся от ядра и тем больше электронное облако.
. Размер орбиталей определяется главным квантовым числом n. Чем больше n, тем дальше внешние электроны находятся от ядра и тем больше электронное облако.
382.Число атомных орбиталей (AO) определяется магнитным квантовым числом ML., оно равно (2L + 1). Так, на s-подуровне количество AO равно 1, т.к. для s-подуровня L=0. на р-подуровне число AO равно 3, т.к. L=1. На d-подуровне число AO равно 5, т.к. L = 2.
383. S-электронное облако имеет форму шара. Оно обладает сферической симметрией. Р-облако имеет гантелеобразную форму и обладает осевой симметрией. D-облака имеют форму скрещенных гантелей и осевую симметрию.
384. Фосфор, № 15. 1s22s22p63s23p3. Атом фосфора имеет в нормальном состоянии 3 неспаренных электрона на 3р-подуровне. При возбуждении электроны с 3s-подуровня распариваются, и один из них переходит на вакантную орбиталь d-подуровня, образуя при этом 5 неспаренных электронов.
 | валентные электроны | n | L | ML | S |
| 3s | +1/2 | ||||
| 3s | -1/2 | ||||
| 3p | +1 | +1/2 | |||
| 3p | +1/2 | ||||
| 3p | -1 | +1/2 |
385. Сера, № 16. 1s22s22p63s23p4. Атом серы имеет в нормальном состоянии 2 неспаренных электрона на 3р-подуровне. При возбуждении электроны с 3s- и 3р-подуровней могут распариваться, и переходить на вакантные орбитали d-подуровня, образуя при этом 4 или 6 неспаренных электронов.
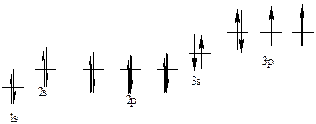 | Элек-троны | 3s | 3p | |||||
| Кв. числа | ||||||||
| N | ||||||||
| L | ||||||||
| M | -1 | -1 | +1 | |||||
| S | 1/2 | -1/2 | 1/2 | -1/2 | 1/2 | 1/2 |
386. Алюминий, № 13. 1s22s22p63s23p1. Атом алюминия имеет в нормальном состоянии 1 неспаренный электрон на 3р-подуровне. При возбуждении электрон с 3s-подуровня может распариться, и перейти на вакантную орбиталь 3d-подуровня, образуя при этом 3 неспаренных электрона.
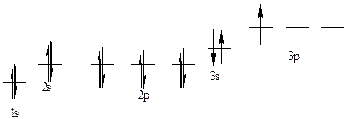 | Элек-троны | 3s | 3p | |||||
| Кв. числа | ||||||||
| N | ||||||||
| L | ||||||||
| M | -1 | |||||||
| S | 1/2 | -1/2 | 1/2 |
387. Кремний, № 14. 1s22s22p63s23p2. Атом кремния имеет в нормальном состоянии 2 неспаренных электрона на 3р-подуровне. При возбуждении электроны с 3s-подуровня могут распариваться, и переходить на вакантные орбитали d-подуровня, образуя при этом 4 неспаренных электрона.
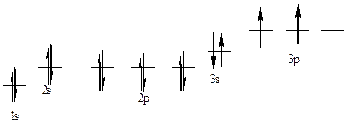 | Элек-троны | 3s | 3p | |||||
| Кв. числа | ||||||||
| N | ||||||||
| L | ||||||||
| M | -1 | |||||||
| S | 1/2 | -1/2 | 1/2 | 1/2 |
388. Хлор, № 17. 1s22s22p63s23p5. Атом хлора имеет в нормальном состоянии 1 неспаренный электрон на 3р-подуровне. При возбуждении электроны с 3s- и 3р-подуровней могут распариваться, и переходить на вакантные орбитали d-подуровня, образуя при этом 3, 5 или 7 неспаренных электронов.
 | Элек-троны | 3s | 3p | |||||
| Кв. числа | ||||||||
| N | ||||||||
| L | ||||||||
| M | -1 | -1 | +1 | |||||
| S | 1/2 | -1/2 | 1/2 | -1/2 | 1/2 | -1/2 | 1/2 |
389.Хром, № 24. 1s22s22p63s23p64s23d4. Атом хрома имеет в нормальном состоянии 4 неспаренных электрона на 3d-подуровне. При возбуждении электроны с 4s-подуровня могут распариваться, и переходить на вакантные орбитали 3d-подуровня, образуя при этом 6 неспаренных электронов.
 | Электроны | 4s | 3d | |||||||||
| Квантовые числа | ||||||||||||
| N | ||||||||||||
| L | ||||||||||||
| M | -2 | -1 | +1 | |||||||||
| S | 0.5 | -0.5 | 0.5 | 0.5 | 0.5 | 0.5 |
390. Ванадий, № 23. 1s22s22p63s23p64s23d3. Атом ванадия имеет в нормальном состоянии 3 неспаренных электрона на 3d-подуровне. При возбуждении электроны с 4s-подуровня могут распариваться, и переходить на вакантные орбитали 3d-подуровня, образуя при этом 5 неспаренных электронов.
 | Электроны | 4s | 3d | |||||||||
| Квантовые числа | ||||||||||||
| N | ||||||||||||
| L | ||||||||||||
| M | -2 | -1 | ||||||||||
| S | 0.5 | -0.5 | 0.5 | 0.5 | 0.5 |
391. Современная формулировка: Свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра элементов. Формулировка Менделеева: свойства элементов находятся в периодической зависимости от их атомных весов. Изменение формулировки произошло в связи с работами Мозли (1912 г.), который показал, что истинной основой закона являются не атомные веса, а положительные заряды ядер атомов, численно выражаемые (в е-единицах) атомными номерами соответствующих элементов.
392. Менделеев предсказал существование трех элементов: галлий, скандий, германий. Свойства элементов, предсказанные Менделеевым совпали очень точно, например, для германия:
| Предсказано Менделеевым (1871) | Найдено Винклером (1886) |
| Атомный вес ~72 Удельный вес ~5,5 Металл не вытесняет водород из кислот Оксид ЭО2 Удельный вес оксида 4.7 и др. | 72.6 5.35 металл не растворяется в HCl, H2SO4 GeO2 4.70 и др. |
393. В 1869 году истинную природу периодического изменения свойств элементов предсказать было невозможно, т.к. еще не была раскрыта структура атома. В настоящее время периодичность изменения свойств элементов связывается с ростом положительных зарядов ядер атомов. Поскольку атом электронейтрален, с ростом положительного заряда ядра увеличивается количество электронов, окружающих атом. Электроны заполняют оболочку последовательно - при этом свойства элементов также периодически изменяются.
394. Атомный номер элемента совпадает с количеством протонов в ядре атома элемента. С ростом атомного номера увеличивается положительный заряд ядра. Соответственно, увеличивается количество электронов, окружающих ядро. Электроны заполняют оболочку вокруг ядра строго последовательно. В связи с этим свойства атомов изменяются периодически.
395. Периодическая система является по отношению к периодическому закону графической формой. ПС содержит в себе громадное количество информации как явной, так и скрытой. Каждый вариант ПС - это способ наглядно представить ту или иную группу периодических свойств элементов.Короткопериодный вариант удобен своей компактностью. В нем наглядно показано как и почему различные элементы объединены в главные и побочные подгруппы. Однако, в короткопериодном варианте периодической системы нелогично разнесены в разные части таблицы d-металлы, разделенные группой благородных газов.Длиннопериодный вариант ПС наглядно представляет периоды, т.к. d-металлы находятся в логичном для них месте. Однако, в длиннопериодном варианте не ясно отражена связь между главными и побочными подгруппами элементов.
396. Короткопериодный вариант удобен своей компактностью. В нем наглядно показано как и почему различные элементы объединены в главные и побочные подгруппы. Однако, в короткопериодном варианте периодической системы нелогично разнесены в разные части таблицы d-металлы, разделенные группой благородных газов.
Длиннопериодный вариант ПС наглядно представляет периоды, т.к. d-металлы находятся в логичном для них месте. Однако, в длиннопериодном варианте не ясно отражена связь между главными и побочными подгруппами элементов.
397. Являющаяся наглядным выражением периодического закона, система элементов Д.И. Менделеева складывается из периодов и групп. Периодов в системе семь, из них три малых и четыре больших. Каждый период (кроме первого и последнего) включает в себя элементы, электронные структуры которых являются промежуточными между структурами двух последовательных инертных газов. Из малых периодов первый содержит только водород и гелий, остальные два - по 8 элементов. Из больших периодов четвертый и пятый содержат по 18 элементов, шестой - 32 элемента и седьмой остается незаконченным. Группы периодической системы объединяют входящие в них элементы по признаку химического сродства. Из них восьмая включает в себя инертные газы, а триады содержат только элементы, относящиеся к большим периодам. В каждой из остальных групп имеются по две подгруппы элементов больших периодов.
398. Элементы одного периода объединяет то, что их внешние (валентные) электроны находятся в одном электронном слое. Элементы одной группы сходны в количестве валентных электронов. Элементы одной группы, но разных подгрупп различаются тем, что они относятся к разным семействам. У элементов одного семейства общим является то, что последний электрон у атомов этих элементов находится на орбиталях с одинаковым орбитальным квантовым числом (l).
399. Периодическая система элементов Д.И. Менделеева складывается из периодов и групп. Периодов в системе семь, из них три малых и четыре больших. Каждый период (кроме первого и последнего) включает в себя элементы, электронные структуры которых являются промежуточными между структурами двух последовательных инертных газов. Из малых периодов первый содержит только водород и гелий, остальные два - по 8 элементов. Из больших периодов четвертый и пятый содержат по 18 элементов, шестой - 32 элемента и седьмой остается незаконченным. Группы периодической системы объединяют входящие в них элементы по признаку химического сродства. Из них восьмая включает в себя инертные газы, а триады содержат только элементы, относящиеся к большим периодам. В каждой из остальных групп имеются по две подгруппы элементов больших периодов. Т.о. емкость уровня совпадает с его заполненостью только для первого и второго периодов. В случае третьего и последующих периодов емкость больше количества элементов. Это связано со следующим явлением: из-за разницы в энергии d- и f-орбитали выталкиваются в верхние электронные слои.
400. Периодическая система элементов Д.И. Менделеева складывается из периодов и групп. Периодов в системе семь, из них три малых и четыре больших. Каждый период (кроме первого и последнего) включает в себя элементы, электронные структуры которых являются промежуточными между структурами двух последовательных инертных газов. Из малых периодов первый содержит только водород и гелий, остальные два - по 8 элементов. Из больших периодов четвертый и пятый содержат по 18 элементов, шестой - 32 элемента и седьмой остается незаконченным. Число электронов в электронном слое определяется принципом Паули (в одном атоме не может быть двух электронов с одинаковым набором четырех квантовых чисел).
Емкость уровня совпадает с его заполненостью только для первого и второго периодов. В случае третьего и последующих периодов емкость больше количества элементов. Это связано со следующим явлением: из-за разницы в энергии d- и f-орбитали выталкиваются в верхние электронные слои.
401. Число элементов в периоде определяется значением главного квантового числа: 2n2. Т.е. в седьмом периоде должно содержаться 98 элементов. Последний элемент должен иметь порядковый номер 86+14+10+6 = 116. Он будет являться аналогом радона.
402. Водород и гелий помещают соответственно в первую и вторую группы, т.к. они являются электронными аналогами соответствующих элементов. Однако, физико-химические свойства водорода и гелия более сходны с элементами, соответственно, седьмой и восьмой групп. Водород схож с галогенами по следующим признакам: газообразный, в свободном состоянии - димер. Гелий, как и благородные газы, чрезвычайно инертен.
403. До 1963г. благородные газы помещали в т.н. «нулевую группу», которая располагалась перед группой щелочных металлов. после определения точного строения электронной оболочки благородных газов, было выяснено, что она является не началом электронного слоя, а его завершением. Поэтому сейчас группу благородных газов помещают в последнюю восьмую группу.
404. Атомный номер элемента совпадает как с количеством протонов в ядре его атома, так и с числом электронов. Поскольку последовательность заполнения электронами электронных слоев известна, то, зная количество электронов, можно легко определить положение элемента в ПС.
Элемент №20: электронная формула - 1s22s22p63s23p64s2. Это s-элемент, активный металл. В соединениях имеет положительную степень окисления +2. Формула оксида МеО, гидроксида Ме(ОН)2. Оксид и гидроксид имеют основные свойства и т.д.
Элемент №34: электронная формула - 1s22s22p63s23p64s23d104p4. Это p-элемент, неметалл. В соединениях может иметь степени окисления -2, +2, +4, +6. Наиболее устойчивой является СО = +4. Формула оксида ЭО2, гидроксида Э(ОН)4. Оксид и гидроксид имеют амфотерные свойства и т.д.
405. Элемент №19: электронная формула 1s22s22p63s23p64s1. Четвертый период, первая группа, главная подгруппа. Это s-элемент, активный металл. В соединениях имеет положительную степень окисления +1. Формула оксида Ме2О, гидроксида МеОН. Оксид и гидроксид имеют основные свойства и т.д. Элемент №35: электронная формула 1s22s22p63s23p64s23d104p5. Четвертый период, 7 группа, главная подгруппа. Это p-элемент, неметалл. В соединениях может иметь степени окисления -1, +1, +3, +5, +7. Наиболее устойчивой является СО = -1. Формула гидрида НЭ, гидроксида НЭО1,3,5,7. Оксиды и гидроксиды имеют кислотные свойства и т.д.