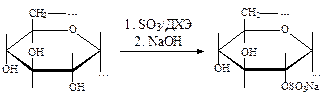Сульфирование растворами триоксида серы в инертных растворителях
Сульфирование концентрированной серной кислотой, олеумом и чистым серным ангидридом имеет ряд существенных недостатков:
1) дезактивация некоторых субстратов (аминов, азолов, пиридина и т. п.);
2) окисление и разрушение лабильных и ацидофобных соединений (углеводов, стероидов, фурана, пиррола, индола и т.д.);
3) необходимость утилизации большого количества серной кислоты. Особенно часто эти методы оказываются непригодными для введения сульфогруппы в молекулу лекарственного вещества.
Сульфирование неводными растворами и комплексами серного ангидрида позволяет решить большинство этих проблем.
Сульфирование растворами триоксида серы в инертных растворителях наиболее универсальный и перспективный метод, который позволяет сульфировать самые различные субстраты — от очень активных (например, фурана, тиофена и пиррола) до инертных (например, азолов) и создавать практически безотходную технологию.
В качестве растворителяиспользуют жидкий сернистый ангидрид, полигалогеналканы (дихлор-, тетрахлорэтан, метиленхлорид) и некоторые другие соединения.
Активностьсерного ангидрида зависит от полярности среды, которая влияет на поляризацию молекулы триоксида серы и величину +d заряда на атоме серы:
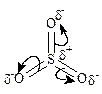
Варьируя растворитель или состав смеси растворителей можно менять сульфирующую активность SO3.
Сульфирование аренов растворами сульфотриоксида в инертных растворителях идет по механизму электрофильного замещения (SE), при этом:
· в полярных средах (например, жидком SO2, 1-фтор-2-хлорэтане), а также в неполярных средах при большом избытке SO3, механизм принципиально не отличается от рассмотренного в разделе 2;
· в неполярных средах (1,2-дихлорэтан, 1,1,2,2-тетрахлорэтан) и мольном соотношении реагентов реакция идет по пиросульфатной схеме. В качестве электрофила помимо SO3 выступает продукт его взаимодействия с образовавшейся сульфокислотой ArSO3SO3H — пиросульфат.
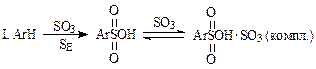
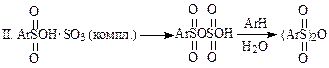
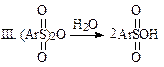
В этом случае кроме первой быстрой стадии наблюдаются еще две медленные. Причем вторая, где сульфирующим агентом является арилпиросульфат, характеризуется некоторым уменьшением концентраций сульфокислот, а третья — медленным достижением 80—95 % превращения субстрата в целевой продукт.
Сульфирование аренов растворами триоксида серы в сернистом ангидриде (полярном растворителе) применяется в синтезе поверхностно-активных веществ (алкиларенсульфонатов). Чаще всего сульфируют алкилбензолы с минимально разветвленной алкильной группой С10—С16. В этом случае продукты сульфирования имеют хорошую биологическую разлагаемость:
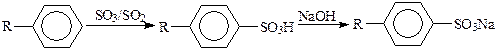
Ароматические соединения, как правило, хорошо растворяются в диоксиде серы, поэтому реакция протекает в гомогенной среде. Процесс ведут при температуре кипения сернистого ангидрида (при –10 °С). Реакция сильно экзотермическая (217 кДж/моль), отвод тепла осуществляется за счет испарения растворителя. Избыток серного ангидрида составляет обычно не более 5 %.
Частичное окисление SO2 в SO3 осуществляется техническим кислородом в блоке 1. Продукты окисления после охлаждения и конденсации в холодильнике 2 собирают в сборнике 3 в виде 10—15 %-ного раствора SO3 в жидком SO2. Этот раствор и раствор алкилбензола в жидком SO2 подают на мешалку в центр тарелки реактора 4. Реактор представляет собой охлаждаемый через рубашку сосуд, внутри которого расположена тарелка с бортиком (стакан), охлаждающими змеевиками и мешалкой. Частично прореагировавшая смесь стекает через бортик тарелки на охлаждаемую стенку корпуса аппарата. Здесь в падающей тонкой пленке жидкости реакция завершается, и большая часть SO2 удаляется через верх реактора. Жидкость, выходящая из нижней части реактора, еще содержит 5—7 % SO2, и для удаления последнего ее подогревают и направляют в вакуумный испаритель 6, после чего она стекает в сборник и поступает на дальнейшую переработку. Газообразный SO2 возвращается в блок 1.
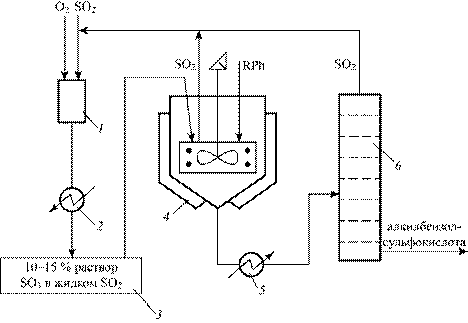
Рис. 2. Схема сульфирования аренов серным ангидридом в жидком SO2
1 — блок окисления SO2 в SO3; 2 — холодильник; 3 — сборник; 4 — реактор; 5 — подогреватель; 6 — испаритель
Сульфирование растворами SO3 в неполярных растворителях (дихлорэтане, метиленхлориде и других) широко используют в синтезе лекарственных веществ. В разработке этого метода активное участие приняли профессор Б.В. Пассет с сотрудниками. С помощью растворов SO3 в неполярных растворителях сульфируют как ароматические субстраты, так и полисахариды:
1. Сульфирование карбоциклических аренов (бензола, нафталина и др.). В синтезе диазолина замена H2SO4 раствором серного ангидрида в дихлорэтане позволила увеличить выход 1,5-нафталин-дисульфокислоты почти вдвое:
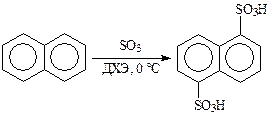
2. Сульфирование ароматических аминов (Б.В. Пассет с сотр.). В отличие от «метода запекания», сульфирование растворами SO3 — процесс одностадийный, идет при 20—30 °С (против 180 °С) без деструкции субстрата вследствие отсутствия высокой температуры и кислотности среды, позволяет сократить время реакции до 1 часа и создавать практически безотходное производство, так как дихлорэтановый фильтрат, содержащий непрореагировавший серный ангидрид, и исходный амин возвращаются в цикл.
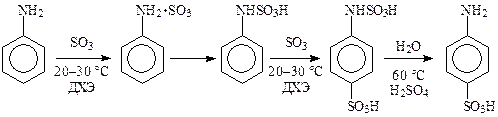
Например, при синтезе сульфаниловой кислоты к раствору анилина в дихлорэтане постепенно, при хорошем перемешивании и температуре не выше 30 °С, прибавляют раствор SO3 в ДХЭ (3 моль на 1 моль анилина), после чего выдерживают 0,5—1 ч. Выпавший осадок отфильтровывают. Дихлорэтановый фильтрат, который не содержит исходного амина, после увеличения концентрации серного ангидрида вновь используют для сульфирования. Бесцветный твердый продукт сульфирования растворяют в воде и нейтрализуют раствором аммиака. Высвободившийся анилин отгоняют с водяным паром, а раствор аммониевой соли упаривают до получения концентрированного раствора и выделяют сульфаниловую кислоту при подкислении серной кислотой и охлаждении. Выход сульфаниловой кислоты составляет 48—49 % на загруженный анилин и 96—98 % на вступивший в реакцию (с учетом возврата).
Метод применим и к замещенным аминам.
3. Сульфатирование полисахаридов (Б.В. Пассет с сотр.). В полигалогенидах (ДХЭ и метиленхлориде) при температуре 0—5 °С реакция идет практически без деструкции полисахарида с образованием ценных биологически активных продуктов (декстрансульфата, ронасана, сульфата альгиновой кислоты и др.) с выходом до 80 %. Механизм реакции SN2, нуклеофилом является кислород спиртового гидроксила, поэтому большое значение имеют строение и надмолекулярная структура молекулы полисахарида (пространственные факторы).