Атериальный баланс диафрагменного электролизера
До сих пор мы рассматривали электролизеры, работающие без разделения электродных пространств. Тем не менее, многие электрохимические аппараты работают с разделением анодных и катодных пространств проточными (получение хлора и щелочей диафрагменным методом, рафинирование никеля) или непроточными (электролиз воды) диафрагмами. Схема аппарата с проточной диафрагмой и потоков в нем показана на рис. 2.19.
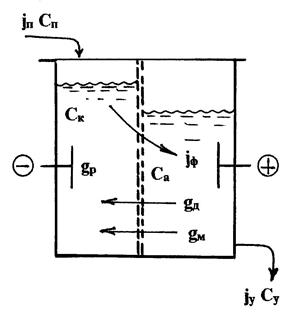 |
Рис.2.19. Схема ЭХА с проточной диафрагмой.
При составлении материальных балансов таких электролизеров электродные пространства можно рассматривать, как отдельные аппараты идеального смешения, проточные и непроточные. В проточных аппаратах перенос вещества через диафрагму осуществляется фильтрацией, диффузионными и миграционными потоками, в непроточных - только диффузией и миграцией.
Составим материальный баланс электролизера для рафинирования никеля, работающего в стационарных условиях. Баланс электролизера будет слагаться из отдельных балансов катодного и анодного пространств. В качестве балансируемого вещества выбираем ионы никеля, принимающие участие и в анодном, и в катодном процессах.
Питающий раствор подается в катодное пространство, где ионы никеля осаждаются на катоде. Из катодного пространства обедненный раствор через диафрагму фильтруется в анодное пространство. На аноде происходит растворение чернового никеля и раствор обогащается ионами Ni2+. Из анодного пространства ионы никеля уносятся уходящим раствором, а также возвращаются в катодное пространство за счет диффузионного переноса (концентрация ионов никеля в катодном пространстве меньше, чем в анодном из-за электрохимической реакции) и миграционного потока.
Для условия сохранения количества вещества мы можем записать
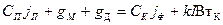 (2.41)
(2.41)
где Сп , jп - концентрация и объемный поток поступающего вещества, gм - миграционный поток, gд - диффузионный поток, Cк, - концентрация вещества в катодном пространстве, jф - поток фильтрации; jп=jф=jу=j, Са=Су.
Миграционный поток равен:
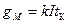
где tк - число переноса катионов
Диффузионный поток определяется из закона Фика:
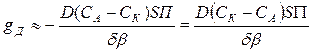
где D - коэффициент диффузии , S - площадь диафрагмы, П -пористость диафрагмы, b- коэффициент извилистости пор, d - толщина диафрагмы.
Примечание. Знак минус в диффузионном потоке означает, что перенос вещества осуществляется против градиента концентрации. При составлении баланса катодного пространства диффузионный перенос увеличивает концентрацию вещества, поэтому в формуле (2.41) стоит знак «плюс».
Подставим формулы потоков в (2.41). Это дает возможность установить необходимую концентрацию и расход питающего раствора:
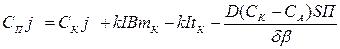 (2.42)
(2.42)
Аналогично составим баланс для анодного пространства
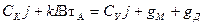
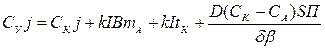 (2.43)
(2.43)
Если просуммировать приходные и расходные статьи балансов по формулам (2.42) и (2.43), то получим уравнение материального баланса ЭХА ИС НД, работающего в стационарном режиме :
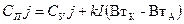
2.7.6. Материальный баланс гальванической ванны
Дано: ванна с начальным объемом раствора V и концентрацией Со, jбр - унос электролита с брызгами, jисп - поток испарения, jдв=jдр=jд - потоки воды и раствора, приносимые в ванну и уносимые из нее на поверхности деталей (рис.2.20).
Определить: изменение концентрации раствора в ванне во время ее работы.
При работе гальванической ванны происходит изменение количества растворенного вещества и объема электролита.
1. Изменение количества растворенного вещества происходит за счет уноса электролита с брызгами, на поверхности деталей и протекания электрохимической реакции:
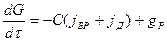 (2.44)
(2.44)
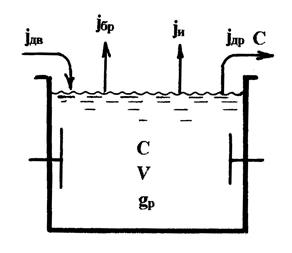 |
Рис.2.20. К материальному расчету гальванической ванны.
Изменение количества вещества за счет электрохимической реакции определяется законом Фарадея (2.45)
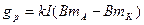 (2.45)
(2.45)
2. Изменение объема раствора во времени обусловлено переносом воды и раствора на поверхности деталей, уносом с брызгами и испарением:
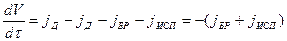 (2.46)
(2.46)
В свою очередь
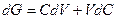 (2.47)
(2.47)
Подставив выражение (2.47) в уравнение (2.44), получаем:
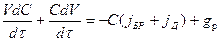
Разделим обе части на V, вынесем С/V
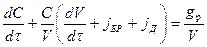 (2.48)
(2.48)
Подставим в формулу (2.44) величину изменения объема (2.46).
Получаем:
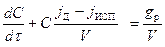
Мы пришли к уже известному дифференциальному уравнению первого порядка. Решение этого уравнения дает
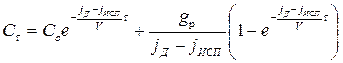 (2.49)
(2.49)
Следствия из уравнения (2.49):
1. Объем электролита в ванне составляет около 1000 л и больше. Величина уноса и испарения редко превышает нескольких литров в час. То есть, 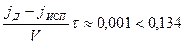 Как известно, если х<0,134, то е-х=1-х и формула (2.48) упрощается. С точностью до одного процента
Как известно, если х<0,134, то е-х=1-х и формула (2.48) упрощается. С точностью до одного процента
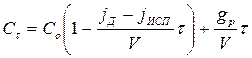
2. Если jд = jисп, то количество принесенной на поверхности деталей воды равно количеству испарившейся воды и концентрация меняется только за счет электрохимической реакции. В этом случае приходим к уравнению материального баланса аппарата идеального смешения периодического действия
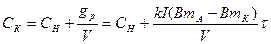 .
.
