Определение общей жесткости
Рабочим раствором метода является 0,05Н раствор комплексона III,известного под названием «трилон Б». Индикатором метода служит хромоген синий (могут использоваться и другие индикаторы, например, эрио-хром черный Т).
Трилон Б представляет собой двунатриевую соль этилендиаминтетрауксусной кислоты:
NaOOCH2C \ /CH2COONa
N-CH2-CH2-N
HOOCH2C / \ CH2COOH
Поскольку в молекуле трилона есть
O
карбоксильные группы —С\//
OH
и аминный азот — N — ,
|
он способен к солеобразованию и к комплексообразованию, т.е. к образованию внутрикомплексных солей.
С ионами кальция и магния трилон Б в щелочной среде дает прочные, растворимые в воде бесцветные внутрикомплексные соли :
NaOOCH2C\

 N -CH2 - CH2 - N
N -CH2 - CH2 - N
OOCH2C/ \CH2COO
|______________Ca_______________|
Стрелками обозначены донорно-акцепторные связи между атомами азота, имеющими свободные электронные пары (донор) и ионами Са2+, имеющими свободные атомные орбитами (акцептор). Реакция образования этого соединения необратима при рН~10. Так как при взаимодействии ионов Ca 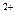 с трилоном выделяются ионы H
с трилоном выделяются ионы H 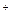 из карбоксильных групп, их необходимо связывать для поддержания постоянного значения рН~10. Для этого к исследуемой воде добавляют аммиачный буферный раствор (смесь NH4OH + NH4C1).
из карбоксильных групп, их необходимо связывать для поддержания постоянного значения рН~10. Для этого к исследуемой воде добавляют аммиачный буферный раствор (смесь NH4OH + NH4C1).
Индикатор метода хромоген синий тоже образует комплексные соли с ионами кальция и магния,растворимые в воде, окрашенные в красный цвет и менее прочные, чем комплексы с трилоном . Наэтом и основаноопределение. При титровании воды трилоном менее прочные окрашенные комплексы ионов Са2+ и Mg2+ с индикатором разрушаются, и ионы образуют прочный бесцветный комплекс с трилоном. В точке эквивалентности индикатор полностью выделяется в свободном состоянии, и красная окраска переходит в синюю. Сложность определения заключается в том, чтоиндикатор не реагирует на избыток трилона, окраска остается синей, поэтому титровать нужно очень осторожно. Кроме того, реакция солей с трилоном идет значительно медленнее, чем с соляной кислотой, поэтому добавление каждой новой порции трилоиа должно сопровождаться хорошим перемешиванием и большей выдержкой.
Если изобразить трилон как двухосновную кислоту в виде Н2-Тр, то все определение, описанное выше, можно представить в виде следующих уравнений:
Ind +Ca2+—> Ca...Ind
синий непрочный комплекс
красного цвета
Ca...Ind + H2-Tp —>Ca...Tp + 2Н+ + Ind
красный бесцветный синий
комплекс
Н+ + NH4OH —>NH4+ + Н2О
Н2-Тр + Ind ≠
