Получение оксидов неметаллов
а) Из простого вещества - взаимодействием простых веществ: S+O2 = SO2, C+O2 = CO2
б) Из кислоты - дегидратацией - разложением на воду и оксид: H2SO3 = SO2 + H2O, H2CO3 = CO2 + H2O
в) Из соли - термическим разложением - разложением на оксид металла и оксид неметалла: MgSO3 = MgO + SO2, ZnCO3 = ZnO + CO2
153. a) BaO - основной оксид, т.к. взаимодействует только с кислотами: BaO + 2HCl = BaCl2 + H2O
б) Al2O3, - амфотерный оксид, т.к. взаимодействует и с кислотами и со щелочами: Al2O3 + 6HCl = 2AlCl3 + 3H2O; Al2O3 + 2NaOH = 2NaAlO2 + H2O
в) Cl2O7 - кислотный оксид, т.к. взаимодействует только со щелочами: Cl2O7 + 2NaOH = 2NaClO4 + H2O
154. Sn(OH)2 - амфотерный гидроксид, т.к. взаимодействует и со щелочами и с кислотами: Sn(OH)2 + 2NaOH = Na2[Sn(OH)4], Sn(OH)2 + 2HCl = SnCl2 + 2H2O.
155. Доказательством амфотерности указанных соединений служит тот факт, что оксид и гидроксид хрома (III) растворяются как в щелочах, так и в кислотах:
Cr2O3 + 2NaOH = 2NaCrO2 + H2O, Cr2O3 + 6HCl = 2CrCl3 + 3H2O
б) Cr(OH)3 + 3NaOH = Na3[Cr(OH)6], Cr(OH)3 + 3HCl = CrCl3 + 3H2O.
156. Для получения формулы кислоты необходимо прибавить математически к формуле ангидрида формулу воды и, если это необходимо, сократить коэффициенты:
SO3 + H2O = H2SO4, SO2 + H2O = H2SO3, N2O5 + H2O = H2N2O6 = 2HNO3, N2O3 + H2O = H2N2O4 = 2HNO2
157. Для получения формулы ангидрида необходимо вычесть математически из формулы кислоты формулу воды, предварительно, если количество протонов нечетное, умножив формулу кислоты на 2:
H2SiO3 - H2O = SiO2, 2H3PO4 - 3H2O = P2O5, 2HClO - H2O = Cl2O, H2CrO4 - H2O = CrO3
158. a) CaO - основной оксид, взаимодействует только с кислотами: CaO+2HCl = CaCl2 + H2O
б) Al2O3, - амфотерный оксид, взаимодействует и с кислотами и со щелочами: Al2O3 + 6HCl = 2AlCl3 + 3H2O; Al2O3 + 2NaOH = 2NaAlO2 + H2O
в) P2O5 - кислотный оксид, взаимодействует только со щелочами: P2O5 + 6NaOH = 2Na3PO4 + 3H2O
159. а) Разделить BaO и MgO можно, обработав их водой: гидроксид магния выпадет в осадок, а гидроксид бария останется в растворе.
б) Разделить CdO и ZnO можно, обработав их NaOH: гидроксид цинка растворится, т.к. он амфотерен, а гидроксид кадмия останется в осадке, т.к. он имеет основные свойства: ZnO + 2NaOH = Na2ZnO2 + H2O
в) Разделить СО и СО2 можно при помощи сорбентов: силикагель поглощает СО2, но не абсорбирует СО.
г) Разделить Al(OH)3 и La(OH)3 можно, обработав их щелочью: амфотерный гидроксид алюминия растворяется в щелочах, а основный гидроксид лантана нет: Al(OH)3 + 3NaOH = Na3[Al(OH)6].
160. С повышением степени окисления металла в гидроксиде (оксиде), свойства гидроксида (оксида) становятся более кислотными и менее основными: CrO - основный, Cr2O3 - амфотерный, CrO3 - кислотный.
CrO + 2HCl = CrCl2 + H2O
Cr2O3 + 2NaOH = 2NaCrO2 + H2O, Cr2O3 + 6HCl = 2CrCl3 + 3H2O
CrO3 + 2NaOH = Na2CrO4 + H2O
161. Получение нитрата калия:
а) Основание с кислотой: KOH + HNO3 = KNO3 + H2O
б) Основной оксид с кислотным: K2O + N2O5 = 2KNO3
в) Основание с кислотным оксидом: 2KOH + N2O5 = 2KNO3 + H2O
г) Основной оксид с кислотой: K2O + 2HNO3 = 2KNO3 + H2O
162. Получение хлорида магния:
а) Металл с кислотой: Mg + 2HCl = MgCl2 + H2
б) Оксид с кислотой: MgO + 2HCl = MgCl2 + H2O
в) Основание с кислотой: Mg(OH)2 + 2HCl = MgCl2 + 2H2O
г) Соль + соль: MgSO4 + PbCl2 = MgCl2 + PbSO4
163. 2Fe + O2 = 2FeO, FeO + SO3 = FeSO4, FeSO4 + 2KOH = Fe(OH)2 + K2SO4, 4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3, Fe(OH)3 + 3HNO3 = Fe(NO3)3 + 3H2O, 2Fe(NO3)3 =нагрев= Fe2O3+ 3N2O5, Fe2O3 + H2 = 2FeO + H2O, FeO + H2 = Fe + H2O
164. 2Zn + O2 = 2ZnO, ZnO + HNO3 = Zn(NO3)2 + H2O, Zn(NO3)2 +2KOH = Zn(OH)2 + 2KNO3, Zn(OH)2 = ZnO + H2O, ZnO + H2 = Zn + H2O
165. S + O2 = SO2, 2SO2 + O2 = 2SO3, SO3 + H2O= H2SO4, H2SO4 + 2KOH = K2SO4 + 2H2O, K2SO4 + Ba(NO3)2 = BaSO4 + 2KNO3
166. 4P + 5O2 = 2P2O5, P2O5 + H2O = 2HPO3, 2HPO3 + H2O= H4P2O7, H4P2O7 + H2O = 2H3PO4, H3PO4 + KOH = KH2PO4 + H2O, KH2PO4 + KOH = K2HPO4 + H2O, K2HPO4 + KOH = K3PO4 + H2O.
167. a) FeCl3+ 3KOH = Fe(OH)3 + 3KCl, 2Fe(OH)3 = Fe2O3+ 3H2O
б) Fe2O3 + 3HNO3 = 2Fe(NO3)3 + 3H2O, Fe(NO3)3 + 3KOH = Fe(OH)3 + 3KNO3
в) FeS + 2KOH = Fe(OH)2 + K2S, 4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3
168. Поскольку оксид кальция - основное соединение, то СаО взаимодействует с веществами кислотной природы: CaO + 2HNO3 = Ca(NO3)2 + H2O, CaO + 2HNO2= Ca(NO2)2 + H2O, CaO + SO3 = CaSO4, CaO + Al2O3 = Ca(AlO2)2, CaO + Zn(OH)2 = CaZnO2 + H2O.
169. Поскольку соляная кислота - кислотное соединение, то она взаимодействует с веществами основной природы: 2HCl + Zn(OH)2 = ZnCl2 + 2H2O, 2HCl + CaO = CaCl2 + H2O, HCl + AgNO3= AgCl + HNO3.
170. Поскольку щелочи - основные соединения, то они взаимодействует с веществами кислотной природы: KOH + HCl= KCl + H2O, 2NaOH + H2S= Na2S + 2H2O, NaOH + SO2 = NaHSO3, NaOH + SO3 = NaHSO4.
171. NO2 - диоксид азота, HF - фтористый водород, H2SiO3 - метакремниевая кислота, H4SiO4 - ортокремниевая кислота; а) сульфат лития - Li2SO4, б) сульфит магния - MgSO3, в) дигидрофосфат калия -KH2PO4, г) сульфат гидроксомеди(II) - (CuOH)2SO4.
172. SnO - оксид олова(II), SnO2 - оксид олова(IV), HMnO4 - марганцевая кислота, SiH4 - гидрид кремния (силан), а) нитрат бария - Ba(NO2)2, б) нитрит аммония - NH4NO2, в) нитрат гидроксожелеза(III) - FeOH(NO3)2.
173. CaCl2 - хлорид кальция, CaOHCl -гидроксохлорид кальция, Ca(NO3)2 - нитрат кальция, CaOH(NO3) - гидроксонитрат кальция, CaSO4 - сульфат кальция, (CaOH)2SO4 - гидроксосульфат кальция, Ca(HSO4)2 - гидросульфат кальция.
174. Na2SO4 - сульфат натрия, NaHSO4 - гидросульфат натрия, Na2SO3 - сульфит натрия, NaHSO3 - гидросульфит натрия, Na2S - сульфид натрия, NaHS - гидросульфид натрия.
175. HNO2 - азотистая кислота, NH3 - нитрид водорода, P2O3 - оксид фосфора (III), Zn(OH)Cl - гидроксохлорид цинка, BiONO3 - оксонитрат висмута (III); оксид хрома (VI) - CrO3, нитрид кальция - Ca3N2, сульфид аммония - (NH4)2S, гидрокарбонат натрия - NaHCO3.
176.
| Вещество | Название | Структура |
| Na2S | Сульфид натрия | Na-S-Na |
| KClO3 | Хлорат калия | 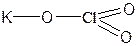 |
| FePO4 | Фосфат железа | 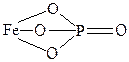 |
| MgOHCl | Гидроксохлорид магния | H-O-Mg-Cl |
| KH2PO4 | Дигидрофосфат калия | 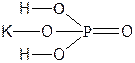 |
| K2HPO4 | Гидрофосфат калия | 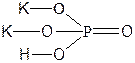 |
| K3PO4 | Фосфат калия | 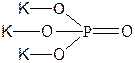 |
177.
| Вещество | Название | Структура |
| N2O5 | Азотный ангидрид | 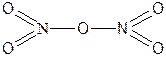 |
| Pb(HSO4)2 | Гидросульфат свинца(II) | 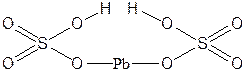 |
| (FeOH)2SO4 | Сульфат гидроксожелеза (II) | 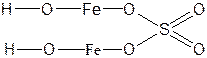 |
| NaNO3 | Натриевая селитра | 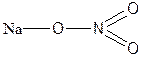 |
| SbOCl2 | Хлорид оксосурьмы(III) | 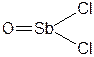 |
178.
| Вещество | Название | Структура |
| Cr2O3 | Оксид хрома(III) | 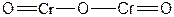 |
| CrO3 | Оксид хрома(VI) | 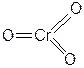 |
| (BeOH)2 | Гидроксид бериллия | H-O-Be-O-H |
| HMnO4 | Марганцевая кислота | 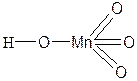 |
| MgSO4 | Сульфат магния | 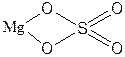 |
| CuCl2 | Хлорид меди (II) | Cl-Cu-Cl |
| Ca(HCO3)2 | Гидрокарбонат кальция | 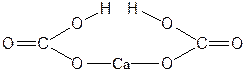 |
179. а) Оксид железа (III), б) Сульфит кальция, в) Гидрофосфат натрия.
180.KAl(SO4)2 - калия алюминия сульфат (двойная соль), FeSO4*7H2O - гептаакважелеза (II) сульфат (кристаллогидрат). А) Сульфит стронция - SrSO3, б) сульфат дигидроксоалюминия (Al(OH)2)2SO4, в) гидрокарбонат магния -Mg(HCO3)2, г) ортомышьяковая кислота - H3AsO3.
