Менделеев Дмитрий Иванович 1834 – 1907
 Орыс ғалымы, Петербург ҒА-ның мүше-корреспондентi (1876 жылдан) Менделеев Д.И. Тобольскiде туылып (1834ж.), Петербургтегi Бас педагогикалық институтты (1855ж.) тәмамдады.
Орыс ғалымы, Петербург ҒА-ның мүше-корреспондентi (1876 жылдан) Менделеев Д.И. Тобольскiде туылып (1834ж.), Петербургтегi Бас педагогикалық институтты (1855ж.) тәмамдады.
1855 – 1856 жылдары Одессадағы Ришельевский лицейi жанындағы гимназия мұғалiмi. 1857 – 1890 жылдары Петербург университетiнде (1865 жылдан профессор) дәрiс оқыды, сонымен бiр мезгiлде 1863 – 1872 жылдары Петербург технология институтының проессоры. 1859 – 1861 жылдары Гейдельбергте ғылыми iс-сапарда болды. 1890 жылы оқу-ағарту министрiмен келiспеушiлiктен кейiн университеттен шығып кеттi.
Ғылыми жұмыстары негiзнен химия саласына және одан басқа физика, химиялық технология, экономика, ауылшаруашылығы, метрология, география, метеорология салаларына қатысты.
Изоморфизм құбылысын (1854-1856 жылдары) және элементтер қасиетiнiң олардың атомдық көлемiнен тәуелдiлiгiн зерттедi.
1860 жылы “сұйықтың абсолюттiк қайнау температурасын” (немесе дағдарыстық) ашты.
“Органикалық химия” – атты бiрiншi орыс оқулығының авторы (1861ж.). “Химия негiздерi” еңбегiмен жұмыс кезiнде (1869ж. февраль) химиялық элементтердiң периодтық заңын ашты. Ол ашқан периодтық заңы кейiнгi химиктер мен физиктерге атом құрылысын зерттеуге, периодтық себептерiн талқылауға және заңның физикалық мағынасын зерттеуге жол ашты.
1859 ж. сұйық тығыздығын анықтайтын құралды – пикнометрдi құрастырды. 1865 – 1887 жылдары қопалардың гидраттық теориясын жасады.
Газдарды зерттей келе (1874ж.) 1834ж. физик Клапейронның алған (Клапейрон-Менделеев теңдеуi), газ күйiнiң температурадан тәуелдiлiгiнiң жеке жағдайы болатын, идеал газ күйiнiң жалпы теңдеуiн тапты.
Ол көптеген ғылым академиялары мен ғылыми қоғамдардың мүшесi. Орыс физика-химия қоғамын (1868ж.) құрушылардың бiрi.
Оның құрметiне N101 – менделевий элементi аталған.
Химия және химиялық технология саласы бойынша үздiк еңбектер үшiн КСРО ҒА-сы (1962ж.) Д.И.Менделеев атындағы премия және алтын медаль тағайындады.
Реферат
Тақырыбы:Химиялық реакциялырдың жылдамдықтары
Тексерген:Жапанова Альфия Бекжановна
МДТ 1(9) жб
Орындаған:Советова Эльмира
Жоспары:
1.Химиялық реакцияның жылдамдығы.
2. Химиялық реакциялардың жылдамдығына әсер ететін негізгі фактор.
3. Химиялық реакциялардың жүру заңдылықтары.
Химиялық реакциялардың жылдамдығы. Химиялық реакциялардың жүру заңдылықтарын зерттеу химияның негізгі мәселесі. Химиялық заттар алу үшін реакцияның жүру механизмі мен жылдамдығын білу керек. Реакцияның жүру механизмін, жылдамдығын және сол жылдамдыққа әрекеттесетін заттардың концентрацияларының, температураның, қысымның, катализатордың әсерін зерттейтін ғылым химиялық кинетика деп аталады.
· Әр түрлі реакциялар әр түрлі жылдамдықпен жүреді. Кейбір реакциялар өте жай жүреді, ал басқа біреулері өте тез қопарылыс беріп жүреді. Бір реакцияның өзі жағдайларға байланысты әр түрлі жылдамдықпен жүреді. Мысалы, сутегі мен оттегінің қоспасы қалыпты температурада әрекеттеспей көп уақыт өзгеріссіз қала береді, ал енді осы қоспаны 6300С – ға дейін қыздырса немесе қыздырмай – ақ тиісті катализатор қолданса, реакция қопарылыс беріп,су түзіледі.
· Химиялық реакция кезінде реакцияласушы заттардың мөлшері, демек, концентрациясы өзгереді. Сондықтан химиялық реакцияның жылдамдығын кесімді уақыт ішінде (секунд, сағат, жыл) реакцияласушы заттардың концентрациясының өзгеруімен өлшейді. Концентрация дегніміз- көлем бірлігіндегі заттың мөлшері, көбнесе 1 л/моль саны алынады.
Химиялық реакциялардың жылдамдығына әсер ететін негізгі факторларға әсер етуші заттардың концентрациясы, температура, катализатордың болуы жатады.
Реакцияның жылдамдығына температураның әсері. Заттардың әрекеттесуі үшін олардың бөлшектері өзара кездесіп соқтығысуы қажет. Соқтығысу нәтижесінде бөлшектердің электрон бұлттарының тығыздықтары өзгеріп, жаңа химиялық байланыс түзіледі.
- Тәжірибе жүзінде температура әрбір 100С – қа артқанда реакция жылдамдығы 2-4 есе өсетіндігі анықталған. Бұл ереже оны ашқан ғалымның атымен Вант – Гоффережесі деп аталады. {\displaystyle ~V_{2}=V_{1}\cdot \gamma ^{\frac {T_{2}-T_{1}}{10}}}
Концентрацияның әсері. Химиялық реакция тездеу үшін, реакцияласушы заттардың молекулалары жиі түйісуі қажет екендігі анықталды. Түйісуді жиілендіру үшін алдымен реакцияласушы молекулалардың санын, демек, концентрациясын өсіру керек.
· Мысалы: Н2 + І2 = 2HI реакциясын алсақ, реакцияның жылдамдығы минутына 0,001 моль болсын. Енді, реакцияласушы заттың бірінің айталық, иодтың концентрациясын 3 есе өсірдік; онда иод пен сутектің молекулаларының белгілі уақыт ішінде түйісу саны үш есе артады, демек, олардың арасындағы реакцияның жылдамдығы да үш есе артады; 2 есе өсірсек, онда реакцияның жылдамдығы алты есе артып, минутына 0,001 ∙ 3 ∙ 2 = 0,006 моль болады.
Химиялық реакцияның жылдамдығына әрекеттесуші заттардың концентрациясының әсерін зерттеген, Норвегияның екі ғалымы Гульдберг пен Вооге 1867 жылы мынандай қорытындыға келеді:
· Химиялық реакцияның жылдамдығы реакцияласушы заттар концентрацияларының көбейтіндісіне тура пропорционал. Мұны әрекеттесуші массалар заңы деп атайды. Енді сол заңды математика тіліне аударып, реакцияны жалпы теңдігі :А + В = С А және В затының концентрацияларын [A] және [B] деп, реакцияның жылдамдығын υ арқылы белгілесек, онда, υ = k ∙ [A] ∙ [B] болады; бұл арадағы k – пропорционалдық коэфициенті деп аталады. Егер алынған теңдікте [A] = 1 және [B] = 1 болса, онда, υ = k болады, демек, k – реакцияласушы заттардың концентрациялары бірге тең (1 моль/л) болған жағдайдағы реакция жылдамдығы, k - әрбір реакцияның өзіне лайықты тұрақты шама, ол тек қана реакцияласушы заттардың жаратылыстық қасиетіне қарай және температураға тәуелді өзгереді, сондықтан оны реакцияның жылдамдық константасы деп атайды.
Реакцияласу үшін заттың біреуінен теңдік бойынша бір емес бірнеше молекула керек болса, онда, реакция жылдамдығының теңдігі басқа түрде болады, мысалы:
· 2А + В = D не A + A + B = D
Осы реакция жүру үшін А затының екі молекуласы мен В затының бір молекуласы бір мерзім ішінде түйісу керек. Мұндай жағдайда математикалық анализге сәйкес реакция жылдамдығының теңдігінде А заты концентрациясының мәнін екі рет алу қажет: υ = k ∙ [A] ∙ [A] ∙ [B] = k ∙ [A]2 ∙ [B] жалпы алғанда А затының m молекуласымен В затының п молекуласы реакцияласса: тА + пВ = Г реакцияның жылдамдығының теңдігі мынадай түрге ауады:
· υ = k ∙ [A]т ∙ [B]п
Катализатордың әсері. Катализатор дейтініміз – реакцияның жылдамдығын өзгертіп, бірақ реакция нәтижесінде өздері химиялық өзгермей қалатын заттар.
· Әрбір реакцияның өзіне лайықты катализаторлары болады, ол катализатор басқа реакцияларға әсер етпеуі мҥмкін. Кей жағдайда әр түрлі катализаторлар қолданып, бір заттан бірнеше өнімдер алуға болады. Реакцияға катализатор қатысқандықтан ондағы актив молекулалар саны артады, содан барып реакциялар жылдамдығы артады. Катализаторлар қатты, сұйық және газ күйінде де болады. Қатты катализаторлардың катализаторлық активтігінен айырылып қалуы оның улануы, мұндай заттар катализатордың уы деп аталады. Катализатордың уымен қатар активаторлары белгілі, бұл өз бетінше катализаторлық активтілігі жоқ, бірақ аз мөлшерде катализаторға араластырса, оның активтігін көтеретін заттар; мұндай заттарды промотр деп атайды. Реакция жылдамдығын тездететін катализатордан басқа реакцияны баяулататын қасиеттері бар заттар да бар, оларды ингибитор деп атайды.
· Катализатор әсерінен жылдамдығын өзгертетін процестерді каталитикалық процесс немесе катализ деп атайды. Катализде гомогенді және гетерогенді болады. Гомогенді катализде катализатор да, реакцияласушы заттар да бір фазада болады. Гетерогенді катализде катализатор мен рекцияласушы заттар әр түрлі фазаға жатады. Гомогенді катализдегі катализатордың әсері аралық қосылыстардың түзілуі арқылы түсіндіріледі. Айталық А + Б = АБ реакциясы өте баяу жүреді; оған катализатор К қатынастырсақ, реакция тездейді, өйткені ол арада реакцияласқыш аралық қосылыс АК түзіледі:
· А + К = АК
Түзілген аралық қосылыс АК, Б затымен реакцияласып бізге керекті АБ қосылысын түзеді: катализатор К бос таза күйде бөлініп шығады; АК + Б = АБ + К Бұдан катализатор реакцияға қатысқанымен реакция нәтижесінде химиялық өзгермей қалатындығын көреміз.
Химиялық реакциялардың жүру заңдылықтарымен танысу үшін мынадай түсініктерге және заңдарға анықтама берейік:
o фаза
o гомогенді және гетерогенді жүйелер мен реакциялар
o химиялық реакциялардың жылдамдығы
o әрекеттесуші массалар заңы
o Вант-Гофф ережесі
o катализ
o катализатор.
Фаза – гетерогенді (әртүрлі) жүйенің біртекті бөлігі. Мысалы, О˚С су үш агрегаттық күйде болып: мұз, су мен бу – үш фазадан тұратын гетерогенді жүйе түзеді: қатты фаза – мұз, сұйық – су және газтекті фаза – бу.
Гомогенді жүйелерде әрекеттесетін заттардың агрегаттық күйі бірдей немесе бір фазаның көлемінде жүретін реакцияларды гомогенді реакциялар деп атайды.
Гетерогенді жүйелер бірнеше фазадан тұрады; әрекеттесуші заттар әр түрлі агрегаттық күйде болатын реакцияларды гетерогенді реакциялар деп атайды.
Азот N2 мен оттек О2 әрекеттескенде, азот (ІІ) оксидінің түзілу реакциясы гомогендік реакцияға жатады. Себебі бастапқы және түзілген заттар бірдей күйде – газ күйінде болады. Бұл процесті былай өрнектеуге болады:
N2(г) + O2(г) = 2NO(г) – Q, мұнда г – газ, Q – реакцияның жылу эффектісі.
Кальций оксидінің көміртек (ІV) оксидімен әрекеттесу процесі – гетерогендік реакцияға жатады, өйткені CaO және түзілетін CaCO3 – қатты күйде, ал CO2 газ күйінде болады:
CaO(қ) + CO2(г) = CaCO3(қ) , мұнда қ – қатты.
Химиялық реакцияның жылдамдығы уақыт өлшемінде әрекеттесетін заттардың немесе түзілген өнімдерінің біреуінің зат мөлшері жүйенің белгілі бір көлемінде (гомогенді реакция) немесе фаза бетінің аудан бірлігінде (гетерогенді реакция) өзгеруін айтады.
Гомогенді реакция жүйенің бүкіл көлемінде жүреді:
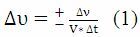
мұнда: ∆υ – реакцияның орташа жылдамдығы, моль/л · с;
∆ν(ню) – зат мөлшерінің өзгеруі, моль;
V – жүйенің көлемі, л;
∆t – уақыт интервалы, с.
Химиялық реакцияның жылу жылдамдығының шамасы оң таңба болу үшін математикалық өрнектеуінің алдында оң және теріс таңбалар қойылды.
Себебі егер химиялық реакцияның жылдамдығын реагенттердің мөлшерінің өзгеруі бойынша есептегенде, реакция кезінде бастапқы заттардың мөлшері азаяды да, реакцияның жылдамдығы теріс шама болмау үшін 1 – теңдеуде (-) таңба қойылған.
теңдеуде 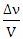 қатынасы заттың молярлық концентрациясын көрсетеді.
қатынасы заттың молярлық концентрациясын көрсетеді.
CМ, онда бұл теңдеуі басқаша өрнектеледі:
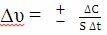
Гетерогенді жүйелерде реакция фазааралық бетте жүреді:
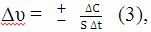 мұнда S – реакция өтетін фаза бетінің ауданы.
мұнда S – реакция өтетін фаза бетінің ауданы.
Гетерогендік реакцияның жылдамдығы жанасу бетінің шамасына және араластыру жылдамдығына тәуелді болады.
Әрекеттесуші массалар заңы: химиялық реакцияның жылдамдығы әрекеттесуші заттардың концентрацияларының көбейтіндісіне тура пропорционал.
Мынадай реакцияны қарастырайық:
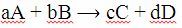
Мұнда А, В, С, D – газ және сұйық күйдегі заттар, ал а, в, с, d – реакция теңдеудегі стехиометриялық коэффициенттер.
Осыдан әрекеттесуші массалар заңы математикалық түрде былай бейнеленеді:
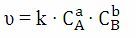
мұнда СА және СВ – А және В заттардың молярлық концентрациялары, k – пропорционалдық коэффициенті немесе берілген реакцияның жылдамдық константасы.
Вант-Гофф ережесі: гомогенді жүйелерде химиялық реакциялардың жылдамдығы әрбір 10 градусқа көтергенде шамамен 2-4 есе артады.
Вант-Гофф ережесін, математикалық теңдеуі жылдамдықтардың қатынасы арқылы өрнектеледі:
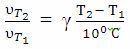
мұнда 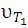 – бастапқы температурадағы реакция жылдамдығы;
– бастапқы температурадағы реакция жылдамдығы;
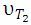 - соңғы температурадағы және соңғы реакция жылдамдығы;
- соңғы температурадағы және соңғы реакция жылдамдығы;
Т1 және Т2 бастапқы және соңғы температуралар;
γ – температуралық коэффициент, ол – температураны 10˚C - ға жоғарылатқанда белгілі реакция жылдамдығының неше есе өсетінін көрсететін сан, 2 ≤ γ ≤ 4
Катализ: катализаторлардың әсерінен химиялық жылдамдықтың өзгеруі.
Катализаторлар, өршіткілер – химиялық реакцияның жылдамдығын өзгерте алатын, бірақ реакция өнімдерінің құрамына кірмейтін заттар.
Пайдалынылған әдебиет:
Ғаламтор желісі.
