Результаты расчета коагулирующей силы испытуемого золя
| Электролиты | Испытуемый золь | |||
| Ионы – коагуляторы | Знак заряда коллоидной частицы | Порог коагуляции | Коагулирующая сила | |
| KCl | ||||
| CaCl2 | ||||
| K2SO4 |
Задание 2. Коагуляция гидрофильных коллоидов действием дегидратирующих веществ и установление их обратимости.
Таблица 22
Результаты коагуляции гидрофильных и гидрофобных золей и определение их обратимости
| Золь | Реактив | Кол-во реактива пошедшее на коагуляцию, мл. | Кол-во воды пошедшее на превращение геля в золь | Вывод об обратимости коллоидов |
| Гидрозоль желатины | Этиловый спирт | |||
| Гидрозоль желатины | Сульфат аммония | |||
| Гидрозоль сернистой сурьмы | Этиловый спирт | |||
| Гидрозоль сернистой сурьмы | Сульфат аммония |
На основании полученных данных определите знак заряда коллоидных частиц исследуемого золя и сделайте письменный вывод.
ВОПРОСЫ ДЛЯ САМОКОНТРОЛЯ:
1. Явление электрофореза и электроосмоса.
2. Что такое коагуляция коллоидных систем.
3. Правило Шульце-Гарди.
4. Чем можно вызвать коагуляцию гидрофобных коллоидов.
5. Механизм коагуляции гидрофобных коллоидов.
ЛАБОРАТОРНАЯ РАБОТА № 10.
ОПРЕДЕЛЕНИЕ ИЭТ ГИДРОФИЛЬНОГО ЗОЛЯ ЖЕЛАТИНЫ ВИЗКОЗИМЕТРИЧЕСКИМ МЕТОДОМ.
КРАТКИЙ КОНСПЕКТ:
ОБЩАЯ ПОСТАНОВКА ЗАДАЧИ:Измерение относительной вязкости на вискозиметре Оствальда в модификации С.Н.Булычёва. Измерение вязкости гидрофильного золя в зависимости от величины рН среды. Нахождение ИЭТ.
ОБОРУДОВАНИЕ И РЕАКТИВЫ:
1. Вязкозиметр Оствальда в модификации С.Н. Булычёва с термостатом.
2. Измерительный стаканчик.
3. 2 % раствор желатины с различными значениями рН.
4. Дистиллированная вода.
Задание 1. Определение постоянной вискозиметра
Поскольку вязкость, плотность, а следовательно, и время истечения являются величинами постоянными при данных условиях, то
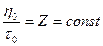
Величина Z называется постоянной вискозиметра. Тогда вязкость исследуемого золя можно рассчитать по формуле
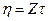
Вязкость воды при 250С – 0,8939 сП, плотность – 0,99707 г/см3.
Задание 2. Измерение вязкости лиофильного золя при различных значениях рН среды. Нахождение изоэлектрической точки
Приступают к измерению времени истечения растворов гидрофильного золя одинаковой концентрации, но с различными значениями рН. Измерения начинают с раствора с минимальным рН. Перед работой с каждым последующим раствором вискозиметр ополаскивают дистиллированной водой.
Точность измерения времени истечения каждого раствора должна быть 0,5 с.
Рассчитывают вязкость золей. Данные записывают в табл. 17. По полученным данным строят график зависимости вязкости h лиофильного золя от рН. Допускаются и графики в координатах:
время истечения t (в cекундах) от рН;
или 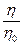 от рН.
от рН.
На графике находят ИЭТ исследуемого лиофильного золя.
Таблица 23
Результаты измерений
| Исследуемый раствор | РН Раствора | Время истечения определённого объёма раствора, t, с | h раствора | |||
| Измерения | ||||||
| Среднее | ||||||
| Вода | 5,70 | |||||
| 1 % желатины | 1,54 | |||||
| 2,80 | ||||||
| 3,46 | ||||||
| 4,70 | ||||||
| 6,70 | ||||||
| 9,00 | ||||||
| 12,0 |
Z = ………
По полученным данным построить график зависимости вязкости η лиофильного золя желатины от величины рН. Допускаются графики в координатах время истечения от рН (t от рН).
График зависимости относительной вязкости от рН и нахождения ИЭТ.
ВОПРОСЫ ДЛЯ САМОКОНТРОЛЯ:
1. Что такое вязкость.
2. Напишите формулу Эйнштейна. Зависимость вязкости от концентрации.
3. В каких системах образуются студни. Чем отличается студень от геля. Обратим ли эластичный студень.
4. Что такое набухание и чем обусловлено это явление.
5. Что такое изоэлектрическое состояние белка. От чего зависит положение ИЭТ на графике зависимости вязкости от рН среды.
