Кривые амперометрического титрования
АМПЕРОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
В процессе амперометрического титрования после прибавления отдельных порций реактива отмечают силу тока при напряжении, соответствующем величине предельного тока. По этим данным строят кривую амперометрического титрования в координатах сила тока – объём титранта и графически находят точку эквивалентности. В качестве индикаторного электрода в амперометрическом титровании обычно применяются вращающиеся платиновые, графитовые и другие твёрдые электроды.
Кривые амперометрического титрования
Вид кривой амперометрического титрования зависит от того, какой компонент реакции титрования вступает в электродную реакцию – определяемое вещество, титрант или продукт реакции. Например, если при титровании серебра иодидом используется процесс восстановления серебра на платиновом вращающемся катоде, кривая титрования имеет вид, представленный на рис. 1а.
 Id Id
Id Id
 | |||
 | |||



Vт.э. V Vт.э. V
а б
Рис. 1. Кривые амперометрического титрования: а - электрохимически активно определяемое вещество; б - электрохимически активен титрант
Если в этом титровании используется процесс анодного окисления иодид - иона (титранта), кривая титрования имеет вид, приведенный на рис. 1 б.
В первом случае в ходе титрования сила тока уменьшается, так как концентрация серебра в растворе падает в результате образования осадка AgI, а после достижения точки эквивалентности остаётся постоянной. Во втором случае, когда используется анодное окисление иодид – иона, концентрация его после точки эквивалентности увеличивается и это отражается в возрастании силы тока. Точка эквивалентности в обоих случаях находится графически как точка пересечения соответствующих прямых (касательных к двум ветвям кривой титрования).
Также различают кривую амперометрического титрования по диффузионному току, обусловленному концентрацией образовавшегося продукта реакции титрования. Этот случай реализуется, например, при титровании мышьяковой кислоты, иодидом калия:
|
По мере титрования концентрация свободного иода, выделяющегося как продукт реакции, будет возрастать до точки эквивалентности, после чего останется постоянной (рис. 2 а)
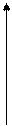

 Id Id
Id Id
 |

 а б
а б
 | |||||
 |  | ||||



Vт.э. V Vт.э. V
Рис. 2. Кривые амперометрического титрования: а - электрохимически активен только продукт реакции; б - электрохимически активны определяемое вещество и титрант.
Если на рабочем электроде при заданном потенциале возможно восстановление (или окисление) определяемого вещества и титранта, то наблюдаются V -образные кривые титрования, например, кривые снятые на ртутном капающем катоде при титровании ионов Zn2+ хромат ионами.