Препараты карбоновых кислот и их солей
RCOOH(Me, R’) – увеличение растворимости, уменьшение токсичности, Н обеспечивает раздражающее действие и антимикробную активность.
Получение: 1. Окислением спиртов 2. Из галогенпроизводных УВ.
Физическиесвойства: от подвижной жидкости через вязкие до твердых веществ
Растворимость: падает с увеличением Mr, в спирте хор. растворимы, для солей – наоборот.
Химическиесвойства:
1. Кислотность: Ка = 10-4-10-5. Способны образовывать соли с Ме, оксидами Ме, растворами едких щелочей, гидроксидами Ме, карбонатами Ме. Соли подвергаются гидролизу – рН>7.
2. Образуют комплексные соединения с солями тяжелых Ме – Fe(III), Cu(II).
3. Вступают в реакции этерификации
Препараты:
Kalii acetas. Калия ацетат. CH3COOK
Описание: Белый, кристаллический порошок со слабым запахом уксусной кислоты, гигроскопичен, на воздухе расплываются.
Растворимость: ОЛР в воде, ЛР в спирте.
Подлинность:
CH3COO- + C2H5OH 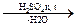 CH3COOC2H5 Запах
CH3COOC2H5 Запах
7CH3COO- + 3FeCl3 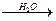 2(CH3COO)3Fe•Fe(OH)2(CH3COO) + 7Cl- + 2HCl красный цвет.
2(CH3COO)3Fe•Fe(OH)2(CH3COO) + 7Cl- + 2HCl красный цвет.
Чистота: допускаются общие примеси, OH-, недопустима примесь восст-щих веществ.
Количественноеопределение:
1. Неводное титрование в ледяной уксусной кислоте. Титрант – раствор HClO4 в ледяной уксусной, индикатор – кристаллический фиолетовый.
HClO4 + CH3COOH « ClO4- + CH3COOH2+
CH3COOK « CH3COO- + K+
CH3COO- + CH3COOH2+ à 2CH3COOH
K+ + ClO4-« KClO4
f=1; 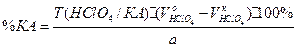
2. Нефармакопейный метод: прямая ацидиметрия с индикатором треополином 00:
CH3COOK + 0,1M HCl à CH3COOH + KCl
До перехода окраски из желтой в красноватую, рТ инд. = 1,3 – 3,2
f=1; 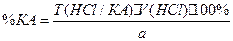
3. Ионообменная хроматография.
Хранение: хорошо укупоренная тара, предохраняет от попадания воды.
Применение: как диуретическое средство; при гипокалемии.
Calcii lactas. Кальция пропионат-2-ол пентагидрат. (CH3-CHOH-COO)2Ca•5H2O
Описание: белый аморфный порошок почти без запаха, на воздухе выветривается
Растворимость: медленно растворим в воде, легко растворим в горячей воде, практически нерастворим в 95% спирте.
Получение: окисление глюкозы в присутствии солей кальция.
Подлинность: ИК-спектроскопия – характерные пики на группы COO- и OH. Реакция А на ион кальция.
На лактат-ион: к раствору препарата прибавляют H2SO4 и KMnO4 до малиново-фиолетовой окраски, окраска исчезает, запах уксусного ангидрида:
(CH3-CHOH-COO)2Ca + 4KMnO4 + 11H2SO4 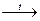 10CH3CHO + 2K2SO4 + 4MnSO4+10CO2+5CaSO4+ 16H2O
10CH3CHO + 2K2SO4 + 4MnSO4+10CO2+5CaSO4+ 16H2O
Нефармакопейные:
Ацетальдегид в прис. нитропруссида Na дает синюю окраску.
С реактивом Несслера – темно-бурый осадок.
Йодоформная проба
Чистота: прозрачность и цветность в сравнении с эталонами, щелочность и кислотность (ФФ + NaOH).
Наличие летучих и жирных кислот (при нагревании с H2SO4 не д. б. запаха жирных кислот).
общие – Cl-, SO42-; частные – Ba, Mg, щелочные Me; микробиологическая чистота; потеря в массе при выслушивании 20-30%
Количественноеопределение: прямая комплексонометрия с аммиачным буфером, индикатор– кислотный хром темно-синий, f=M, расчет производится на безводный препарат.
Хранение: хорошо укупоренная тара
Применение: источник кальция, антиаллергическое средство.
