Растворы. дисперсные системы 3 страница
= –0,2145 B.
При составлении гальванического элемента более отрицательным электродом будет система Zn | Zn2+, более положи-тельным – Pb | Pb2+. Схема гальванического элемента примет следующий вид
(–) Zn | ZnSO4 (0,01 M) || Pb(NO3)2 (0,001 M) | Pb (+).
При наличии внешней цепи на электродах протекают следующие реакции
Zn0 = Zn+2 + 2 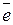 | окисление | восста- новитель | Анод | |
Pb2+ + 2 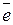 = Pb0 = Pb0 | восста- новление | окисли- тель | Катод |

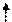 Реакция в элементе в целом Zn0 + Pb2+ = Zn2+ + Pb0.
Реакция в элементе в целом Zn0 + Pb2+ = Zn2+ + Pb0.
 |
2 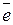
Электродвижущая сила этого элемента может быть рассчитана как по ранее определенным электродным потенциалам, так и непосредственно.
1 вариант E298 = φкатода – φанода = φ 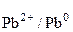 – φ
– φ 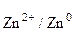 =
=
= – 0,2145 – (– 0,822) = 0,6075 В.
2 вариант
E298 = φ 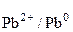 – φ
– φ 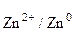 = φ
= φ 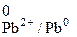 +
+ 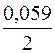 lg
lg 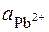 – φ
– φ 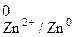 –
–
– 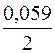 lg
lg 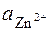 = (φ
= (φ 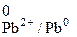 –φ
–φ 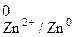 ) +
) + 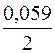 lg
lg 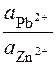 = (– 0,126 –
= (– 0,126 –
– (–0,763)) + 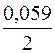 lg
lg 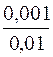 = 0,6075 B.
= 0,6075 B.
Если бы в условии были заданы металлы в разных степенях окисления, то следовало бы использовать величины количеств электронов z1, z2.
Пример 6.4. При электролизе раствора данной соли металла током I, A, масса катода возросла на m грамм. Учитывая, что выход по току металла Bi, %, рассчитайте, какое количество электричества и в течение какого времени пропущено. Составьте схему электролиза.
Дано: CoSO4; I = 1,25 A; m = 1,0883 г; Bi = 72 %.
Р е ш е н и е
Составляем схему электролиза с нерастворимым анодом. Электрохимическая система имеет следующий вид
(–) Fe | CoSO4, H2O | Ti (+).
В качестве покрываемого металла выбрано железо; нерастворимого анода – титан.
В растворе присутствуют следующие ионы и молекулы
CoSO4 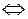 Co2+ + SO
Co2+ + SO 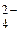 (электролитическая диссоциация);
(электролитическая диссоциация);
CoSO4 + 2H2O = Co(OH)2 + H2SO4 (гидролиз);
Со2+ + 2Н2О = Со(ОН)2 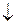 + 2Н+, рН < 7, среда кислая.
+ 2Н+, рН < 7, среда кислая.
Следовательно, при составлении схемы электролиза надо учитывать ионы Со2+, SO 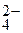 , Н+, молекулы СоSO4, H2O, Co(OH)2.
, Н+, молекулы СоSO4, H2O, Co(OH)2.
Реакции на электродах
А: 2Н2О = О2 + 4Н+ + 4 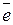 ;
;
К: Со2+ + 2 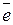 = Со0; 2Н+ + 2
= Со0; 2Н+ + 2 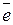 = Н2.
= Н2.
Из-за выделения водорода на катоде совместно с восстановлением ионов Со(II) выход по току металла меньше 100 %.
Схема электролиза водного раствора CoSO4 с нерастворимым анодом:
CoSO4
Катод Анод
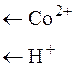
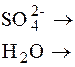
 |
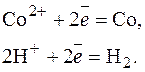
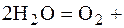 + 4
+ 4 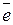 .+ 4
.+ 4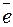 .
.
Далее составляем схему электролиза с растворимым анодом. Электрохимическая система:
(–) Fe | CoSO4, H2O | Co (+).
Реакции на электродах:
А:2Со0 = 2Со2+ + 4 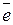 .
.
К:Со2+ + 2 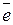 = Со0,
= Со0,
2Н+ + 2 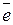 = Н2.
= Н2.
Схема электролиза водного раствора СоSO4 c растворимым анодом:
CoSO4
Катод Анод
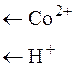
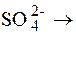
 Со2+ + 2
Со2+ + 2 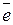 = Со0,
= Со0,
2Н+ + 2 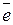 = Н2. 2Со0 = 2
= Н2. 2Со0 = 2 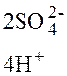 +4
+4 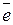 .
.
Количество электричества по закону Фарадея составит
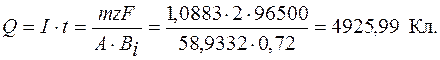
Оно пропущено в течение времени t:
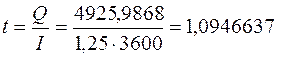 ч ≈ 1,1 ч.
ч ≈ 1,1 ч.
Пример 6.5. Установите, в какой последовательности вероятно восстановление на катоде при электролизе данных ионов, пользуясь значениями стандартных электродных потенциалов и перенапряжений. Объясните, когда возможно совместное восстановление металла и водорода на катоде. Чем отличается последовательность электрохимических реакций на аноде от аналогичной последовательности на катоде?
В растворе присутствуют следующие ионы: Ag+, Cr3+, Zn2+, Sn2+, H+.
Р е ш е н и е
Находим значения стандартных электродных потенциалов соответствующих электрохимических систем и перенапряжений.
| Ион | Ag+ | Cr3+ | Zn2+ | Sn2+ | H+ |
| Электрохимическая система | Ag+/Ag0 | Cr3+/Cr0 | Zn2+/Zn0 | Sn2+/Sn0 | 2H+/H 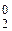 |
| φ0 , В | 0,799 | -0,744 | -0,763 | -0,136 | |
| ηк , В | 0,18 | 0,41 | 0,03 | 0,01 | 0,18 (на Ag) |
Рассчитываем значения катодных потенциалов в реальных условиях электролиза, под током
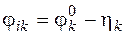 .
.
| Электрохимическая система | Ag+/Ag0 | Cr3+/Cr0 | Zn2+/Zn0 | Sn2+/Sn0 | 2Н+/Н02 |
| φiк , В | 0,619 | -1,154 | -0,766 | -0,146 | -0,18 (на Ag) |
Последовательность разряда ионов на катоде устанавливаем исходя из того, что на катоде восстанавливаются в первую очередь ионы с наиболее положительным электродным потенциалом соответствующей электрохимической системы.
| φiк , В | 0,619 | -0,146 | -0,18 | -0,766 | -1,154 |
| Электрохимическая система | Ag+/Ag0 | Sn2+/Sn0 | 2H+/H 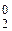 | Zn2+/Zn0 | Cr3+/Cr0 |
| Ион | Ag+ | Sn2+ | H+ | Zn2+ | Cr3+ |
Отсюда видно, что на катоде будут восстанавливаться в первую очередь ионы Ag+. При повышенных плотностях тока, в случае, если достигается предельный ток по ионам Ag+, может начаться восстановление ионов Sn2+, что используют, в частности, при электролитическом рафинировании металлов – можно отдельно выделить серебро, затем олово. Восстановления водорода в обычных условиях совместно с металлом – серебром не происходит, оно возможно лишь при плотностях тока, намного превышающих предельную по ионам Ag+.
Анодное поведение рассматриваемых ионов прямо противоположно катодному: на аноде в первую очередь будут идти процессы окисления в электрохимических системах с наиболее отрицательным электродным потенциалом.
Задачи
6.1. Для данного окислительно-восстановительного процесса:
а) составьте реакции окисления и восстановления; б) укажите окислитель и восстановитель; в) составьте сокращенное ионное и полное молекулярное уравнения ионно-электронным методом; г) покажите переход электронов; д) рассчитайте 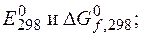
е) укажите возможное направление протекания процесса;
ж) составьте гальванический элемент на основе данной реакции.
Т а б л и ц а 6.1
| Вариант | Реакция |
H2O2 + KMnO4 + H2SO4  MnSO4 + K2SO4 + O2 + H2O MnSO4 + K2SO4 + O2 + H2O | |
NaNO2 + NaI + H2SO4  NO + I2 + Na2SO4 + H2O NO + I2 + Na2SO4 + H2O | |
NaI + H2SO4 + MnO2  NaHSO4 + H2O + I2 + MnSO4 NaHSO4 + H2O + I2 + MnSO4 | |
MnSO4 + S + K2SO4 + H2O  KMnO4 + H2S + H2SO4 KMnO4 + H2S + H2SO4 | |
K2SO4+ Cr2(SO4)3+ Fe2(SO4)3+ H2O  K2Cr2O7+H2SO4+FeSO4 K2Cr2O7+H2SO4+FeSO4 | |
KCl + Fe2(SO4)3 + H2O  KClO3 + FeSO4 + H2SO4 KClO3 + FeSO4 + H2SO4 | |
FeCl3 + MnCl2 + KCl + H2O  FeCl2 + KMnO4 + HCl FeCl2 + KMnO4 + HCl | |
K2SO4 + Cr2(SO4)3 + H2O  K2Cr2O7 + H2SO4 + SO2 K2Cr2O7 + H2SO4 + SO2 | |
K2Cr2O7 + H2S + H2SO4  Cr2(SO4)3 + S + K2SO4 + H2O Cr2(SO4)3 + S + K2SO4 + H2O | |
K2SO4 + I2 + NO2 + H2O  KI + HNO3 + H2SO4 KI + HNO3 + H2SO4 | |
Fe2(SO4)3 + NO + H2O  FeSO4 + HNO3 + H2SO4 FeSO4 + HNO3 + H2SO4 | |
MnSO4+Br2+Na2SO4+K2SO4 + H2O  KMnO4 + NaBr + H2SO4 KMnO4 + NaBr + H2SO4 | |
| Окончание табл. 6.1 | |
HMnO4 + Pb(NO3)2 + H2O  PbO2 + Mn(NO3)2 + HNO3 PbO2 + Mn(NO3)2 + HNO3 | |
KCl + NaCl + H2O + CO2  KClO3 + Na2C2O4 + HCl KClO3 + Na2C2O4 + HCl | |
Na2C2O4+KMnO4+H2SO4  MnSO4+K2SO4+Na2SO3+H2O+CO2 MnSO4+K2SO4+Na2SO3+H2O+CO2 | |
| 1’ | K2MnO4 + O2 + H2O  KMnO4 + H2O2 + KOH KMnO4 + H2O2 + KOH |
| 2’ | MnCl2 + Cl2 + KCl + H2O  KMnO4 + HCl KMnO4 + HCl |
| 3’ | HNO2 + KMnO4 + H2SO4  HNO3 + MnSO4 + K2SO4 + H2O HNO3 + MnSO4 + K2SO4 + H2O |
| 4’ | PbSO4 + ZnSO4 + H2O  PbO2 + H2SO4 + Zn PbO2 + H2SO4 + Zn |
| 5’ | Al2(SO4)3+Cr2(SO4)3+K2SO4+H2O  Al+K2Cr2O7+H2SO4 Al+K2Cr2O7+H2SO4 |
| 6’ | K2CrO4 + KBr +H2O + KCl  CrCl3 + Br2 + KOH CrCl3 + Br2 + KOH |
| 7’ | Na2SO4 + I2 + K2SO4 + H2O  Na2SO3 + KIO3 + H2SO4 Na2SO3 + KIO3 + H2SO4 |
| 8’ | Na2SO4 + Ag + NaNO3 + H2O  Na2SO3 + AgNO3 + NaOH Na2SO3 + AgNO3 + NaOH |
| 9’ | KI + KNO2 + H2SO4  I2 + NO + K2SO4 + H2O I2 + NO + K2SO4 + H2O |
| 10’ | CO2 + MnSO4 + H2O  H2C2O4 + MnO2 + H2SO4 H2C2O4 + MnO2 + H2SO4 |
| 11’ | H2O2 + PbO2 + CH3COOH  O2 + Pb(CH3COO)2 + H2O O2 + Pb(CH3COO)2 + H2O |
| 12’ | Ti(SO4)2+MnSO4+ K2SO4 + H2O  Ti2(SO4)3 + KMnO4 + H2SO4 Ti2(SO4)3 + KMnO4 + H2SO4 |
| 13’ | KBr + MnO2 + KCl + H2O  KBrO + MnCl2 + KOH KBrO + MnCl2 + KOH |
| 14’ | MnSO4 + NaHSO4 + H2O + Cl2  MnO2 + NaCl + H2SO4 MnO2 + NaCl + H2SO4 |
| 15’ | K2Cr2O7 + KI + H2SO4  Cr2(SO4)3 + I2 + K2SO4 + H2O Cr2(SO4)3 + I2 + K2SO4 + H2O |
6.2. Расчет электродвижущей силы гальванического элемента в стандартных условиях по известной реакции в элементе.
Дана реакция, протекающая в гальваническом элементе. Рассчитайте 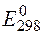 по данным
по данным 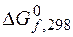 , составьте схему элемента, реакции на электродах.
, составьте схему элемента, реакции на электродах.
Т а б л и ц а 6.2
| Вариант | Реакции |
| PbO2 (к) + 2H2SO4 (ж) + Zn (к) = PbSO4 (к) + ZnSO4 (к) + 2H2O (ж) | |
| PbO2 (к) + 2H2SO4 (ж) + Cd (к) = PbSO4 (к) + CdSO4 (к) + 2H2O (ж) | |
| Cu2Cl2 (к) + Mg (к) = 2Cu (к) + MgCl2 (к) | |
| 2Ag (к) + MgCl2 (к) = 2AgCl (к) + Mg (к) | |
| PbO2 (к) + 2H2SO4 (ж) + Pb (к) = 2PbSO4 (к) + 2H2O (ж) | |
| 2Pb (к) + O2 (г) + 2H2O (ж) = 2Pb(OH)2 (к) | |
| O2 (г) + 2Sn (к) + 2H2O (ж) = 2Sn(OH)2 (к) | |
| O2 (г) + 2Mn (к) + 2H2O (ж) = 2Mn(OH)2 (к) | |
| Ag2O (к) + Cd (к) = 2Ag (к) + CdO (т) | |
| O2 (г) + 2Fe (т) + 2H2O (ж) = 2Fe(OH)2 (к) | |
| HgO (красн.к) + Zn (к) = ZnO (к) + Hg (к) | |
| 2CuCl (к) + Mg (к) = MgCl2 (к) + 2Cu (к) | |
| Th (к) + O2 (г) + 2H2O (ж) = Th(OH)4 (к) | |
| Окончание табл. 6.2 | |
| 2Ga (к) + 3/2 O2 (г) + 3H2O (ж) = 2Ga(OH)3 (к) | |
| 1’ | O2 (г) + 2Mg (к) + 2H2O (ж) = 2Mg(OH)2 (т) |
| 2’ | O2 (г) + 2Ni (к) + 2H2O (ж) = 2Ni(OH)2 (т) |
| 3’ | 3/2 O2 (г) + 2Fe (к) + 3H2O (ж) = 2Fe(OH)3 (к) |
| 4’ | Ag2O (к) + Zn (к) = 2Ag (к) + ZnO (к) |
| 5’ | CuCl2 (к) = CuCl (к) + ½ Cl2 (г) |
| 6’ | Cl2 (г) + Zn (к) = ZnCl2 (к) |
| 7’ | 2H2O (ж) + 2Li (к) = 2LiOH (к) + H2 (г) |
| 8’ | O2 (г) + 4Li (т) + 2CO2 (г) = 2Li2CO3 (т) |
| 9’ | Mg (к) + 2H2O (ж) = Mg(OH)2 (к) + H2 (г) |
| 10’ | O2 (г) + 2Zn (к) = 2ZnO (к) |
| 11’ | 3/2 O2 (г) + 2Au (к) + 3H2O (ж) = 2Au(OH)3 (к) |
| 12’ | 2Cd (к) + O2 (г) + 2H2O (ж) = 2Cd(OH)2 (к) |
| 13’ | 5Zn(к)+2KIO3(к)+6H2SO4(ж)=5ZnSO4(к)+I2(к)+K2SO4(к)+6H2O (ж) |
| 14’ | PbSO4 (к) + H2O (ж) = Pb (к) + ½ O2 (г) + H2SO4 (ж) |
6.3. Составьте схему гальванического элемента, образованного двумя данными металлами, погруженными в растворы солей с известной активностью ионов; рассчитайте ЭДС этого элемента и 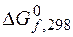 .
.
Т а б л и ц а 6.3
| Вариант | Металлы | Соли | Активности |
| Cr, Al | CrCl3, AlI3 | 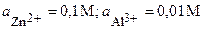 | |
| Mn, Co | MnCl2, CoCl2 | 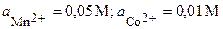 | |
| Fe, Cd | FeCl2, CdBr2 | 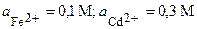 | |
| Cu, Ag | CuSO4, AgNO3 | 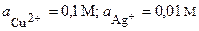 | |
| Sn, Al | SnBr2, AlCl3 | 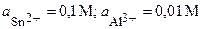 | |
| Au, Fe | AuCl3, FeCl2 | 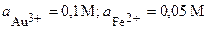 | |
| Cd, In | CdBr2, In(NO3)3 | 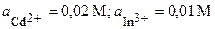 | |
| Sb, Co | SbF3, CoCl2 | 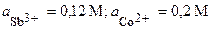 | |
| Cd, Ni | CdCl2, NiSO4 | 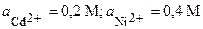 | |
| Re, Co | ReCl3, Co(NO3)2 | 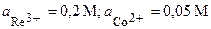 | |
| Pd, Cd | PdSO4, CdI2 | 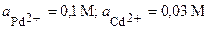 | |
| Sb, Co | SbCl3, CoSO4 | 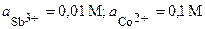 | |
| Окончание табл. 6.3 | |||
| Cr, Sn | CrBr3, SnCl4 | 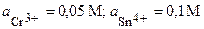 | |
| Nd, Mn | NdCl3, MnSO4 | 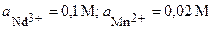 | |
| Sn, Cd | SnBr2, CdSO4 | 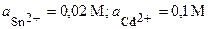 | |
| 1’ | Ti, Cr | TiCl3, CrCl2 | 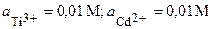 |
| 2’ | Mn, In | MnSO4, InBr3 | 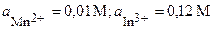 |
| 3’ | Pd, Cr | PdCl2, CrCl3 | 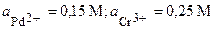 |
| 4’ | Ni, Nd | Ni(NO3)2, NdCl3 | 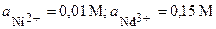 |
| 5’ | Re, Cr | ReCl3, Cr(NO3)3 | 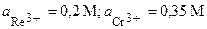 |
| 6’ | Cu, Cd | CuCl2, CdBr2 | 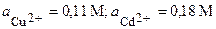 |
| 7’ | In, Cr | In(NO3)3, Cr2(SO4)2 | 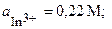 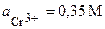 |
| 8’ | Mn, Cu | MnCl2, Cu(NO3)2 | 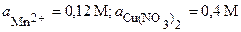 |
| 9’ | Ni, Cu | NiSO4, CuBr2 | 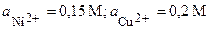 |
| 10’ | Ti, Fe | TiCl3, FeBr2 | 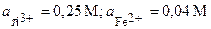 |
| 11’ | Cr, Fe | CrCl3, FeCl3 | 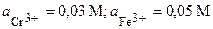 |
| 12’ | Mn, In | Mn(NO3)2, InCl3 | 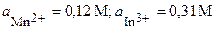 |
| 13’ | Pd, Fe | PdCl2, Fe(NO3)3 | 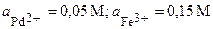 |
| 14’ | Ni, In | NiCl2, InBr3 | 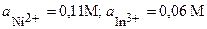 |
| 15’ | Re, Fe | ReCl3, Fe2(SO4)3 | 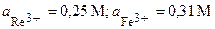 |
