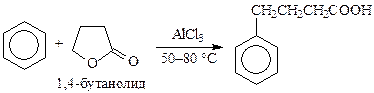Особенности технологии алкилирования аренов по Фриделю-Крафтсу
Условия проведения С-алкилирования аренов по Фриделю-Крафтсу определяются структурой субстрата и типом алкилирующего агента.
Алкилирование аренов алкилгалогенидамииспользуется наиболее широко и проводится в безводном инертном растворителе (например, нитробензоле) или в избытке субстрата в присутствии кислот Льюиса:
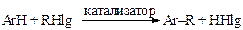
Активность алкилгалогенидов увеличивается от первичных к третичным. Скорость реакции может отличаться на 4 порядка, однако четкую границу во многих случаях провести нельзя, так как многое определяется катализатором.
Кислота Льюиса определяет, во-первых, строение и полярность электрофильной частицы, атакующей арен. При ее взаимодействии с алкилгалогенидом образуются поляризованный комплекс, ионная пара или карбокатион:
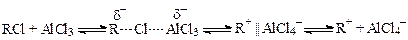
В связи с этим, во-вторых, кислота Льюиса, определяет скорость реакции, состав продуктов реакции и возможность изомеризации алкилгалогенида и продукта реакции.
Например, состав продуктов метилирования толуола метилбромидом и метилиодидом в одних и тех же условиях разный, поэтому можно предположить, что реакция протекает с участием разных электрофильных частиц. Если бы частицей был катион СН3+, состав продуктов был бы одинаков:
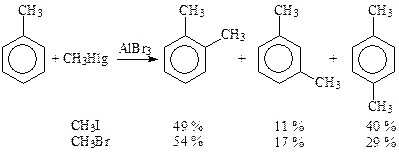
Активный катализатор в большей степени образует карбокатион, который до взаимодействия с ареном успевает изомеризоваться в более устойчивый. В случае малоактивного катализатора основной атакующей частицей является поляризованный комплекс, и изомеризация алкила не наблюдается. Например, при алкилировании бензола неопентилхлоридом в присутствии AlCl3 образуется трет.пентилбензол, а в случае FeCl3, — неопентилбензол:
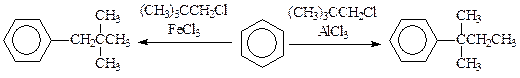
Хлористый алюминий практически всегда вызывает изомеризацию углеродной цепи галогеналкилов.
Алкилирование аренов геминальными ди-, три- и тетрагалогенидамиидет в тех же условиях, что и с алкилгалогенидами, с образованием ди- и трифенилметана и их производных:
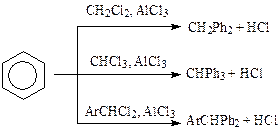
Однако четыре фенильных ядра к одному атому углерода не присоединяются:
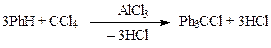
В производстве димедрола из тетрахлорметана и бензола получают дихлордифенилметан:
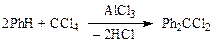
В синтезе противогрибкового препарата клотримазола используют о-хлорбензилидинхлорид или о-хлорбензофенон после превращения в дигалогенид:
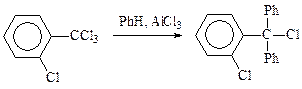
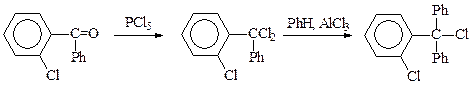
Алкилирование аренов алкенамиведут в присутствии протонных или апротонных кислот в безводном инертном растворителе или в избытке субстрата аналогично алкилированию галогенидами.
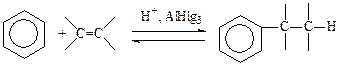
Образование электрофильных частиц проходит по схеме:
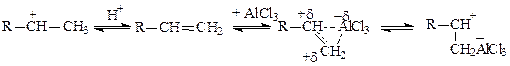
Согласно другой точке зрения кислота Льюиса в присутствии протонсодержащих веществ (следы воды, спирт и др.) сначала превращается в протонную кислоту, которая и катализирует процесс:
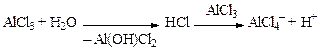
Радикалы при двойной связи повышают ее нуклеофильность и скорость взаимодействия с катализатором, поэтому, чем больше радикалов, тем активнее алкены в реакциях с аренами.
Этим способом получают этилбензол (из бензола и этилена), который затем превращают в стирол и используют в синтезе левомицетина и ряда других препаратов; изопропилбензол (из бензола и пропилена), который служит сырьем для синтеза фенола и ацетона по кумольному методу.
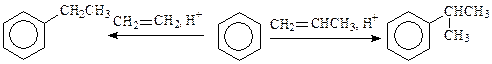
Алкилированием бензола неразветвленными, содержащими от 10 до 15 атомов углерода алкенами (или алкилхлоридами) в присутствии фтороводорода или хлорида алюминия, с последующим сульфированием образовавшихся продуктов, получают биологически мягкие поверхностно-активные вещества:
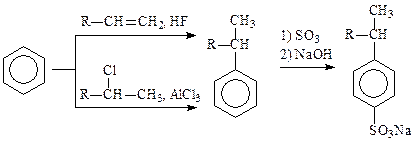
В ряде случаев используют сложные алкилирующие реагенты, как, например, в синтезе витамина Е триметилгидрохинон алкилируют непредельным спиртом изофитолом при 135—140 °С в среде о-ксилола с азеотропной отгонкой воды:
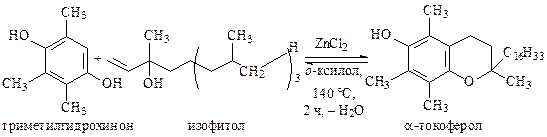
Алкилирование аренов спиртамиприменяют сравнительно редко, и ведут в присутствии сильных протонных кислот (серной и фосфорной), а также хлорида алюминия, алюмосиликата и др. Реакцию проводят как в жидкой, так и в паровой фазе.
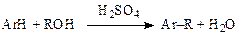
Электрофильные частицы образуются по следующим схемам:
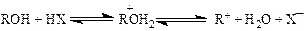
или
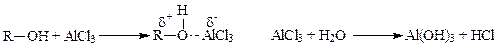
Реакционная способность спиртов в этих реакциях увеличивается от первичных к третичным.
В качестве примеров использования метода, можно привести синтез бутилоксианизола (антиоксидант для пищевой и химфармпромышленности), который ведут в присутствии фосфорной кислоты, и метилирование фенола метанолом в парах в синтезе 2,3,5-триметилфенола, который является сырьем в производстве витамина Е:
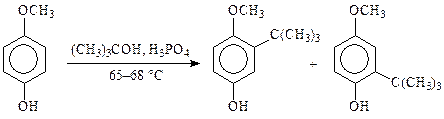
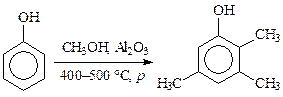
Иногда вместо спиртов используют их сложные эфиры. Так, в производстве хлорбутина алкилирование бензола проводят g-бутиролактоном в присутствии хлорида алюминия: