I. Приготовление рабочего раствора сыворотки
1. Депротеинизация сыворотки крови. В пробирку наливают 2 мл сыворотки крови и 5 мл спирта, перемешивают стеклянной палочкой, нагревают на водяной бане (800С) в течение 10 мин. Пробирку охлаждают и содержимое фильтруют через сухой фильтр в сухую пробирку.
2. Минерализация. Фильтрат (1 мл) переносят в тугоплавкую колбу Кьельдаля для сжигания и добавляют осторожно по стенкам колбы 10 капель концентрированной H2SO4. Через 15 минут после начала сжигания, в колбу Кьельдаля добавляют несколько капель пероксида водорода и продолжают нагревать до просветления жидкости. Колбу охлаждают и содержимое количественно переносят в мерную пробирку. Эти две стадии делаются предварительно, и студентам предлагается начать с нейтрализации полученного раствора.
3. Нейтрализация. Содержимое мерной пробирки доводят по бумажке с универсальным индикатором до рН = 7,0 (светло-зеленый цвет) 10%-ным раствором щелочи. В случае добавления избытка щёлочи проводят нейтрализацию 10%-ым раствором серной кислоты.
II. Определение концентрации фосфатидолхолинов по содержанию фосфора.
К содержимому мерной пробирки после нейтрализации добавляют 2,5 мл молибдата аммония и 0,5 мл 1% р-ра аскорбиновой кислоты, доводят водой до 10 мл. Пробу оставляют на 20 мин при комнатной температуре для развития окраски, а затем проводят измерение оптической плотности на ФЭК в кювете (1 см) при 670 нм. Схема определения представлена в таблице 1.
Параллельно строят калибровочную кривую (см. табл. 2). Расчёт содержания фосфора в пробе Сх (мкг/мл) проводят по калибровочному графику.
Схема определения оптической плотности исследуемого раствора, содержащего фосфор.
| Реактивы и этапы | Пробы | |
| Опыт | Контроль | |
| 1. Проба (мерная пробирка) | Весь объем | – |
| 2. Молибдат аммония, мл | 2,5 | 2,5 |
| 3. Аскорбиновая кислота, мл | 0,5 | 0,5 |
| 4. Н2О | до 10 мл | до 10 мл |
| Термостатируют 20 минут при комнатной температуре | ||
| 5. Фотометрируют против Н2О (λ= 670 нм, толщина кюветы 1 см) D670 | ||
| Dоп - Dк |
Данные для построения калибровочного графика
| Содержание фосфора в стандартном растворе, мкг/мл (Сх) | Dоп-Dк |
| 0,26 | |
| 0,54 | |
| 0,80 |
Расчет результатов
 По калибровочному графику находят содержание фосфора в пробе (Сх) в мкг/мл. Коэффициент пересчета содержания фосфора в одном мл: 2/7 (2 мл сыворотки + 5 мл спирта (см. пункт 1 «Депротеинизация сыворотки крови»).
По калибровочному графику находят содержание фосфора в пробе (Сх) в мкг/мл. Коэффициент пересчета содержания фосфора в одном мл: 2/7 (2 мл сыворотки + 5 мл спирта (см. пункт 1 «Депротеинизация сыворотки крови»).
Ср = 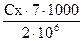 [г/л], где Ср – содержание фосфора в г/л
[г/л], где Ср – содержание фосфора в г/л
Так как усредненная молярная масса фосфатидилхолинов 750 г/моль, а фосфора 31 г/моль, то:
Содержание фосфатидилхолинов = 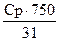 [г/л]
[г/л]
Норма: 1,5 – 2,5 г/л.
Выводы
Тестовые задания по теме: «Расщепление жиров, глицерина и высших жирных кислот»
1) Ответить на каждый вопрос однозначно: «да» или «нет»
1. Жиры расщепляются с образованием свободных жирных кислот.
2. Пальмитиновая и олеиновая жирные кислоты являются ненасыщенными соединениями.
3. Транспортной формой триацилглицеролов являются хиломикроны.
4. Глицерин нельзя отнести к жирам.
5. Наличие желчи ускоряет действие липазы.
6. Активирование жирных кислот требует затраты энергии.
7. Участвует ли карнитин в транспорте ВЖК внутрь митохондрии?
8. Может ли глицерин в живой клетке превращаться в 3-фосфоглицериновый альдегид?
9. Необходимо ли предварительное активирование жирной кислоты для синтеза нейтральных жиров?
10. Расщепляются ли белки под действием липазы?
11. Являются ли желчные кислоты производными циклопентанпергидрофенантрена?
12. Содержит ли фосфатидная кислота атом азота?
2) Выбрать один правильный ответ
| Гормон, активирующий липазу в адипоцитах: 1. инсулин 2. адреналин 3. кальцитонин 4. окситоцин 5. альдостерон | Биологической активностью обладают: 1. моноациглицеролы 2. диацилглицеролы 3. триацилглицеролы 4. глицерин 5. все вышеперечисленные соединения |
3) Установить соответствие для свободных и парных желчных кислот
| Свободная Коньюгированная с глицином Коньюгированная с таурином | А. Тауродезоксихолевая Б. Холевая В. Гликохолевая Г. Литохолевая |
