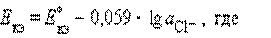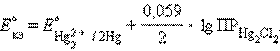Электроды второго рода
Электроды второго рода представляют собой металлические электроды, покрытые слоем труднорастворимой соли того же металла. При погружении в раствор соли одноименного аниона его потенциал будет определяться активностью иона в растворе.
а) Хлорсеребряный электрод (ХСЭ) Ag, AgCl|Cl– представляет собой серебряный проводник, покрытый твердым AgCl, который погружен в насыщенный раствор KCl.
Серебро электрохимически взаимодействует со своим ионом:
Ag+ + e– = Ag.
Уравнение Нернста для этого процесса:
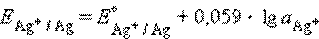 (16.2)
(16.2)
Однако в присутствии труднорастворимого AgCl активность ионов серебра очень мала, и ее трудно определить. Но активность ионов Ag+ связана с легко задаваемой в данной системе активностью ионов Cl– произведением растворимости хлорида серебра ПРAgCl:
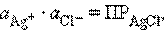 откуда
откуда
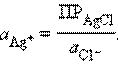
Подставляя это выражение в (16.2), получаем:
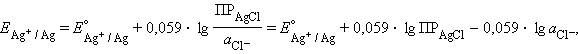
и обозначив
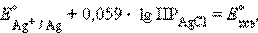
получим уравнение Нернста для хлорсеребряного электрода:
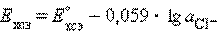 .
.
Потенциалопределяющими являются ионы хлора, а электродный процесс может быть представлен уравнением
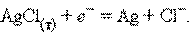
б) Каломельный электрод (КЭ) Hg, Hg2Cl2|Cl– – это ртуть, находящаяся в контакте с пастой из смеси ртути и каломели Hg2Cl2, которая, в свою очередь, соприкасается с насыщенным раствором KCl.
Принцип действия каломельного электрода тот же, что и хлорсеребряного.
Электродная реакция сводится к восстановлению каломели до металлической ртути:
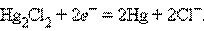
Потенциал каломельного электрода определяется активностью ионов хлора: