Лабораторная работа № 6. Приготовление раствора и определение его концентрации
Цель работы: Ознакомиться с методами приготовления растворов заданной концентрации и анализом раствора при помощи титрования.
Сущность работы: растворы часто готовят путем разведения более концентрированного раствора до необходимой величины концентрации. Концентрацию приготовленного раствора уточняют количественным химическим анализом, например, титрованием (прием количественного анализа, при котором к точному объему раствора определяемого вещества по каплям приливают раствор реагента точно заданной концентрации – титранта). Задача титрования – определить объем титранта, необходимый для установления точки эквивалентности (состояние системы, в котором аналитическая реакция прошла полностью). В эквивалентной точке изменяется окраска индикатора, что позволяет определить эквивалентный объем титранта.
Общие сведения
Раствором называется гомогенная (однородная) система, состоящая из двух или более компонентов, состав которой может непрерывно изменяться в определенных пределах. По агрегатному состоянию растворы могут быть газообразными, жидкими и твердыми.
В растворах выделяют растворитель и растворенное вещество. Растворителем называют компонент, который образует непрерывную среду. остальные компоненты, которые распределены в среде растворителя в виде дискретных частиц, называются растворенными веществами. Состав раствора (концентрация) чаще всего выражается следующими способами.
Массовая доля или процентное содержание w – соотношение масс растворенного mв вещества и раствора mр-р, выраженное в долях или процентах.
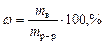 .
.
Концентрация, выраженная в граммах на литр, Сг/л – показывает, какая масса растворенного вещества mв, выраженная в граммах, содержится в единице объема раствора Vр-р:
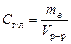 , г/л.
, г/л.
Молярная концентрация или молярность, СМ – число молей растворенного вещества nв в одном дм3 (л) раствора:
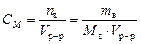 , моль/л.
, моль/л.
Моляльная концентрация или моляльность, Сm– число молей растворенного вещества, приходящееся на один килограмм растворителя:
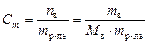 , моль/кг.
, моль/кг.
Мольная доля или мольные проценты xi – число молей компонента (растворителя или растворенного вещества) содержащееся в одном моле раствора:
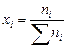 .
.
Нормальная концентрация или нормальность, CN – количество эквивалентов растворенного вещества nэв, содержащееся в одном литре раствора:
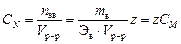 экв/л,
экв/л,
где z – количество обменных эквивалентов растворенного вещества, содержащееся в одном его моле.
Прием количественного анализа, при котором к раствору определяемого вещества по каплям приливают раствор реагента точно заданной концентрации, называют титрованием. Состояние системы, в котором аналитическая реакция прошла полностью в соответствии со стехиометрическим уравнением при отсутствии избытка реагента, называют точкой эквивалентности. Задача титрования – определить эквивалентный объем добавляемого реагента – титранта, необходимый для установления точки эквивалентности, так как в ней числа эквивалентов определяемого вещества и титранта равны между собой. Из определения нормальной концентрации следует, что число эквивалентов вещества в растворе равно произведению нормальности на объем раствора. Следовательно:
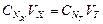 .
.
Отобрав для титрования мерной пипеткой точный объем пробы Vx, зная нормальность титранта 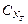 и определив эквивалентный объем VT, можно вычислить концентрацию пробы
и определив эквивалентный объем VT, можно вычислить концентрацию пробы 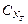 .
.
До эквивалентной точки в ходе титрования в растворе присутствует избыток определяемого вещества, а после – избыток титранта. Поэтому в эквивалентной точке свойства раствора резко изменяются, в частности, изменяется окраска специально подобранных цветных индикаторов, что позволяет определить эквивалентный объем титранта.
Выполнение работы
Приготовление раствора
1. При помощи ареометра определить плотность сходного раствора соляной кислоты. По таблице 1 определить концентрацию исходного раствора кислоты.
Плотности водных растворов соляной кислоты при 20 °С
Таблица 1.
| Плотность раствора, г/см3 | Концентрация раствора | |
| % | моль/л | |
| 1,01 | 2,3640 | 0,655 |
| 1,02 | 4,3880 | 1,227 |
| 1,03 | 6,4330 | 1,817 |
| 1,04 | 8,4900 | 2,421 |
| 1,05 | 10,5200 | 3,029 |
| 1,06 | 12,5100 | 3,638 |
| 1,07 | 14,5000 | 4,253 |
| 1,08 | 16,4700 | 4,878 |
2. Рассчитать, какой объем исходного раствора соляной кислоты следует взять для приготовления 100 мл раствора заданной преподавателем концентрации.
3. Рассчитанный объем исходного раствора из бюретки отобрать в мерную колбу, довести уровень жидкости в колбе дистиллированной водой до метки по нижнему краю мениска и перемешать раствор путем переворачивания плотно закрытой колбы.
