Стандартные электродные потенциалы j0 некоторых металлов
| Электрод | j0, В | Электрод | j0, В |
| Li+/Li | -3,05 | Cd2+/Cd | -0,40 |
| Rb+/Rb | -2,93 | Co2+/Co | -0,28 |
| K+/K | -2,92 | Ni2+/Ni | -0,25 |
| Ba2+/Ba | -2,90 | Sn2+/Sn | -0,136 |
| Ca2+/Ca | -2,87 | Pb2+/Pb | -0,127 |
| Na+/Na | -2,71 | 2H+/H2 | 0,00 |
| Mg2+/Mg | -2,37 | Sb3+/Sb | +0,20 |
| Al3+/Al | -1,70 | Bi3+/Bi | +0,22 |
| Ti2+/Ti | -1,60 | Cu2+/Cu | +0,34 |
| V2+/V | -1,18 | Ag+/Ag | +0,80 |
| Mn2+/Mn | -1,18 | Hg2+/Hg | +0,85 |
| Zn2+/Zn | -0,76 | Pt2+/Pt | +1,19 |
| Cr3+/Cr | -0,74 | Au3+/Au | +1,50 |
| Fe2+/Fe | -0,44 |
|
 |
|
|
|
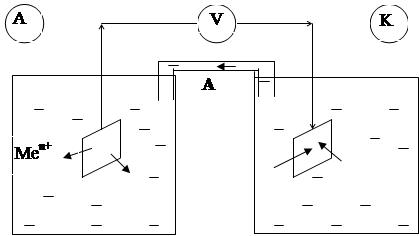
А- - анионы соли
Электродный процесс (31) Электродный процесс (32) или (33)
Рис. 2. Схема работы гальванического элемента
Электродвижущая сила Е характеризует способность гальванического элемента совершать электрическую работу:
Е = j К - jА (34)
Электрическая работа определяется максимально полезной работой, совершаемой химической реакцией, которая равна изменению изобарно-изотермического потенциала DG:
DG = - nFE, (35)
где n – число электронов.
Известно, что при самопроизвольном процессе DG <0, поэтому величина Е должна быть больше нуля Е >0 и jК > jА.
Величина 
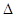 G связана с константой равновесия реакции соотношениями:
G связана с константой равновесия реакции соотношениями:

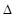 G =-RTlnKравн (36)
G =-RTlnKравн (36)

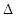 G =-2,3RTlgKравн, (37)
G =-2,3RTlgKравн, (37)
где R – универсальная газовая постоянная, R = 8,31 Дж/моль·К;
Т – температура.
Гальванические элементы являются первичными (однократно используемыми) химическими источниками тока (ХИТ). Вторичными (многократно используемыми) ХИТ являются аккумуляторы. Процессы, протекающие при зарядке и разрядке аккумуляторов, взаимообратны.
Гальваническиеэлементы, у которых электроды выполнены из одного и того же металла и опущены в раствор своих солей разной концентрации, называются концентрационными. Функцию анода в таких элементах выполняет металл, опущенный в раствор соли с меньшей концентрацией, например:


А Zn | ZnSO4|| ZnSO4| Zn K
C1 < C2
Пример 1. Составьте схему гальванического элемента, в основе работы которого лежит следующая реакция: Mg + ZnSO4 « MgSO4 + Zn. Что является катодом и анодом в этом элементе? Напишите уравнения процессов, протекающих на электродах. Рассчитайте ЭДС элемента при стандартных условиях (Т=298 К) и определите, в каком направлении реакция протекает самопроизвольно. Вычислите константу равновесия для токообразующей реакции.

 Решение. В таблице находим значения стандартных электродных потенциалов систем Zn/Zn2+ и Mg/Mg2+: j0Zn/Zn2+= -0,76 B, j0Mg/Mg2+= -2,37 B.Поскольку j0Mg/Mg2+<j0Zn/Zn2+,то магниевый электрод является анодом, а цинковый катодом. Схема гальванического элемента имеет вид:
Решение. В таблице находим значения стандартных электродных потенциалов систем Zn/Zn2+ и Mg/Mg2+: j0Zn/Zn2+= -0,76 B, j0Mg/Mg2+= -2,37 B.Поскольку j0Mg/Mg2+<j0Zn/Zn2+,то магниевый электрод является анодом, а цинковый катодом. Схема гальванического элемента имеет вид:
А Mg | MgSO4 || ZnSO4 | Zn K
 На аноде идет процесс окисления:
На аноде идет процесс окисления:
А Mg – 2ē ® Mg2+
 На катоде – восстановление катионов среды:
На катоде – восстановление катионов среды:
К Zn2++2ē ® Zn
ЭДС гальванического элемента Е = jК - jА = -0,76-(-2,37) = 1,61 В.
Величина 
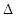 Е >0,следовательно, реакция протекает самопроизвольно в прямом направлении. По уравнению (37) вычисляем константу равновесия токообразующей реакции:
Е >0,следовательно, реакция протекает самопроизвольно в прямом направлении. По уравнению (37) вычисляем константу равновесия токообразующей реакции:
lgKравн.= 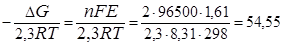 .
.
Потенциируя это уравнение, находим К = 3,5·1054. Поскольку К >> 1, то суммарная реакция протекает самопроизвольно в прямом направлении и практически необратима.
Пример 2. Составьте схему гальванического элемента, состоящего из цинкового и серебряного электродов, погруженных в растворы их солей с концентрациями ионов: СZn2+ = 0,1 моль/л, СAg+ = 0,01 моль/л. Укажите катод и анод. Напишите уравнения реакций, протекающих на данных электродах, а также суммарное уравнение реакции в гальваническом элементе. Рассчитайте ЭДС элемента.
Решение. Так как концентрации ионов не равны единице, то вначале рассчитаем потенциалы электродов, используя формулу Нернста. Если в условии задачи отсутствуют значения температуры, то её принимают равной стандартной температуре Т = 298 К. Поэтому будем использовать уравнение (30):
j=j0+ 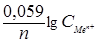 .
.
Подставим числовые значения в эту формулу, используя данные табл. 6:
jZn/Zn2+= -0,76 + 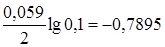 B,
B,
jAg/Ag+= 0,80 + 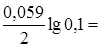 0,741 B.
0,741 B.
Из расчета видно, что jZn/Zn2+< jAg/Ag+.Поэтому цинковый электрод является анодом, а серебряный – катодом.

 Схема гальванического элемента:
Схема гальванического элемента:
A Zn | Zn2+ || Ag+ | Ag K
Вычислим ЭДС элемента по формуле (34):
E= jК - jА = 0,741 – (-0,789) = 1,530 B
Теперь запишем электродные реакции.
 На аноде идет процесс окисления:
На аноде идет процесс окисления:
А Zn – 2ē ® Zn2+ ,
 а на катоде – восстановления:
а на катоде – восстановления:
К 2Ag+ + 2 ē ® 2Ag.
Складывая уравнения электродных процессов (с учетом числа принимаемых и отдаваемых электронов), получаем суммарное уравнение реакции:
Zn + 2Ag+ ® Zn2+ + 2Ag.
ЗАДАЧИ
161-164. Напишите уравнения катодного и анодного процессов и составьте схему гальванического элемента, при работе которого протекает следующая реакция (см. номер задачи). На основании стандартных электродных потенциалов рассчитайте константу равновесия данной реакции и ЭДС элемента.
| № задачи | Реакция | Ответы |
| Zn + CuSO4 = ZnSO4 + Cu | Кр = 2,5·1037; Е = 1,103 В. | |
| Sn + PbCl2 = SnCl2 + Pb | Кр = 2; Е = 9·10-3 В. | |
| Zn + Pb(NO3)2 = Zn(NO3)2 + Pb | Кр = 3,5·1021; Е = 0,636 В. | |
| Zn + CdSO4 = ZnSO4 + Cd | Кр = 1,56·1012; Е = 0,36 В. |
165-169. Постройте график зависимости ЭДС гальванического элемента от логарифма концентрации ионов металла одного из электродов в растворе:
а) 10; б) 1; в) 0,1; г) 0,01; д) 0,001 моль/л, считая концентрацию ионов другого металла постоянной и равной CMe,2. Напишите уравнение суммарной реакции, протекающей в гальваническом элементе. При каких концентрациях ионов элемент работает за счет протекания реакции в прямом направлении?
Ме1 – анод; Ме2 – катод.
| № задачи | Гальванический элемент | СМе,2, моль/л |
| Sn | Sn2+ || Pb2+ | Pb | 0,1 | |
| Al | Al3+ || Fe2+ | Fe | ||
| Cd | Cd2+|| Ni2+ | Ni | 10-3 | |
| Ni | Ni2+ || Cu2+ | Cu | ||
| Fe | Fe2+ || Sn2+ | Sn | 0,1 |
170-173.Запишите уравнения электродных реакций и составьте схему гальванического элемента, работа которого выражается уравнением, представленным в таблице. Рассчитайте его ЭДС при Т = 298 К и концентрациях солей С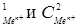 ,в растворы которых опущены электроды. Сделайте вывод о том, в каком направлении возможно самопроизвольное протекание реакции.
,в растворы которых опущены электроды. Сделайте вывод о том, в каком направлении возможно самопроизвольное протекание реакции.
Ме1 – анод, Ме2 – катод.
| № задачи | Реакция | С 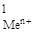 , моль/л , моль/л | С 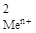 , моль/л , моль/л | Ответы |
| Fe + 2Ag+ « 2Ag + Fe2+ | 0,01 | 0,1 | 1,24 | |
| Ni + Cu2+ « Ni2+ + Cu | 0,1 | 0,1 | 0,59 | |
| Mg + Pb2+ « Mg2+ + Pb | 0,01 | 2,184 | ||
| Zn + Ni2+ « Ni + Zn2+ | 0,01 | 0,01 | 0,513 |
174-177.Составьте схему гальванического элемента, состоящего из металлов Ме1 и Ме2, погруженных в растворы их солей при концентрациях С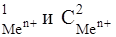 ,указанных в таблице. Напишите электронные уравнения катодных и анодных процессов. Рассчитайте ЭДС элемента. Изменится ли величина ЭДС, если концентрацию каждого из ионов понизить в 10 раз?
,указанных в таблице. Напишите электронные уравнения катодных и анодных процессов. Рассчитайте ЭДС элемента. Изменится ли величина ЭДС, если концентрацию каждого из ионов понизить в 10 раз?
| № задачи | Ме1 | Ме2 | С 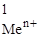 , моль/л , моль/л | С 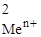 , моль/л , моль/л | Ответы |
| Zn | Ni | 0,01 | 0,01 | 0,513 В | |
| Fe | Cu | 0,1 | 0,01 | 0,750 В | |
| Fe | Ag | 0,001 | 0,01 | 1,210 В | |
| Mg | Fe | 0,01 | 1,99 В |
178.Какой гальванический элемент называется концентрационным? Составьте схему, напишите уравнениякатодного и анодного процессов, вычислите ЭДС гальванического элемента, состоящего из серебряных электродов, опущенных: первый - в 0,01 М, второй – в 0,1 М растворы AgNO3.
Ответ: 0,059 В.
179.Составьте схемы двух гальванических элементов, в одном из которых никель был бы катодом, а в другом – анодом.Напишите для каждого из этих элементов уравнения реакций, протекающих на катоде и аноде,рассчитайте их ЭДС при стандартных условиях. Изменится ли ЭДС, если концентрацию каждого из ионов уменьшить в 10 раз?
180.Железная и серебрянаяпластины соединены внешним проводником и погружены в раствор серной кислоты. Составьте схему данного гальванического элемента и напишите электронные уравнения процессов, происходящих на катоде и аноде.
Коррозия металлов
Коррозия – самопроизвольное разрушение металлов в результатевзаимодействия с окружающей средой.
По механизму протекания коррозия подразделяется на химическую и электрохимическую. Химическая коррозия протекает в газовой среде при повышенных температурах (в отсутствии влаги) или в жидких неэлектролитах. Сущность процессов коррозии этого вида сводится к окислительно-восстановительной реакции, осуществляемой непосредственным переходом электронов металла на окислитель. В качестве окислителя могут выступать такие газы, как O2 , SO2, Cl2, HCl и др. Коррозии способствуют также H2S, CO2. В результате реакции на поверхности металла образуются пленки оксидов, сульфидов, хлоридов и т.д. Развитие коррозии происходит за счет переноса катионов металла и частиц окислителя через эту пленку во встречных направлениях. Если образуется плотная сплошная, хорошо сцепленная с металлом пленка, то дальнейшее окисление металла протекает очень медленно. Такие пленки могут быть использованы для защиты металлов от коррозии. Напротив, пористая рыхлая пленка не способна защищать металл от взаимодействия с окружающей средой.
Качество пленки определяется на основании расчета фактора рыхлости П:
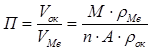 ,(38)
,(38)
где Voк – молярный объем продуктов коррозии;
rок – их плотность;
VMe – молярный объем металла;
М – молярная масса продукта коррозии (оксида, сульфида, хлорида и т.д.);
А – атомная масса металла;
rМе – плотность металла;
n – число атомов металла в молекуле оксида, сульфида и др.
Если П<1, то образуется плёнка, частично покрывающая поверхность металла (рыхлая пленка).
Сплошные плёнки получаются при условии 1<П<2,5.
Если фактор рыхлости П>2,5,то в плёнке возникают напряжения, разрушающие ее и нарушающие сплошность (плёнка растрескивается).
Пример 1.При химической коррозии железа в атмосфере сухого воздуха, содержащего газообразные Cl2, H2S и O2, образуются пленки FeS, FeO, FeCl2. Напишите уравнения образования этих соединений. Рассчитайте фактор рыхлости П и сделайте вывод о защитных свойствах плёнок. Плотности rFe = 7,87; rFeS = 4,7; rFeО = 5,7; rFeCl 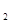 = 2,9 г/см3.
= 2,9 г/см3.
Решение. Плёнки образуются при взаимодействии с агрессивной средой в результате следующих реакций:
2Fe + 2H2S + O2 ® 2FeS + 2H2O
2Fe + O2 ® 2FeO
Fe + Cl2 ® FeCl2
Находим значения фактора рыхлости П:
ПFeS = 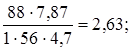 Fe0 =
Fe0 = 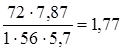 ;
;
ПFeCl 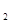 =
= 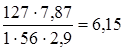 .
.
Поскольку для сульфидной и хлоридной пленок П > 2,5, то возможно их растрескивание и нарушение сплошности. Критерий П для оксидной пленки лежит в интервале 1 < ПFe0 < 2,5. Следовательно, пленка FeO является сплошной и обладает хорошими защитными свойствами.
Электрохимическая коррозия – самопроизвольное разрушение металлов в присутствии электролитов (жидких или расплавленных веществ, проводящих электрический ток) в результате образования микрогальванических элементов.
При электрохимической коррозии процессы окисления и восстановления протекают на участках, имеющих различные значения электродных потенциалов j.
На анодных участках, имеющих меньшее значение j, происходит окисление металла:
 А Me – nē ® Men+
А Me – nē ® Men+
При этом электроны внутри металла перемещаются к катодным участкам, на которых происходит восстановление ионов или молекул из коррозионной среды. В зависимости от состава среды возможны следующие процессы:
 в кислой среде:
в кислой среде:
К 2Н+ + 2ē = Н2;
 в нейтральной или слабощелочной среде:
в нейтральной или слабощелочной среде:
К 2Н2О + 2ē = Н2 + 2ОН-.
Наиболее вероятным катодным процессом при наличии растворенного в воде воздуха является следующий:

К О2 + 2Н2О + 4ē = 4ОН-.
Пример 2. Составьте электронные уравнения катодного и анодного процессов коррозии железа с примесью никеля в а) соляной кислоте и б) влажном воздухе. Каков состав продуктов коррозии?
Решение. Выпишем стандартные электродные потенциалы металлов: j0 Fe/Fe2+ = -0,44 В;
j0Ni/Ni2+ = -0,25 В.
Поскольку j0Fe/Fe2+ < j0Ni/Ni2+ , железо выполняет функциюанода,а никель – катода.
 а) В кислой среде электронные уравнения процессов имеют вид:
а) В кислой среде электронные уравнения процессов имеют вид:
АFe – 2ē ® Fe2+–анодное окисление;

К 2Н+ + 2ē ® Н2 –катодное восстановление.
Продуктами коррозии являются хлорид железа FeCl2 и водород.
б) Во влажном воздухе на катодном и анодном участках происходят следующие реакции:
 А Fe - 2ē ® Fe2+,
А Fe - 2ē ® Fe2+,

К О2 + 2Н2О + 4ē ® 4ОН-;
Продукт коррозии: Fe2+ + 2OH- ® Fe(OH)2.
В присутствии влаги и кислорода происходит дальнейшее окисление железа до трехвалентного состояния:
4 Fe(OH)2 + 2H2O + O2 = 4 Fe (OH)3.
Для количественной оценки коррозионной стойкости металлов используют массовые ( j ) и линейные (П) показатели.
Скорость коррозии j определяется:
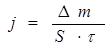 (г/м2·час или г/м2·год), (39)
(г/м2·час или г/м2·год), (39)
где Dm – изменение массы образца, г, при коррозии металла в течение времени t, час (или год) на поверхности S, м2.
Глубинный показатель коррозии П равен:
П =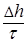 (мм/год), (40)
(мм/год), (40)
где Dh – толщина металла, мм, разрушенного в течение времени t, год.
Величины П и j связаны соотношением:
П= 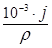 ,если j измеряется в г/м2·год;
,если j измеряется в г/м2·год;
или П = 8,76 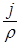 , если j измеряется в г/м2·час;
, если j измеряется в г/м2·час;
где r – плотность металла, г/см3.
Защита металлов от коррозии
Защита металлов от коррозии в основном осуществляется путем создания изолирующих плёнок или ингибирующих покрытий, а также электрохимическими методами (включая гальванические покрытия).

 Металлические покрытия делятся на катодные и анодные в зависимости от соотношения электродных потенциалов j защищаемого изделия (Ме1) и покрытия (Ме2).
Металлические покрытия делятся на катодные и анодные в зависимости от соотношения электродных потенциалов j защищаемого изделия (Ме1) и покрытия (Ме2).









































 А К
А К















 Ме2 Ме2
Ме2 Ме2


Ме1 К Ме1 А
а) б)
Рис. 3. Анодное а) и катодное б) покрытия
При нарушении целостности покрытия оба металла соприкасаются с агрессивной средой, возникает гальванический элемент. Если j1>j2, то Ме2 будет анодом (анодное покрытие), а Ме1 –катодом. Анодное покрытие очень эффективно, т.к., разрушаясь само, оно предохраняет защищаемый металл от разрушения.
Если j1<j2, то при нарушении целостности покрытия, защищаемый металл будет анодом, а металл покрытия - катодом. Катодные покрытия защищают металл до тех пор, пока пленка будет сплошной.
Электрохимическая защита подразделяется на катодную, протекторную и анодную. В коррозионную среду вводят также ингибиторы.
Ингибиторами называются добавленные в раствор вещества, которые накапливаются на границе металл – электролит и снижают скорость коррозии.
Эффективность действия ингибиторов оценивается величинами коэффициента торможения К и степени защиты Z:
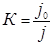 ;
; 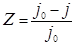 ×100%,(41)
×100%,(41)
где j0 – скорость коррозии в растворе без ингибитора,
j – с ингибитором.
Величина К показывает, во сколько раз снижается скорость коррозии металла при введении ингибитора.Z характеризует относительное понижение скорости коррозии.
Пример 3. Можно ли использовать цинковое покрытие для защиты стального изделия от коррозии во влажном воздухе? Составьте электронные уравнения катодного и анодного процессов коррозии, наблюдаемой при нарушении этого покрытия. Каков состав продуктов коррозии? Какой должна быть толщина покрытия, чтобы оно прослужило 5 лет, если величина его глубинного показателя П равна 0,16 мм/год? Покрытие считается недействующим, если его остаточная толщина составляет 18 % от первоначального значения.
Решение. Сопоставляя электродные потенциалы 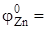 -0,76 В и
-0,76 В и 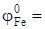 -0,44 В, мы видим, что
-0,44 В, мы видим, что 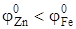 . Следовательно, цинк по отношению к железу будет являться анодом. Цинковое покрытие – анодное. На аноде идет процесс окисления:
. Следовательно, цинк по отношению к железу будет являться анодом. Цинковое покрытие – анодное. На аноде идет процесс окисления:

А Zn - 2ē ® Zn2+.
На катоде (Fe) процесс восстановления частиц среды (во влажном воздухе это кислород и вода):

К О2 + 2Н2О + 4ē = 4ОН-.
Продукт коррозии: Zn2+ + 2OH- ® Zn (OH)2
При нарушении покрытия сталь не растворяется, следовательно, цинковое покрытие использовать можно.
Толщину покрытия Dh можно найти из уравнения (40):
П = 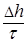 , откуда Dh = П×t = 0,16×5=0,8 (мм).
, откуда Dh = П×t = 0,16×5=0,8 (мм).
Но коррозии подвержено 82 % первоначальной толщины. Тогда вся толщина покрытия должна быть равной 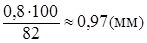 .
.
ЗАДАЧИ
181-183.Можно ли использовать предлагаемый материал в качестве протектора для защиты стального изделия от коррозии в природной воде, насыщенной кислородом?
Составьте электронные уравнения катодного и анодного процессов коррозии. Каков состав продуктов коррозии?
Определите возможный срок службы протектора сечением а х×в, если скорость его коррозии j, г/м2×год, а масса m, г.
| № задачи | Материал протектора | а, см | в, см | j, 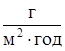 | m, г | Ответы |
| Zn | ||||||
| Al | 2,5 | |||||
| Mg |
184-188. Составьте электронные уравнения анодного и катодного процессов коррозии стального трубопровода, содержащего включение А, во влажной почве (Н2О и О2). Каков состав продуктов коррозии?
Рассчитайте необходимую толщину стенок трубопровода (мм), который должен прослужить tлет, если скорость его коррозии равна j. Остаточная толщина стенок трубопровода должна быть не меньше 25% от первоначального значения. Плотность железа r = 7,87 г/см3.
| № задачи | Примесь А | j, кг/м2·год | t, лет | Ответы, мм |
| Ni | 3,305 | 8,4 | ||
| Sn | 6,558 | 6,67 | ||
| Pb | 4,984 | 5,07 | ||
| Cu | 1,695 | 3,73 | ||
| Sb | 6,690 | 4,53 |
189-192.Можно ли использовать данное покрытие для эффективной защиты стального изделия от коррозии во влажном воздухе?
Составьте электронные уравнения катодного и анодного процессов коррозии, возникающей при нарушении целостности покрытия. Каков состав продуктов коррозии?
Какой должна быть толщина покрытия, чтобы оно прослужило tлет, если величина его глубинного показателя коррозии П, мм/год. Покрытие считается действующим до тех пор, пока его остаточная толщина не составит 15% от первоначального значения.
| № задачи | Металл покрытия | t, лет | П, мм/год | Ответы, мм |
| Mg | 0,7 | 3,3 | ||
| Zn | 0,3 | 1,76 | ||
| Al | 0,6 | 3,53 | ||
| Ti | 0,3 | 4,23 |
193-196. При химической коррозии металлов (Ме) в атмосфере сухого воздуха, содержащего газообразные O2, HCl, H2S, под воздействием высоких температур образуются пленки продуктов коррозии.
Напишите уравнения образования этих соединений.
Зная плотности металлов, их оксидов, хлоридов, сульфидов, определите, какие из плёнок будут обладать защитным действием.
| № задачи | Металл, Ме | rМе, г/см3 | Продукты коррозии и их плотности, г/см3 |
| Fe | 7,87 | FeO – 5,7; Fe2O3 – 5,25; FeCl2 – 2,98; FeS2 – 5,03; Fe3O4 – 5,18. | |
| Cu | 8,94 | CuO – 6,46; Cu2O – 3,7; CuCl2 – 3,05; Cu2S – 5,4; CuS - 4,68. | |
| Mn | 7,44 | MnO – 5,18; Mn2O3 - 4,3; Mn3O4 – 7,42; MnCl2 - 2,98; MnO2 - 5,03. | |
| Ni | 8,91 | NiO - 7,45; Ni2S3 - 5,82; NiCl2 - 3,51; NiS - 4,1. |
197-200.Металлическое изделие, содержащее примесные включения А, сильно корродирует в растворе HCl. Скорость коррозии составляет j0, г/м2·час. Для замедления процесса в растворах кислот используют ингибиторы. Скорость коррозии изделия в присутствии ингибитора – j. Определите коэффициент торможения коррозии К и степень защиты Z.
Составьте электронные уравнения катодного и анодного процессовкоррозии изделия в кислоте. Каков состав продуктов коррозии?
| № задачи | Металл изделия | Примесь А | j0 | j | Ответы |
| Fe | Sb | 1,25 | 0,36 | 3,5; 71,2% | |
| Fe | Ni | 1,05 | 0,13 | 8,0; 87,6% | |
| Cd | Sn | 0,45 | 0,14 | 3,2; 68,9% | |
| Zn | Cu | 9,6 | 2,6; 61,6% |
ЭЛЕКТРОЛИЗ
Электролизомназывается окислительно-восстановительная реакция, которая протекает на электродах при пропускании через раствор или расплав электролита электрического тока.
При этом катод электролизёра подключается к отрицательному полюсу источника тока, анод - к положительному. Аноды, используемые при электролизе, подразделяются на инертные (графит, уголь, Рt, Аu, Jr)и активные, или растворимые (все остальные металлы). Активные анодырастворяются в первую очередь в ходе электролиза: Ме0 – nē = Men+.
При электролизе с инертным анодом в первую очередь окисляются простые ионы (I-, Br-, Cl-,OH-).Если таких ионов в растворе нет, то тогда окисляются молекулы воды: 2 H2O - 4ē = O2 + 4H+. Сложные ионы (SO 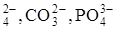 и др.) из водных растворов не окисляются – вместо них окисляется вода.
и др.) из водных растворов не окисляются – вместо них окисляется вода.
Последовательность процессов окисления на аноде можно представить следующей схемой:
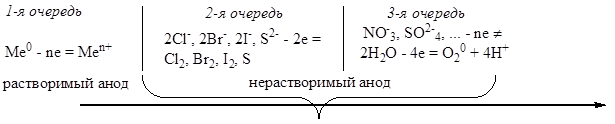
На катоде более легко восстанавливаются частицы с наибольшим электродным потенциалом. Продукты восстановления определяются величиной стандартного электродного потенциала металла. Последовательность разряда на катоде в водной среде можно представить следующей схемой:
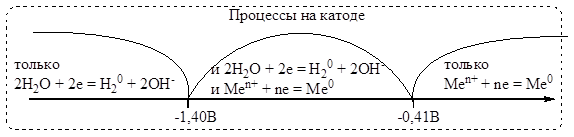
В соответствии с этой схемой из водных растворов восстанавливаются только те металлы, у которых электродный потенциал jMe/Men+>jH2O= -0,41 B.
Активное разложение воды происходит при потенциале металла jMe/Men+< -1,4 B.Как видно из рисунка, существует зона конкурирующих процессов (-1,4 B < jMe/Men+ < -0,41 B).
В расплавах молекулы воды отсутствуют. Поэтому на катоде и аноде протекают процессы с участием только ионов расплава.
Пример 1. Составьте электронные уравнения катодных и анодных процессов, протекающих при электролизе раствора K2SO4 с графитовыми электродами.
Решение. В водном растворе сульфат калия K2SO4 диссоциирует на ионы:
K2SO4 « 2K+ + SO42-
К катоду подходят катионы К+ и H2O, к аноду – анионы SO42- и Н2О. Поскольку потенциал системы jк/к+ = -2,924 В (табл. 6, с. 49) меньше, чем –1,4, то на катоде будут восстанавливаться частицы воды (см. схему).
Анионы SO42- - это сложные ионы, и в водных растворах они не окисляются, поэтому на аноде разряжаются молекулы воды:
 - К: К+, Н2О 2 Н2О + 2ē ® 2OH- + H2 – восстановление
- К: К+, Н2О 2 Н2О + 2ē ® 2OH- + H2 – восстановление
+А: SO42-, H2O 2 Н2О – 4ē ® 4 H+ + O2 – окисление
Раствор у катода подщелачивается (ионы ОН-), у анода – становится более кислым (ионы Н+).
Суммарное уравнение реакции:
K2SO4 + 4Н2О  2Н2+ 2 КОН + H2SO4 + O2
2Н2+ 2 КОН + H2SO4 + O2
KOH и H2SO4 образуются из ионов К+ и ОН-, Н+ и SO42-, находящихся в растворе.
Пример 2.Составьте электронные уравнения катодных и анодных процессов, протекающих при электролизе раствора CuCl2 с медным анодом.
Решение. Уравнение диссоциации соли имеет вид:
CuCl2 « Cu2+ + 2Cl-
К катоду подходят катионы Cu2+ и H2O;к аноду – ионы Cl- и H2O. Медный анод – растворимый, он принимает участие в электродной реакции. Потенциал меди составляет j0Cu/Cu2+ = 0,34 B, т.е. jCu/Cu2+>j 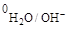 = –0,41 B. На катоде в соответствии с приведенной схемой будут восстанавливаться катионы Cu2+. В анодном процессе окисляется материал анода.
= –0,41 B. На катоде в соответствии с приведенной схемой будут восстанавливаться катионы Cu2+. В анодном процессе окисляется материал анода.
 - К: Cu2+, H2O Cu2+ + 2ē ® Cu
- К: Cu2+, H2O Cu2+ + 2ē ® Cu
+A: Cl-, H2O, Cu Cu - 2ē ® Cu2+
В ряде случаев путем изменения концентрации ионов соли можно изменить величину потенциала разряда иона и в соответствии с приведенной схемой уменьшить скорость разряда молекул воды.
Это необходимо учитывать при практическом использовании электролиза. Минимальный потенциал, при котором процесс электролиза становится возможным, называется потенциалом (напряжением) разложения Ер вещества. Его теоретическую величину находят как разность электродных потенциалов для процессов, происходящих на электродах:
Ер = jА - jк. (42)
Количественная характеристика процессов электролиза даётся законами Фарадея. Им можно дать следующую общую формулировку:
Масса электролита, подвергшаяся превращению при электролизе, а также массы образующихся на электродах веществ прямо пропорциональны количеству электричества, прошедшего через раствор или расплав электролита, и эквивалентным массам соответствующих веществ.
Закон Фарадея выражается следующим уравнением:
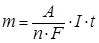 , (43)
, (43)
где А – атомная масса вещества;
n – заряд иона;
I – сила тока, А;
t – время пропускания тока, с.
Эквивалентная масса вещества Э = 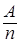 . Поскольку обычно имеются конкурирующие процессы, законы Фарадея нуждаются в поправках.
. Поскольку обычно имеются конкурирующие процессы, законы Фарадея нуждаются в поправках.
Отношение массы фактически выделившегося на электроде вещества mпр. к массе вещества, которая должна была выделиться в соответствии с законом Фарадея, называется выходом по току h:
h = 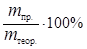 .(44)
.(44)
Пример 3Электрический ток силой 1А проходит в течение 1 часа через раствор ZnCl2 (электроды инертные). Определите количество выделившегося на катоде за указанное время цинка, если выход по току hравен 64%. Объясните, на какие процессы расходуется остальной ток.
Решение. Потенциал jZn0/Zn2+ = -0.76 B (см. табл. 5) и лежит в области –1,4 В <j < -0,41 В. Следовательно, на катоде будет идти совместный разряд Zn2+ и молекул воды:
Zn2+ + 2ē ® Zn
частично: 2H2O + 2ē ® 2OH- + H2
Для определения количества выделившегося на катоде цинка воспользуемся уравнением закона Фарадея:
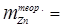
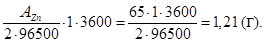
Выход по току h = 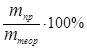 ;
;
отсюда
mпр = 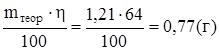 .
.
На получение цинка на катоде расходуется 64% всего прошедшего через электролит тока, остальной ток тратится на восстановление воды.
ЗАДАЧИ
201-205.Составьте электронные уравнения процессов, протекающих на катоде и аноде при электролизе расплава А, растворов Б и В (формулы веществ см. в табл.). В случае соединений А и Б использовались инертные электроды, а при электролизе В – растворимый анод. Масса твердого вещества, выделившегося на катоде при электролизе раствора Б при прохождении тока I, А в течение tчасов, составляет m, г. Вычислите выход по току.
Объясните, почему в ряде случаев не весь ток расходуется на выделение металла.
| № задачи | Соединения | Растворимый анод | I, A | t, ч | m, г | Ответы, % | ||
| А | Б | В | ||||||
| KCl | SnCl2 | ZnSO4 | Zn | 8,5 | 36,6 | |||
| FeCl2 | ZnSO4 | MgCl2 | Mg | 1,5 | 11,3 | |||
| NaOH | FeCl2 | MnSO4 | Mn | 0,5 | 4,2 | |||
| PbCl2 | Cu(NO3)2 | FeCl2 | Fe | 7,1 | ||||
| Ca(OH)2 | NiCl2 | AlCl3 | Al | 9,3 | 18,8 | 91,1 |
206-210.Составьте электронные уравнения процессов, протекающих на катоде и аноде при электролизе расплава А, растворов Б и В (формулы веществ см. в табл.). В случае соединений А и Б использовались инертные электроды, соединения В – растворимый анод.
Вычислите время, необходимое для получения электролизом 100 г металла из раствора Б при силе тока I, A, если выход по току h.
| № задачи | Соединения | Растворимый анод | I, A | h, % | Ответы, ч. | ||
| А | Б | В | |||||
| SnCl2 | Fe(NO3)2 | NiSO4 | Ni | 66,7 | |||
| Ni(OH)2 | CoCl2 | Pb(NO3)2 | Pb | 9,5 | |||
| MgCl2 | NiSO4 | ZnSO4 | Zn | 6,4 | 17,3 | ||
| ZnCl2 | AgNO3 | CuCl2 | Cu | 14,8 | 1,7 | ||
| CuBr2 | Cd(NO3)2 | AgNO3 | Ag | 8,7 | 6,4 |
211-215.Составьте электронные уравнения процессов, протекающих на катоде и аноде при электролизе расплава А, растворов Б и В (формулы веществ см. в табл.). В случае соединений А и Б использовались инертные электроды, соединения В – растворимый анод. Как изменится масса анода после пропускания тока силой I, A в течение времени t, ч через раствор В.
| № задачи | Соединения | Растворимый анод | I, A | t, ч | Ответы, г | ||
| А | Б | В | |||||
| NaJ | MgSO4 | ZnCl2 | Zn | 8,5 | 20,6 | ||
| CaCl2 | Cu(NO3)2 | FeCl2 | Fe | 31,3 | |||
| RbCl | AgNO3 | CuSO4 | Cu | 7,5 | 2,5 | 22,4 | |
| KOH | ZnCl2 | CoCl2 | Co | 3,7 | 4,1 | ||
| CuCl2 | NaNO3 | Pb(NO3)2 | Pb | 2,5 | 38,6 |
216-220.Составьте электронные уравнения процессов, протекающих на катоде и аноде при электролизе расплава А, растворов Б и В(формулы веществ см. в табл.). В случае соединений А и Б использовались инертные электроды, соединения В – растворимый анод.
Сколько граммов кислоты образуется возле анода при электролизе раствора Б, если на аноде выделилось 1,12 л кислорода, измеренного при н.у.?
Вычислите массу вещества, выделяющегося на катоде.
| № задачи | Соединения | Растворимый анод | Ответы, г | ||
| А | Б | В | |||
| KOH | Na2SO4 | NiCl2 | Ni | 4,9; 0,2 | |
| RbCl | Li2SO4 | Pb(NO3)2 | Pb | 4,9; 0,2 | |
| NaCl | Ni(NO3)2 | AgNO3 | Ag | 12,6; 5,9 | |
| AlCl3 | Fe2(SO4)3 | CuSO4 | Cu | 9,8; 3,7 | |
| NaJ | Cu(NO3)2 | ZnCl2 | Zn | 12,6; 6,4 |
