Сероводород, получение и свойства. Сероводородная кислота. 1-я и 2-я константы диссоциации. Роль в окислительно-восстановительных процессах. Соли сероводородной кислоты.
Получение:
1) прямой синтез из элементов, при температуре 600 °C;
2) воздействием на сульфиды натрия и железа соляной кислотой.



10. Серная кислота. Роль в окислительно-восстановительных процессах. Соли серной кислоты. Применение.

Оксид SO2 и серная кислота проявляют только окислительные свойства, что обусловлено высшей степенью окисления серы (+6)


11. Соединения серы в степени окисления +4. Роль в окислительно-восстановительных процессах (примеры). Применение.



12. Общая характеристика подгруппы азота.

Могут проявлять в соединениях степени окисления от −3 до +5.
13. Аммиак. Получение, химические свойства, применение.

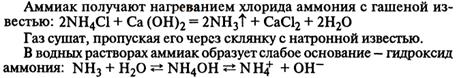

14. Азотная кислота. Химические свойства. Взаимодействие с металлами. Нитраты. Обнаружение.



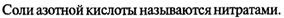
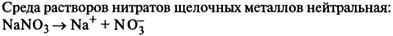

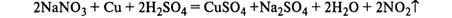

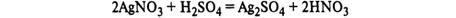
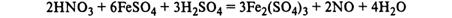
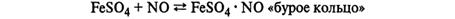

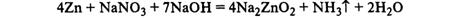
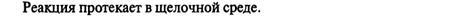
Обнаружение:
В колбу, соединенную с холодильником, конец которого опускают в колбу с водой, помещают исследуемую жидкость и медные опилки. Колбу нагревают на бане с минеральным маслом или на песчаной бане и жидкость выпаривают почти досуха. При достаточной концентрации азотной кислоты происходит восстановление ее медью в окись азота, которая с кислородом воздуха образует двуокись азота (оранжевые пары). Последняя, растворяясь в воде, дает азотную и азотистую кислоты, которые и обнаруживаются химическими реакциями:
3Сu + 2HNO3 = ЗСuО + 2NO + Н2O
3СuО + 6HNO3 = 3Cu(NO3)2 + 3H2O
2NO + O2 = 2NO2; 2NO2 + H2O = HNO2 + HNO3
15. Азотистая кислота и ее соли. Роль в окислительно-восстановительных процессах. Применение.
- HNO2. Соли азотистой кислоты (нитриты) получают восстановлением нитратов:
NaNO2+HCI = NaCI+HNO2.
-Азотистая кислота проявляет как окислительные, так и восстановительные свойства. При действии более сильных окислителей (Н2О2, KMnO4) окисляется в HNO3:
2HNO2 + 2HI → 2NO↑ + I2↓ + 2H2O;
5HNO2 + 2HMnO4 → 2Mn(NO3)2 + HNO3 + 3H2O;
HNO2 + Cl2 + H2O → HNO3 + 2HCl.



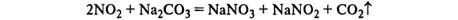
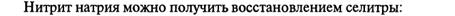
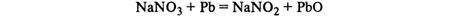

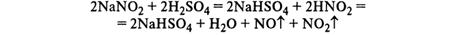


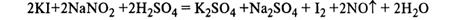
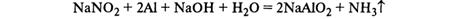

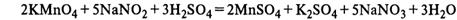
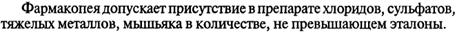
16. Биологическая роль азота и фосфора. Применение.

- Азот входит в состав хлорофилла, гемоглобина и др.

Фосфор присутствует в живых клетках в виде орто- и пирофосфорной кислот, входит в состав нуклеотидов, нуклеиновых кислот, фосфопротеидов, фосфолипидов, коферментов, ферментов. Кости человека состоят из гидроксилапатита 3Са3(РО4)3·Ca(OH)2. В состав зубной эмали входит фторапатит.
17. Мышьяк и его соединения. Обнаружение. Влияние на живой организм. Применение.




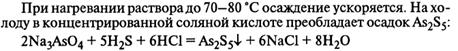

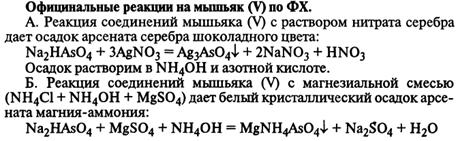
Из неорганических соединений мышьяка мышьяковистый ангидрид может применяться в медицине для приготовления пилюль и в зубоврачебной практике в виде пасты как некротизирующее лекарственное средство.
18. Общая характеристика элементов подгруппы углерода. Влияние на живой организм.
Применение.

- Круговорот углерода в природе включает биологический цикл, выделение СО2(=> фотосинтез).
Соединения кремния относительно нетоксичны. Но очень опасно вдыхание высокодисперсных частиц как силикатов, так и диоксида кремния, попадая в лёгкие, кристаллизующихся в них, а возникающие кристаллики разрушают лёгочную ткань и вызывают тяжёлую болезнь — силикоз.
Малые количества германия не оказывают физиологического действия на растения, но токсичны в больших количествах. Германий нетоксичен для плесневых грибков.
Олово входит в состав желудочного фермента гастрина.
Свинец и его соединения токсичны. Попадая в организм, свинец накапливается в костях, вызывая их разрушение.
Широкого применения в медицине свинец не получил из-за своей высокой токсичности. Используется только Pb(CH3COO)2·3H2O, или свинцовая вода, для примочек от ссадин
В настоящее время олово в медицине не используется.
19. Кислородсодержащие соединения углерода. Цианиды.





20. Кремний¸ строение атома. Важнейшие соединения, их свойства, применение.
-Si +14 )2 )8 )4.



