Опыт 2. Определение энтальпии процесса растворения соли в воде
Предлагается определить энтальпию растворения безводной соли нитрата аммония NH4NO3 и сравнить ответное значение с теоретическим, вычисленным по закону Гесса.
Процесс растворения безводной соли NH4NO3 с образованием катионов аммония и нитрат анионов сопровождается поглощением теплоты:
NH4NO3=NH4++NО3  -Q
-Q
Понижение температуры при растворении соли в воде может быть измерено опытным путем и использовано при расчете энтальпии растворения.
Теоретическое значение энтальпии растворения 1 моля безводной соли NH4NO3 равно: ∆Hºраств = - 6,4 ккал (26,7 кДж).
Последовательность проведения:
1) в сухой реакционный стакан калориметра налейте 50 мл дистиллированной воды, отмеренной измерительным цилиндром;
2) подождите в течение 2-3 мин. выравнивание температуры калориметра и окружающей среды; затем опустите в раствор термометр и, не касаясь дна стакана, измерьте температуру раствора с точностью до 0,1ºС, обозначив ее как tнач.;
2) на технохимических весах взвесьте на листке пергаментной бумаги 3 г нитрата аммония NH4NO, с точностью 0,01 г;
3) сложите листок в виде маленькой воронки, вставьте ее узким концом в свободное отверстие крышки калориметра, аккуратно высыпьте через нее навеску соли в стакан калориметра с водой;
4) осторожно перемешивая раствор мешалкой, следите за понижением температуры в течение 5-6 мин, в конце наблюдений запишите минимальную температуру, обозначив ее как tкон.
Обработка результатов и расчеты:
1) результаты наблюдений запишите в таблицу 4.2.
Таблица 4.2.
| Время от начала опыта, мин | 0,5 | 1,0 | 1,5 | 2,0 | 3,0 | 4,0 | 5,0 | 6,0 | |
| t, 0С |
2) рассчитайте тепловой эффект растворения безводной соли:
q = ∆t(mв + 0,18 mст) ·10-3 [ккал]
где mв – масса воды;
mст – масса реакционного стакана.
3) пересчитайте тепловой эффект на 1 моль безводной соли:
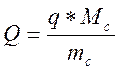 [ккал/моль], где
[ккал/моль], где
Мс – молярная масса соли, г/моль;
mс – навеска соли, г.
4) сравните полученное опытное значение со стандартным значением энтальпии растворения соли, учитывая, что Q= - ∆Ноп.раств..
5) вычислите относительную погрешность (в %) эксперимента:
 П = │ ∆Ннейтр.теор. -∆Ннейтр.эксп. . . 100 %│
П = │ ∆Ннейтр.теор. -∆Ннейтр.эксп. . . 100 %│
∆Ннейтр.теор.
Контрольные вопросы и задания
1. Что называется энтальпией образования вещества? Энтальпией разложения?
2. Какова зависимость между теплотой образования какого-либо химического соединения и теплотой его разложения?
3. Сформулируйте закон Гесса.
4. Как можно подсчитать тепловой эффект химической реакции, если известны энтальпии образования исходных веществ и продуктов реакции?
5. Вычислите тепловой эффект реакции полного сгорания ацетилена С2Н2 (стандартные теплоты образования см. приложение). Ответ: ΔН = -2600,0 кДж (-621,22 ккал).
6. Вычислите тепловой эффект одной из реакций, протекающих в доменной печи:
Fe2O3 + 3CO = 2Fe + 3CO2 + ΔH
(стандартные теплоты образования см. приложение).
Ответ: ΔН = -27,29 кДж (-6,53 ккал).
7. Что такое теплота гидратации? Теплота растворения?
8. Теплота растворения какой соли больше: безводной CuSO4 или CuSO4*5H2O? Ответ мотивируйте.
9. Одинакова ли теплота нейтрализации: а) 1 эквивалента, б) 1 моля соляной, азотной и серной кислот сильной щелочью?
10. При каких условиях тепловой эффект химической реакции численно равен изменению энтальпии?
11. Какие реакции называются экзотермическими:
1)Qp < 0; 2)ΔS > 0; 3)ΔS < 0; 4) ΔH > 0; 5) ΔH < 0?
12. При разложении 0,5 моль СО2 поглощается 196,7 кДж теплоты. Определить энтальпию образования СО2 (в кДж/моль).
13. Для какого вещества энтальпия образования равна нулю:
1)Н2О2; 2)H2SO4; 3)O2; 4)CaCO3; 5)O3; 6)N2; 7)Cl2
14. Из данных по окислению As2O3 кислородом и озоном вычислить изменение энтальпии при переходе 1 моля кислорода в озон:
As2O3 (к) + О2 (г) = As2O5 (к) ΔН1º=-270,8 кДж/моль;
3As2O3 (к) + 2О3 (г) = 3As2O5 (к) ΔН2º=-1096,2 кДж/моль.
Ответ: +96,4 кДж/моль.
Рекомендуемая литература
1. Глинка Н.Л. Задачи и упражнения по общей химии/ Под ред. В.А. Рабиновича и Х.М. Рубиной. – М.: Интеграл – Пресс, 2003. – с.66.
2. Морозов В.В., Тюльнин В.А., Юшина Т.И. Основы химической термодинамики. Учебное пособие по дисциплине «Термодинамика» для студентов, обучающихся по специальности «Обогащение полезных ископаемых». – М.: МГГУ. 2008. – с.42.
