Общая характеристика элементов IIА группы на основании строения их атомов и положения в таблице Д.И. Менделеева
Атомы элементов IIА группы имеют полностью заполненный s-подуровень внешнего электронного слоя и содержат на нем 2 электрона (у Ве отсутствует на внешнем слое d-подуровень):
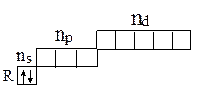
Как и в случае щелочных металлов, элементы IIА группы являются весьма реакционноспособными, с ярко выраженными металлическими свойствами, т.к. их валентные электроны тоже слабо удерживаются ядрами атомов.
Электроотрицательность и энергия ионизации у этих элементов сверху вниз закономерно уменьшается.
В химических реакциях элементы IIА группы всегда выступают в роли восстановителя, отдают атомам других элементов свои валентные электроны с внешнего слоя и в соединениях проявляют степень окисления +2.
По сравнению со щелочными металлами металлические свойства у элементов IIА группы выражены несколько слабее. Причем сверху вниз они возрастают и наиболее сильно проявляются у стронция и бария.
Бериллий, в отличие от всех остальных элементов группы, обладает амфотерными свойствами и поэтому в соединениях его химические связи имеют в значительной степени ковалентный характер.
Щелочноземельные металлы (Ca, Sr, Ba, Ra) образуют химические связи ионного типа.
Всем элементам IIА группы соответствуют простые вещества – металлы серебристо-белого цвета. В отличие от щелочных металлов они тверже и тяжелее: не режутся ножом, не плавают на поверхности воды, хотя тоже относятся к мягким и легким металлам. Металлическая связь в металлах IIА группы прочнее, поэтому все они имеют бόльшую температуру плавления, чем щелочные металлы (1284оС у бериллия и 710оС у бария).
ОБЩАЯ ХАРАТЕРИСТИКА ЭЛЕМЕНТОВ
I А ГРУППЫ
Нахождение в природе
Щелочными металлами называются элементы IА группы: литий Li, натрий Na, калий K, рубидий Rb, цезий Cs и франций Fr. Они относятся к семейству s-элементов и свое название получили из-за того, что их гидроксиды являются сильными щелочами.
Из щелочных металлов на Земле наиболее распространены натрий и калий, мольные доли которых в земной коре равны, соответственно, 2,0 и 1,1%. Содержание лития (0,02%), рубидия (0,004%) и цезия (0,00009%) уже значительно меньше, а франция – ничтожно мало.
Натрий и цезий в природе представлены только одним нуклидом каждый: 23Na и Cs133, литий и рубидий имеют по 2 устойчивых нуклида: 7Li (92,58%) и 6Li (7,42%); 85Rb (72,7%) и 87Rb (27,3%). Калий встречается в виде трех нуклидов: 39K (93,1%), 40K (0,01%) и 41K (6,88%) – но один из них 40K является радиоактивным (Т1/2 = 1,32 ∙ 109 лет).
Франций принадлежит к радиоактивным элементам и все его нуклиды являются короткоживущими. Период полураспада наиболее устойчивого из них 223Fr равен 21,8 минуты.
Щелочные металлы являются сильно реакционноспособными элементами и поэтому в природе существуют только в связанном виде. Наиболее распространенными минералами лития, натрия и калия являются: сподумен – LiAl(SiO3)2; каменная или поваренная соль (галит) – NaCl; сильвинит – KCl ∙ NaCl; сильвин – KCl; карналлит – KCl ∙ MgCl2 ∙ 6H2O; глауберовая соль или мирабилит – Na2SO4 ∙ 10H2O; кристаллическая сода – Na2CO3 ∙ 10H2O; бура – Na2B4O7 ∙ 10H2O; криолит – Na3[AlF6]; полевой шпат или ортоклаз – K2O ∙ Al2O3 ∙ 6SiO2; чилийская селитра – NaNO3.
Соединения рубидия и цезия встречаются обычно в виде примесей к минералам других щелочных металлов: лития, натрия или калия. Следовые количества франция всегда присутствуют в урановых рудах (≈ 4 ∙ 10-28 г на 1 г природного урана). Обычно Fr получают искусственным путем. Но вследствие малого периода полураспада его нуклидов сколько-нибудь заметных количеств франция накопить не удается, поэтому его свойства изучены недостаточно.
Большое количество растворимых соединений натрия находится в природных водах. Так, 1 литр морской воды содержит обычно более 10 г ионов Na+. Калий и натрий являются жизненно важными элементами и присутствуют в биологических жидкостях животных, растительных организмов и человека. Причем ионы Na+ преимущественно находятся в межклеточных жидкостях, а ионы K+ – внутри клеток.
