Примеры решения и оформления заданий к разделу 8
Пример 1.Медно - цинковый гальванический элемент
1. Схема Zn / ZnSO4 //CuSO4 /Cu
Условия стандартные, т.е. 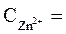 1 моль/л,
1 моль/л, 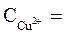 1 моль/л,
1 моль/л,
2. Электродные потенциалы
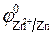 = - 0,76 В (при
= - 0,76 В (при 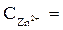 1 моль/л),
1 моль/л), 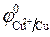 = + 0,34В (при
= + 0,34В (при 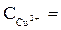 1 моль/л).
1 моль/л).
3. Направление движения электронов по внешний цепи - от цинкового электрода в медному, так как потенциал цинкового электрода меньше.
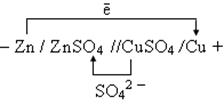
Расчет величины ЭДС.
ЭДС = φ0Ox - φ0Red = 0,34 - (- 0,76) = 1,1 В.
Пример 2 Гальванический элемент с водородным электродом.
1. Схема Zn / ZnSO4 // H2SO4 , Н2 / Pt.
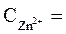 1 моль/л,
1 моль/л, 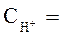 1 моль/л, Т = 298 К, P = 101,3 кПa .
1 моль/л, Т = 298 К, P = 101,3 кПa .
2. Электродные потенциалы
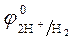 = 0 В ,
= 0 В , 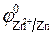 = - 0,76 В (при
= - 0,76 В (при 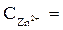 1 моль/л).
1 моль/л).
3. Направление движения электронов по внешней цепи - от цинкового электрода к водородному, так как потенциал цинкового электрода меньше.
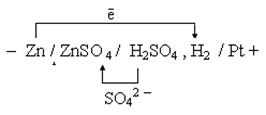
4. Уравнения электродных процессов.
Zn (-): Zn - 2ē = Zn 2+ - процесс окисления
Pt (+): 2Н ++ 2ē = Н 2 - процесс восстановления.
5. Суммарное уравнение:
Zn + 2Н + = Zn 2+ + Н 2
Zn + H2SO4 = ZnSO4 + Н 2
6. Расчет величины ЭДС.
ЭДС = φ0Ox - φ0Red = 0 - (- 0,76) = 0,76 В.
Пример 3. Концентрационный гальванический элемент.
Оба электрода из одного металла, но растворы солей, в которые погружены электроды, разной концентрации.
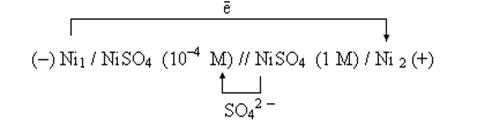
1. Схема гальванического элемента.
Ni / NiSO 4( 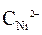 = 10-4 моль/л)// NiSO 4 (
= 10-4 моль/л)// NiSO 4 ( 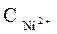 =1моль/л) / Ni
=1моль/л) / Ni
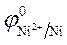 = -0,25 В.
= -0,25 В.
2. Вычисление электродных потенциалов по уравнению Нернста.
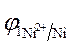 =
= 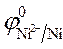 +
+ 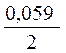 · lg
· lg 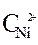 = -0,25 +
= -0,25 + 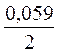 ·lg 10 -4 = -0,309 B.
·lg 10 -4 = -0,309 B.
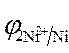 =
= 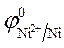 = - 0,25 B.
= - 0,25 B.
3.Направление движения электронов по внешней цепи от Ni1 электрода к Ni2, так как 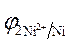 >
> 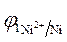 .
.
4. Уравнения электродных полуреакций.
Ni1 (-): Ni - 2ē = Ni 2+ - процесс окисления;
Ni2 (+): Ni2+ + 2ē = Ni -процесс восстановления.
Токообразующая реакция не имеет смысла.
5. Расчет величины ЭДС.
ЭДС = 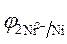 -
- 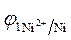 = - 0,25 - (- 0,309) = 0,059 В.
= - 0,25 - (- 0,309) = 0,059 В.
Пример 4. Гальванический элемент на основе окислительно-восстановительной реакции с инертным (С) электродом:
Zn / ZnSO4 // K2Cr2O7, Cr2(SO4)3, H2SO4 (C)
1. Сокращенная схема гальванического элемента
- Zn / Zn 2+ (1 M) // Cr2O72 -, Сr 3+, H+ (1 M) / C +
2. Используем значения стандартных электродных потенциалов, так как концентрации ионов в растворе равны 1моль/л.
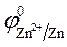 = - 0,76 B;
= - 0,76 B; 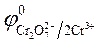 = 1,36 B.
= 1,36 B.
3. Направление движения электронов -от цинкового электрода к
угольному, так как 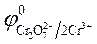 >
> 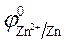 .
.
ē
 |
Zn / ZnSO4 // K2Cr2O7, Cr2(SO4)3, H2SO4 (C)
4. Уравнения электродных процессов.
Zn (-): Zn - 2ē = Zn 2+ - процесс окисления
С (+): Cr2O 7 2- + 6ē + 14Н+ = 2Cr 3+ + 7Н2О - процесс восстановления.
5. Суммарные уравнения.
3Zn + Cr2O72- + 14Н+ = 3Zn 2+ + 2Cr 3+ + 7Н2О
3Zn + K2Cr2O7+ 7H2SO4 = 3ZnSO4 + Cr2(SO4)3 + 7Н2О + K2SO4
6. Расчет величины ЭДС.
ЭДС = Е0Ox - Е0Red = 1,36- (- 0,76) = 2,12 В.
Тема №9: «Взаимодействие металлов с кислотами, водой и
растворами щелочей»
Задание 2. Используя потенциалы (см. таблицу на стр. 43), допишите уравнения реакций (по две для каждого варианта) и составьте к ним электронно-ионные схемы. Для реакций металлов с H2SO4 концентрированной и HNO3 значение потенциала окислителя примите равным более 1 В. Оцените практическую устойчивость металлов в данной среде.
| 1. Al + HCl H2SO4конц. + Сu | 16. Sn + H2O + O2 H2SO4конц. + Bi |
| 2. Al + H2O + O2 H2SO4конц. + Sn | 17. Co + NaOH + H2O + O2 H2SO4конц. + Co |
| 3.Al + H2O H2SO4конц. + Zn | 18. Sn + NaOH + H2O + O2 H2SO4конц. + Be |
| 4.Al + KOH + H2O HNO3разб. + Be | 19. Ni + H2O + O2 HNO3разб. + Pb |
| 5.Al + NaOH + H2O HNO3разб. + Cd | 20. Pb + KOH + H2O + O2 HNO3разб. + Cr |
| 6. Cu + H2O + O2 HNO3разб. + Mg | 21. Cr + KOH + H2O + O2 H2SO4конц., t° + Al |
| 7. Cu + NaOH + H2O + O2 HNO3конц. + Ba | 22. Pb + H2O + O2 HNO3разб. + Bi |
| 8. Fe + H2O + O2 HNO3конц. + Pb | 23. Bi + KOH + H2O + O2 HNO3конц., t° + Ni |
| 9. Cr + H2O HNO3разб. + Fe ® Fe3+ | 24. Cr + HCl H2SO4конц. + Mg |
| 10. Zn + H2O H2SO4конц., t° + Al ® | 25. Al + HCl Zn + NaOH + H2O |
| 11. Zn + NaOH + H2O H2SO4конц., t° + Ni ® | 26. Ti + H2SO4конц., t° Cd + KOH + H2O + O2 |
| 12. Zn + H2SO4разб. +O2 HNO3конц., t° + Fe ® Fe3+ | 27. Ti + HNO3разб. Cd + KOH + H2O |
| 13. Cr + H2O + O2 HNO3разб. +Cu | 28. Cd + HCl + O2 Be + H2SO4конц. |
| 14. Zn + NaOH + H2O + O2 H2SO4конц., t° + Fe ® Fe3+ | 29. Fe + KOH + H2O + O2 Ag + HNO3 конц. |
| 15. Cr + NaOH + H2O HNO3разб. + Sn | 30. Ni + KOH + H2O + O2 Mn + H2SO4конц. |
