Основные положения теории химического строения А.М. Бутлерова
1. Атомы в молекулах соединены друг с другом в определенной последовательности согласно их валентностям. Последовательность межатомных связей в молекуле называется ее химическим строением и отражается одной структурной формулой (формулой строения).
2. Химическое строение можно устанавливать химическими методами. (В настоящее время используются также современные физические методы).
3. Свойства веществ зависят от их химического строения.
4. По свойствам данного вещества можно определить строение его молекулы, а по строению молекулы - предвидеть свойства.
5. Атомы и группы атомов в молекуле оказывают взаимное влияние друг на друга.
Теория Бутлерова явилась научным фундаментом органической химии и способствовала быстрому ее развитию. Опираясь на положения теории, А.М. Бутлеров дал объяснение явлению изомерии, предсказал существование различных изомеров и впервые получил некоторые из них.
НОМЕНКЛАТУРА это система правил, позволяющих дать однозначное название каждому индивидуальному веществу.
В настоящее время общепринятой является систематическая номенклатура ИЮПАК (IUPAC – International Union of the Pure and Applied Chemistry – Международный союз теоретической и прикладной химии).
Наряду с систематическими названиями используются также тривиальные (обыденные) названия.
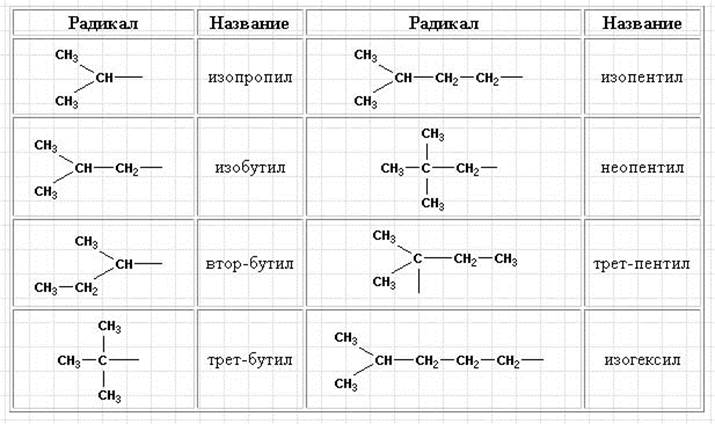
Для применения номенклатуры ИЮПАК необходимо знать названия и строение определенных фрагментов молекул – органических радикалов.
Органические соединения описывают с помощью молекулярных формул, представляющих собой линейную запись символов элементов в определенной последовательности с указанием числа атомов посредством численного индекса справа внизу. Структурная формула определяет последовательность атомов в молекуле с учетом структурной изомерии (скелетной, положения, цепь–цикл, функциональной).
Скелетная изомерия отражает строение углеводородной цепи (скелета):
| Линейный пентан СН3- СН2-СН2-СН2-СН3 1 2 3 4 5 | Изомер пентана СН3-СН-СН2-СН3  xxxxСН3 xxxxСН3 | Изомер пентана СН3   СН3 – С- СН3 СН3 СН3 – С- СН3 СН3 |
| пентан | 2-метилбутан | 2,2-диметилпропан |
Используя названия разветвленных радикалов, приведенных в таблице.
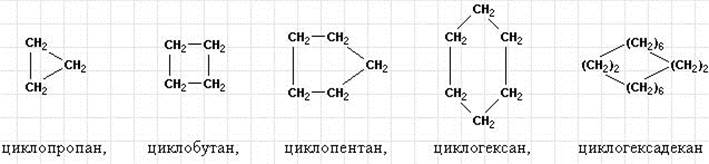
При замыкании углеводородной цепи в цикл с потерей двух атомов водорода образуются моноциклоалканы с общей формулой CnH2n. Циклизация начинается с C3, названия образуются от Cn с префиксом цикло:
Е н 20-22 10-12 5-5.5 0 ~ 2 ккал/моль
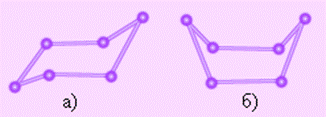
Неустойчивость плоских циклов вызвана значительной деформацией валентных углов. При сохранении тетраэдрических валентных углов вsp3гибридизации (С-С-Н = 109о28,) для циклогексана C6H12 возможны две устойчивые конформации: в форме кресла (а) и в форме ванны (б):
 |
========================================================
АЛКЕНЫ И АЛКИНЫ window.top.document.title = "12.2.2. Алкены и алкины";
Алкены (олефины) – ненасыщенные ациклические углеводороды с одной двойной связью, общая формула гомологического ряда CnH2n. Название образуется от углеводорода с наиболее длинной цепью, содержащей двойную связь, с добавлением суффикса -ен. Цифрой указывается положение двойной связи. В табл. 12.3 приведены первые четыре алкена, число изомеров которых увеличивается не только из-за изомерии скелета, но также изомерии положения двойной связи и геометрической изомерии (цис-транс). Названия одновалентных радикалов получают добавлением -ил к названию соответствующего углеводорода.
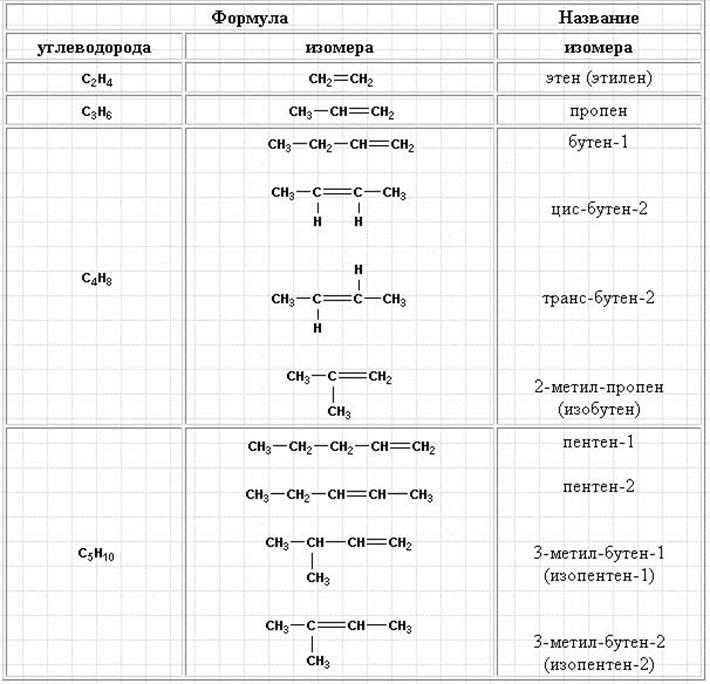
Алкены ациклического ряда CnH2n.
Полиалкены бывают трех типов:
1. С изолированными двойными связями
CH2=CH—CH2—CH2—CH=CH2
1,5-гексадиен
2. С сопряженными двойными связями
CH2=CH-CH=CH2
1,3-бутадиен (используется при получении полимеров)
В полиалкенах с сопряженными (чередующимися) двойными связями происходит делокализация π-электронов. Соединения с двойными связями легко полимеризуются.
Алкины (ацетиленовые углеводороды) содержат тройную связь. Общая формула алкина с одной тройной связью CnH2n–2. Название образуется от соответствующего углеводорода с добавлением суффикса -ин. В табл. 12.4 приведены первые пять алкинов.

АРЕНЫ window.top.document.title = "12.2.3. Арены";
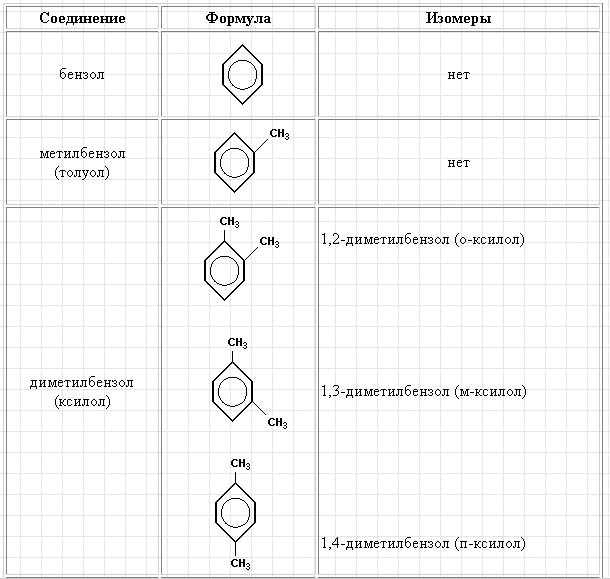
Арены (ароматические углеводороды) составляют многочисленный класс циклических углеводородов с делокализованными π-электронами. Эта делокализация обусловлена сопряженными двойными связями. Поэтому моноциклические арены изображаются шестиугольником с чередующимися простыми и двойными связями или шестиугольником с внутренней окружностью, символизирующей делокализацию π-электронов.
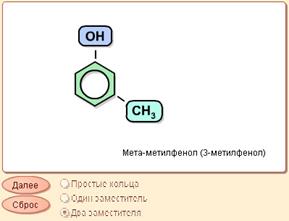 |
| Ароматические соединения. |

Моноциклические арены называют бензоидными. Одновалентные радикалы (арилы) называют
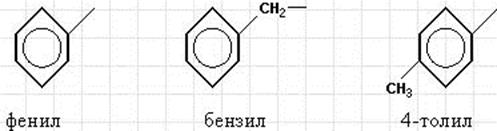
В таблице приведены некоторые моноциклические арены и их ди- и тризамещенные производные. Видно, что последние могут иметь не более трех изомеров.