Перманганатная окисляемость (ПО), или перманганатный индекс
Это самый древний метод определения окисляемости. Основан на окислении проб воды перманганатом калия в кислом растворе (метод Кубеля). На примере окисления фенола процесс можно изобразить схемой:
4 MnO4- + C6H6O + 4 H+ = 6 CO2 + 4 Mn2+ + 5 H2O
Итак, берут точно отмеренное количество КMnO4 и проводят окисление. Затем избыток перманганата связывают щавелевой кислотой:
2 MnO4- + 5 H2C2O4 + 6 H+ = Mn2+ + 10 CO2 + 8 H2O
Затем избыток щавелевой кислоты оттитровывают перманганатом калия до слабо-розовой окраски.
Этот метод используется главным образом при анализе питьевых и слабо загрязненных поверхностных вод с окисляемостью < 10мг О/л. С большей ошибкой можно определять перманганатную окисляемость при окисляемости < 100 мг О/л (при этом пробу предварительно разбавляют).
КMnO4 является более сильным окислителем, чем K2Cr2O7, но в более мягких условиях окисления перманганатом (меньше концентрация, время кипячения) многие органические вещества (спирты, кетоны, жирные кислоты, аминокислоты) совсем не подвергаются воздействию КMnO4 или окисляются в незначительной степени, Другие вещества: фенолы, малеиновая кислота практически полностью окисляются до CO2 и H2O. При наличии в пробе смеси подобных загрязнений, очевидно, невозможно по расходу перманганата сделать вывод о действительном содержании органических примесей.
Перманганатная окисляемость составляет 40 – 60% от истинной окисляемости органических веществ пробы. В последнее время перманганатная окисляемость все чаще уступает свое место определению более точного показателя ХПК.
Биохимическое потребление кислорода (БПК)
Рассмотренные методы позволяют определять общее содержание органических загрязнений вне зависимости от того, могут ли они окисляться микроорганизмами в природных условиях. Для оценки самоочищающей способности водного объекта нужно знать содержание в воде биохимически мягких веществ, т.е. веществ, легко разлагаемых микроорганизмами.
БПК – количество элементного кислорода в мг, требуемое для окисления находящихся в 1 л воды органических веществ в аэробных условиях в результате проходящих в воде биохимических процессов. Таким образом, БПК отражает суммарное содержание биохимически окисляющихся органических примесей. Поскольку органические примеси частично окисляются микроорганизмами до СО2 (с расходом кислорода), а частично расходуются на создание биомассы, БПК всегда меньше ХПК, даже если в воде присутствуют только легкоокисляемые органические вещества.
Рассчитаем удельную теоретическую ХПК (ТПКуд.) казеина:
С8H12O3N2 + 16 O = 8 CO2 + 2 NH3 + 3 H2O
М=184 г - 16×16 г
1 мг - ТПКуд.
ТПКуд. = 16×16/184 = 1,39 мг О/мг казеина
Рассчитаем удельную теоретическую БПК (с учетом размножения клеток микроорганизмов):
С8H12O3N2 + 6 O = С5H7O2N + NH3 + 3 CO2 + H2O
М=184 г - 6×16 г
1 мг - БПКуд.
БПКуд. = 6×16/184 = 0,522
Как видно из приведенного примера, ТПК(ХПК) > БПК.
На самом деле теоретически рассчитать БПК весьма не просто, т.к. доля органического вещества, идущего на образование клеток, зависит от многих факторов: от природы питательной среды, от возраста культуры клетки и др.
Существует два метода экспериментального определения БПК:
Метод разбавления заключается в том, что за процессом биохимического окисления органических веществ следят по убыли количества кислорода, введенного в склянку с пробой, в процессе инкубации этой пробы. Для этого измеряют содержание кислорода в пробе на 3,5,10 и т.д. день.
Название метода происходит из того, что исследуемую воду разбавляют чистой, не содержащей органических примесей, водой так, чтобы содержащегося в ней кислорода хватило для полного окисления всех органических веществ. Для этого используют результаты предварительного определения ХПК, условно принимая, что БПК » ½ ХПК. Так находят ориентировочное БПК (БПКориент.).
В воде содержится около 9 мг/л О2. Чтобы после инкубации можно было с достаточной точностью определить оставшийся кислород, его должно остаться не менее 4 ÷ 5 мг/л. Следовательно, БПКориент. делят на [9 – (4 ÷ 5)], т.е. на 5 или 4 и находят необходимую степень разбавления.
После разбавления воду разливают по склянкам и в одной из них определяют содержание О2. Остальные склянки инкубируют в темноте без доступа кислорода. Определив содержание О2 в определенный день, по убыли кислорода находят БПК. В зависимости от продолжительности инкубации проб при определении БПК различают БПК5 (биохимическое потребление кислорода за 5 суток) и БПКполн. (полное биохимическое потребление кислорода).
Определение БПК5 в поверхностных водах используется с целью оценки содержания биохимически окисляемых органических веществ, условий обитания гидробионтов и в качестве интегрального показателя загрязненности воды (см. табл.). Величины БПК5 используются также при контроле эффективности работы очистных сооружений.
Таблица.Величины БПК5 в водоемах с различной степенью загрязненности
| Степень загрязнения (классы водоемов) | БПК5, мг O2/дм3 |
| Очень чистые | 0,5-1,0 |
| Чистые | 1,1-1,9 |
| Умеренно загрязненные | 2,0-2,9 |
| Загрязненные | 3,0-3,9 |
| Грязные | 4,0-10,0 |
| Очень грязные | >10,0 |
Установлено, что при загрязнении водоемов бытовыми стокам с относительно постоянным составом и свойствам в конце пятого дня инкубации наступает 70%-ное окисление органических веществ, которые могут быть окислены биохимически. Поэтому раньше было оправдано определение БПК5 = 70% от БПКполн.. Сейчас, когда в водные объекты с промышленными сточными водами попадают вещества, трудно поддающиеся биохимическому окислению, или вещества, тормозящие биохимическое окисление органических примесей, определение БПК5 теряет смысл, т.к. иногда к 5 суткам процесс биохимического окисления только начинается (лаг-фаза может быть обусловлена постепенной адаптацией микроорганизмов к токсикантам). Поэтому службы мониторинга переходят от определения БПК5 к определению БПКполн..
Полным биохимическим потреблением кислорода (БПКполн.) считается количество кислорода, требуемое для окисления органических примесей до начала процессов нитрификации. Количество кислорода, расходуемое для окисления аммонийного азота до нитритов и нитратов, при определении БПК не учитывается. Для бытовых сточных вод (без существенной примеси производственных) определяют БПК20, считая, что эта величина близка к БПКполн.
Для более корректного определения БПКполн содержание кислорода в склянках с пробой определяют на 5, 7, 10 и т.д. день. Когда изменение содержания кислорода прекратится, определяют общий расход кислорода и величину БПКполн. Для предотвращения расходования кислорода на окисление аммонийного азота в этом случае в пробы добавляют инигибитор – подавитель нитрификации.
Второй метод заключается в том, что за процессом биохимического окисления наблюдают по убыли содержания органических веществ в пробе. Мерой содержания органических веществ служит ХПК, поэтому БПК определяют по разности между результатами определения ХПК до и после инкубации.
При биохимическом разложении органических веществ они частично окисляются до СО2 и Н2О, а частично превращаются в биомассу. Если количество органических веществ в начале биохимического окисления выразить тем количеством кислорода, которое требуется для полного его окисления, т.е. значением ХПК жидкой и твердой фаз в начале инкубации (ХПКн.ж.+ХПКн.т.), а содержание органических веществ в конце процесса (неокислившихся и превратившихся в биомассу) также представить в виде необходимого на их окисление кислорода (ХПКк.ж.+ХПКк.т.), то разность и будет равна БПК:
БПК =(ХПКн.ж.+ХПКн.т.) - (ХПКк.ж.+ХПКк.т.),
Для подавления нитрификации также вводят ингибитор (например, этилентиокарбамид).
Если в начале и в конце инкубации определять ХПК отдельно для жидкой и твердой фаз, то можно рассчитать следующие показатели, характеризующие способность исследуемой воды к самоочищению:
А = ХПКк.ж./ХПКн.ж. - выражает какая часть присутствующих в пробе органических веществ вообще не подвергается биохимическому окислению.
Б = 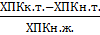 – характеризует количество биомассы, которая образуется в процессе биохимического окисления (прирост биомассы).
– характеризует количество биомассы, которая образуется в процессе биохимического окисления (прирост биомассы).
В = БПКt/ХПКн.ж. – характеризует относительное количество биохимически мягких веществ.
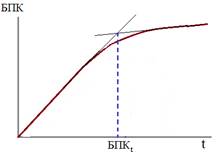 Время t выбирают по кривой БПК – время (см. рис.2), выделив наиболее круто поднимающийся участок.
Время t выбирают по кривой БПК – время (см. рис.2), выделив наиболее круто поднимающийся участок.
Г = 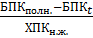 – характеризует относительное количество биохимически жестких органических веществ.
– характеризует относительное количество биохимически жестких органических веществ.
Сумма показателей А+Б+В+Г = 1.
Рис.2. Кинетика БПК.
Понятия «биохимически мягкий» и «биохимически жесткий» тесно связаны со скоростью биохимического окисления. Процесс биохимического окисления протекает в соответствии с закономерностями реакций I порядка, т.е. скорость окисления пропорциональна количеству оставшегося неокисленного вещества:
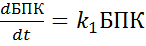 ;
; 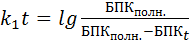 (1)
(1)
где k1 – константа скорости биохимического окисления.
Для чистых водоемов k1 » 0,05;
Для бытовых сточных вод и загрязненных ими водоемов k1 » 0,1;
Для сточных вод k1 ≥ 0,2.
Кроме ур. (1) k1 можно найти по результатам определения БПК в 2 последовательных срока кратных друг другу.
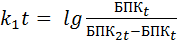 (формула кратных сроков). (2)
(формула кратных сроков). (2)
Зная k1 и БПК5 можно рассчитать БПКполн. и БПК в любой день, если кинетика БПК аппроксимируется уравнением I порядка:
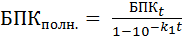 (из уравнения I порядка) (3)
(из уравнения I порядка) (3)
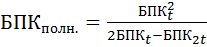 (формула кратных сроков). (4)
(формула кратных сроков). (4)
Время для окисления половины органических веществ называется периодом полураспада: 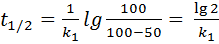 . (5)
. (5)
Для бытовых сточных вод оно равно 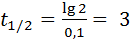 суток.
суток.
По формуле (1) можно доказать, что БПК5 для бытовых сточных вод и загрязненных ими природных вод составляет 70% от БПКполн..
С помощью константы скорости биохимического окисления k1 можно классифицировать органические вещества по способности к биохимическому окислению.
· К легкоокисляющимся (биохимически мягким) веществам относят формальдегид, низшие алифатические спирты, фенол, фурфурол и др., имеющие k1 = 1,4÷0,3 сут-1.
· Среднее положение занимают крезолы, нафтолы, ксиленолы, резорцин, пирокатехин, анионоактивные ПАВ и др. с k1 = 0,3÷0,05 сут-1.
· Медленно разрушаются "биологически жесткие" вещества, такие как гидрохинон, сульфонол, неионогенные ПАВ, гумифицированные отложения и др. с k1 = 0,03÷0,002 сут-1.
