Давление насыщенного пара растворителя
Важной характеристикой веществ, находящихся в жидком или твердом состоянии, является давление насыщенного пара. Давление насыщенного пара определяет при данной температуре равновесие между жидким (твердым) и газообразным состоянием вещества, которое устанавливается на границе раздела фаз.
В любом растворе концентрация молекул растворителя в поверхностном слое меньше, чем в чистом растворителе, и равновесие может быть достигнуто при меньшем давлении насыщенного пара. Под давлением насыщенного пара вещества понимают давление его паров в отсутствие других газов, в частности воздуха.
Первый закон Рауля:для разбавленных растворов относительное понижение давления насыщенного пара растворителя над раствором равно молярной доле растворенного вещества в растворе (рис. 4.7).
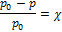
где р0 – давление насыщенного пара растворителя над чистым растворителем; р - давление насыщенного пара растворителя над раствором; χ – мольная доля растворенного вещества.
Следующая закономерность, характеризующая поведение растворов, относится к изменению температур кристаллизации и кипения при переходе от чистого растворителя к раствору.
При понижении температуры давление пара над раствором снижается, и когда оно становится равным давлению пара соответствующей твердой фазы, жидкость замерзает.Давление пара над раствором ниже давления пара над чистым растворителем, поэтому раствор будет замерзать при более низкой температуре, т.е. температура кристаллизации раствора всегда ниже температуры кристаллизации чистого растворителя (рис. 4.7).
Второй закон Рауля (криоскопический): понижение температуры замерзания разбавленного раствора пропорционально моляльной концентрации растворенного вещества.
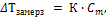
Сm – моляльность; К - криоскопическая константа, зависящая только от природы растворителя и не зависящая от природы растворенного вещества. Для воды К=1,86, для бензола К=5,07.
| B |
| C |
| B’ |
| C’ |
| A |
| A’ |
| p |
| T |
| p |
| P0 |
| Ткип |
| Пар |
| Жидкость |
| Твердое вещество |
| ΔТзам |
Рис. 4.7.Диаграмма состояния чистого растворителя и раствора
(ВА, АС – кривые кристаллизации и кипения растворителя,
B’A’, A’C’ – кривые кристаллизации и кипения раствора)
При повышении температуры давление пара над раствором растет, и когда оно достигает внешнего давления, наблюдается кипение раствора. Давление пара над раствором ниже давления пара над чистым растворителем, поэтому равенство давления пара и внешнего давления будет достигнуто при более высокой температуре, т.е. температура кипения раствора всегда выше, чем температура кипения чистого растворителя.
Второй закон Рауля (эбуллиоскопический): повышение температуры кипения разбавленного раствора пропорционально моляльной концентрации растворенного вещества.
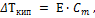
Cm – моляльность; Е - эбуллиоскопическая константа, зависящая только от природы растворителя и не зависящая от природы растворенного вещества. Для воды Е=0,52; для бензола Е=2,6.
Растворимость газов подчиняется закону Генри: при постоянной температуре растворимость газа в данной жидкости прямо пропорциональнадавлению этого газа над раствором.
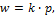
гдеw – массовая доля газа в насыщенном растворе, k – коэффициент пропорциональности, называемый константой Генри, p – парциальное давление.
Так как объем газа связан с его давлением, из закона Генри есть важное следствие: объем газа, растворяющегося при постоянной температуре в данном объеме жидкости, не зависит от его парциального давления.
Растворы электролитов
При изучении свойств водных растворов кислот, щелочей и солей, относящихся к электролитам, было установлено, что они не подчиняются законам Рауля и Вант-Гоффа. Они имеют большие, чем вычисленные по соответствующим формулам, понижение давления насыщенного пара растворителя над раствором, повышение температуры кипения и понижение температуры замерзания, осмотическое давление. Чтобы распространить на растворы электролитов расчетные формулы законов Рауля и Вант-Гоффа, в них был введен поправочный коэффициент i, называемый также изотоническим коэффициентом. Например, для расчета величины осмотического давления пользуются формулой 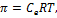 для растворов электролитов эта же формула выглядит следующим образом:
для растворов электролитов эта же формула выглядит следующим образом: 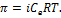 Коэффициент i определяется для каждого раствора экспериментальным путем, например, по понижению давления насыщенного пара, или по понижению температуры замерзания. Изотонический коэффициент показывает, во сколько раз экспериментальные величины больше теоретических, т.е. вычисленных по формулам для растворов неэлектролитов. В таблице приведены значения изотонических коэффициентов некоторых электролитов:
Коэффициент i определяется для каждого раствора экспериментальным путем, например, по понижению давления насыщенного пара, или по понижению температуры замерзания. Изотонический коэффициент показывает, во сколько раз экспериментальные величины больше теоретических, т.е. вычисленных по формулам для растворов неэлектролитов. В таблице приведены значения изотонических коэффициентов некоторых электролитов:
| Соль | Формула | Понижение температуры замерзания | 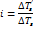 | |
| наблюдаемое (ΔTз’) | вычисленное по формуле Рауля, (ΔTз) | |||
| Хлорид калия | KCl | 0,673 | 0,372 | 1,81 |
| Нитрат калия | KNO3 | 0,664 | 0,372 | 1,78 |
| Хлорид магния | MgCl2 | 0,519 | 0,186 | 2,79 |
| Нитрат кальция | Ca(NO3)2 | 0,461 | 0,186 | 2,48 |
Для объяснения этих свойств шведский ученый С. Аррениус в 1887 г. Предложил теорию электролитической диссоциации.
Основные положения теории электролитической диссоциации:
1.Электролитическая диссоциация – распад молекул электролитов на ионы в среде растворителя.
2. Электролиты при растворении в воде распадаются (диссоциируют) на положительно и отрицательно заряженные ионы.
3. Под действием электрического тока, положительно заряженные ионы движутся к катоду, отрицательно заряженные – к аноду. Поэтому первые называют катионами, вторые – анионами.
4. Сумма положительных зарядов в растворе равна сумме отрицательных зарядов, поэтому раствор в целом электронейтрален.
5. Ионы представляются как точечные заряды, взаимодействия между которыми отсутствуют (подобны идеальным газовым смесям).
6. Диссоциация – процесс обратимый, поскольку одновременно протекают процесс распада молекул на ионы (диссоциация) и процесс соединения ионов в молекулы (ассоциация). Например, уравнение диссоциации молекулы электролита КА на катион К+ и анион Аˉ записывается так:
КА ↔ К+ + А-
Согласно теории Аррениуса, вследствиедиссоциации электролитов на ионы, с одной стороны, увеличивается общее число частиц в растворе, а следовательно, возрастают понижение давления пара и изменение температуры кипения и замерзания, с другой стороны – ионы обусловливают способность раствора проводить электрический ток.
Физический смысл изотонического коэффициента iсостоит в увеличении общего числа частиц в растворе за счет диссоциации растворенного вещества на ионы.
Однако теория Аррениуса рассматривала ионы как свободные не зависимые от молекул растворителя частицы, не учитывала всей сложности явлений в растворах. Теории Аррениуса противостояла химическая, или гидратная, теория растворов Менделеева, в основе которой лежало представление о взаимодействии растворенного вещества с растворителем. В преодолении кажущегося противоречия обеих теорий большая заслуга принадлежит русскому ученому И. А. Каблукову, впервые высказавшему предположение о гидратации ионов. Развитие этой идеи привело в дальнейшем к объединению теории Аррениуса и Менделеева.
В создании современной физико-химической теории растворов большую роль сыграли работы русских ученых Д. И. Менделеева, И. А. Каблукова, Д.П. Коновалова, В. А. Кистяковского и др.
По современным представлениямпричиной электролитической диссоциации является физико-химическое взаимодействие между полярными молекулами и ионами растворяемого вещества и полярными молекулами растворителя (сольватация), приводящее к образованию соединений сольватов (комплексов). В случае если вода – растворитель, говорят о гидратации и образовании гидратов.
В зависимости от состояния растворенного вещества до растворения выделяют два класса растворов электролитов - растворы ионофоров и растворы ионогенов. Ионофоры в чистом состоянии существуют в виде ионных кристаллов (например, галогенидыщелочных металлов). В сильнополярных растворителях (например, в воде) ионофоры, как правило, диссоциируют полностью и составляют растворы сильных электролитов. В слабополярных растворителях (например, в уксусной кислоте) они образуют растворы слабых электролитов. Ионогены до растворения состоят из молекул, они являются потенциальными электролитами, электролитическая диссоциация проходит, как правило, в две стадии и обычно не полностью (хлорная кислота в уксусной кислоте).
Растворители для растворовэлектролитов- как правило, полярные жидкости (чистые или смешанные). Чем больше диэлектрическая проницаемость ε растворителя, тем значительнее ослабляется сильное электростатическое притяжение противоположно заряженных ионов, что способствует возникновению в растворе ионов. Интенсивное взаимодействие последних с молекулами растворителя приводит к связыванию ионов с молекулами растворителя. Важна также способность молекул растворителя выступать в качестве доноров или акцепторов протонов или электронов. В зависимости от этих двух свойств различают четыре группы растворителей:
1) протонные растворители (вода, спирты, карбоновые кислоты и др.), которые являются хорошими донорамипротона (иона Н+)и обладают высокой диэлектрической проницаемостью (ε > 15);
2) апротонные полярные растворители (некоторые апротонные амиды, кетоны, сульфоксиды и др.), обладающие высокой диэлектрической проницаемостью, но не обладающие донорно-акцепторными свойствами в отношении протона;
3) электронодонорные растворители (например, эфиры);
4) неполярные растворители (сероуглерод, углеводороды), которые обладают низкой диэлектрической проницаемостью (ε < 15) и не обладают донорно-акцепторными свойствами ни по отношению к протону, ни по отношению к электрону.
Находящиеся в растворахэлектролитовионы могут существовать в виде свободных сольватированных ионов или в виде ассоциатов-контактных или сольватно разделенных ионных пар, тройников и т.д. Поскольку ионные пары не проводят электрический ток, содержание свободных ионов в растворахэлектролитов определяется по его электрической проводимости, в то время как общее число ионов (свободных и ассоциированных) можно определить, например, спектрофотометрическими методами.
Взаимодействие между молекулами и ионами растворяемого вещества и молекулами воды может состоять из нескольких процессов, протекающих последовательно или одновременно: молекулярной диссоциации, образования сольватов, ионизации и электролитической диссоциации. В зависимости от типа растворяющихся веществ число стадий может изменяться. Так, в случае ионных кристаллов стадии образования гидратов и электролитическая диссоциация совмещены.
В случае ассоциированных веществ первой стадией является молекулярная диссоциация растворенного вещества. Процесс молекулярной диссоциации происходит вследствие химического взаимодействия между молекулами растворяемого вещества КА, (m+n) молекулами воды с образованием гидратированной молекулы КА(m+n)Н2О:
КА + (m+n)Н2О ↔ КА(m+n)·Н2О. (а)
Образующийся гидрат диссоциирует на гидратированные ионы (стадия электролитической диссоциации):
КА(m+n)·Н2О ↔ К+·mН2О + А–·nН2О. (б)
Процесс гидратации может остановиться на любой стадии. Если процесс гидратации останавливается на стадии (а), то система представляет собой раствор неэлектролита. Она характеризуется отсутствием ионов в растворе и соответственно не обладает ионной электрической проводимостью. Если процесс гидратации протекает до стадии (б), то система является раствором электролита, т.е. имеет место электролитическая диссоциация с образованием ионов. Уравнение электролитической диссоциации можно записать, опустив промежуточные стадии, указав лишь начальные и конечные продукты реакции:
КА + (m+n)Н2О ↔ К+·mН2О + А–·nН2О.
Особенностью гидратов (сольватов) как химических соединений является то, что коэффициенты n и m меняются с изменением концентрации, температуры и других параметров раствора. Поэтому приведенные формулы гидратов (сольватов) не отражают их истинного стехиометрического состава.
Однако часто в подобных уравнениях опускают молекулы растворителя, записывая их в таком виде:
КА ↔ К+ + А–.
Электролитическая диссоциация протекает самопроизвольно (∆G < 0). Понижение изобарно-изотермического потенциала обусловлено образованием гидратированных (сольватированных) ионов. Энергии гидратации (сольватации) достаточно для разрушения химических связей в молекулах или ионных кристаллах.
