Практическое применение электрической проводимости. 1 страница
1. Определение fэ сильных электролитов:
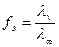
2. Определение константы и степени диссоциации слабых электролитов:
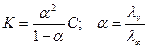
В не слишком разбавленных растворах величина a у слабых кислот и оснований очень мала, и можно считать, что 1 - a » 1. Тогда получаем:
K = a2 C и a = 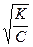
Это уравнение дает простой способ подсчета степени электролитической диссоциации слабого электролита в растворе данной концентрации, когда константа К известна.
 3. Определение солесодержания в растворе электролита:
3. Определение солесодержания в растворе электролита:
 1000 = Сi (lk + la)
1000 = Сi (lk + la)
Сi = 1000 / 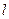 k +
k + 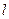 a
a
4. Определение растворимости труднорастворимых солей.
По закону действующих масс для бинарного электролита можно записать:
[K+] [A-] = K [KA] = ПР,
где ПР – произведение растворимости. ПР = const при Т = const
Если соединение диссоциирует нацело, то
 [K+] = [A-] = ÖПР = С (моль/л)
[K+] = [A-] = ÖПР = С (моль/л)
ПР и С определяют из данных насыщенного раствора электролита.
Пример: AgCl

 Сначала измеряют дистиллированной воды ( =1,5×10-6См/м).
Сначала измеряют дистиллированной воды ( =1,5×10-6См/м).
 насыщенного раствора AgCl равна 2,75×10-6См/м.
насыщенного раствора AgCl равна 2,75×10-6См/м.
 Следовательно:
Следовательно:
(AgCl) = 2,75×10-6 - 1,5×10-6 = 1,25×10-6 См/м
Электролитические подвижности ионов Ag+ и Cl- равны соответственно 53,8 и 65,2, а молярная электрическая проводимость при бесконечном разбавлении:
l¥ = 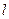 Ag +
Ag + 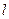 Cl = 53,5 + 65,2 = 119,0 См/м2
Cl = 53,5 + 65,2 = 119,0 См/м2
 Так как
Так как
l¥ = V;
то определяем V, содержащий 1 моль AgCl:
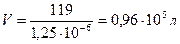
Число молей в 1 литре равно:
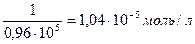
Биологическое значение.
Явления электрической проводимости в тканях растительных и животных организмов имеют большое физиологическое значение.
Электрическая проводимость разных тканей и биологических жидкостей неодинакова: наибольшей электрической проводимостью обладают спинномозговая жидкость, лимфа, желчь, кровь; хорошо проводят ток также мышцы, подкожная клетчатка, серое вещество головного мозга. Значительно ниже электрическая проводимость легких, сердца, печени. Очень низка она у жировой ткани, нервной, костной. Хуже всего проводит электрический ток кожа (роговой слой). Сухой эпидермис почти не обладает электропроводностью.
Жидкость межклеточных пространств гораздо лучше проводит ток, чем клетки, оболочки которых оказываются существенным препятствием при движении многих ионов. Измерение электрической проводимости широко применяется при изучении изменения проницаемости в живых клетках. Возрастание электрической проводимости клетки означает, что ионы проходят через клетку с большей легкостью. При малых изменениях электрической проводимости процесс обратим, но если изменение электрической проводимости слишком увеличивается в сторону возрастания или убывания, то процесс становится необратимым и наступает смерть организма. По величине электрической проводимости биологических жидкостей можно определить их сопротивление. Электрическое сопротивление нормальных водорослей почти в 10 раз больше сопротивления морской воды, тогда как мертвая ткань имеет сопротивление почти равное сопротивлению морской воды. Вообще Са++ понижает проницаемость, а Mg++, Na+, K+ ее увеличивают.
Изучение электрической проводимости растворов называют кондуктометрией. Кондуктометрические методы анализа основаны на зависимости между электрической проводимостью растворов и концентрацией ионов в растворе.
Кондуктометрическое титрование – метод анализа, основанный на определении содержания вещества по излому кривой титрования. Кривую строят по измерениям удельной электрической проводимости анализируемого раствора, изменяющейся в результате химических реакций в процессе титрования.
Кондуктометрические методы по сравнению с другими методами анализа имеют некоторые преимущества. Они дают возможность:
- без больших затруднений проводить определения не только в прозрачных, но и в окрашенных и мутных растворах, а также в присутствии окислителей и восстановителей, ограничивающих применение органических индикаторов в других методах;
- осуществлять определения разнообразных неорганических и органических индивидуальных соединений;
- анализировать не только сравнительно концентрированные растворы, но и разбавленные до 10-4 М;
- проводить исследования не только водных, но и не водных и смешанных водно-органических растворов;
- сравнительно легко осуществлять автоматизацию процессов титрования;
- широко использовать разнообразные типы реакций (нейтрализации, осаждения, комплексообразования, окисления-восстановления, замещения, конденсации, омыления и т.п.), сопровождающихся изменением электрической проводимости анализируемых растворов;
- во многих случаях избежать предварительного отделения примесей, обычно мешающих определению другими методами;
- просто и точно определять конечную точку титрования по пересечению двух прямых и соответственно вычислять точку эквивалентности;
- использовать переменный ток низкой частоты и постоянный ток;
- производить дифференцированное титрование смесей электролитов, что невозможно осуществить другими методами.
Кондуктометрические методы анализа применяются в промышленности для осуществления непрерывного химико-аналитического контроля производства, определения концентрации солевых растворов, содержание солей в минеральной, морской и речной воде, для контроля процесса очистки и качества воды, оценки загрязненности сточных вод, для определения следов воды в неводных растворителях, газах, твердых солях, целлюлозе, бумаге, зерне, для определения влажности зерна и почвы.
Кондуктометрические методы также применяются для анализа окружающей среды, качественного определения различных газов (СО2, СО, О2, NH3, SO2, H2S и др.), содержание вредных примесей в воздухе, воде, пищевых продуктов, для контроля качество молока, вин, напитков, фруктовых соков.
Кондуктометрическое титрование используется для определения индивидуальных сильных, слабых и очень слабых неорганических и органических карбоновых кислот, амино-, галогено- и оксикислот, фенолов и их производных, фармацевтических препаратов, дигуанидина, гуминовых кислот, аминов, четвертичных аммониевых оснований и т.д.
Кондуктометрическое титрование применяется также для анализа многокомпонентных смесей, кислот, оснований, солей, образованных сильными кислотами (основаниями) и слабыми основаниями (кислотами), разнообразных катионов и анионов, окислителей и восстановителей, комплексующихся агентов, смесей минеральных, монокарбоновых и поликарбоновых кислот, смесей оснований и солей слабых кислот, смесей кислот и солей слабых оснований и т.д.
Вопросы для самоконтроля:
1. Понятие электролита. Сильные и слабые электролиты. Понятие степени и константы электролитической диссоциации.
2. Удельная электрическая проводимость растворов, единицы измерения. График зависимости удельной электрической проводимости от концентрации для сильных и слабых электролитов.
3. Основное уравнение электропроводности для сильных и слабых электролитов.
4. Молярная электрическая проводимость. Единицы измерения. График зависимости молярной электрической проводимости от разбавления для сильных и слабых электролитов.
5. Сформулируйте закон независимого перемещения ионов Кольрауша.
6. Закон разведения Оствальда.
7. Метод кондуктометрического титрования, его теоретические основы и преимущества.
8. Как методом электропроводности можно определить константу и степень электролитической диссоциации слабого электролита?
Экспериментальная часть:
Задание 1. Определение электрической проводимости раствора слабого электролита.
Для измерения удельной электрической проводимости раствора электролита используют кондуктометр марки «МАРК-II». Перед началом работы необходимо провести подготовку прибора к работе:
1. Переключатель питания «ВКЛ-ВЫКЛ» перевести в положение «ВКЛ».
2. Переключатель «ПРОВОДИМОСТЬ-ТЕМПЕРАТУРА» установить в положение «ТЕМПЕРАТУРА» - на индикаторе должно высветиться значение температуры. Когда показания будут стабильны – прибор готов к работе. После этого переключатель «ПРОВОДИМОСТЬ-ТЕМПЕРАТУРА» установить в положение «ПРОВОДИМОСТЬ».
3. Переключателем «ДИАПАЗОНЫ ПРОВОДИМОСТИ 1-2» (передняя панель) выставить диапазон в положение «2».
4. Переключателем «РАСШИРИТЕЛЬ ДИАПАЗОНОВ» на торце прибора выставить диапазон в положение «2000 мкСм/см» (рычажок в положении – вниз).
Для выполнения работы получить номерной раствор у преподавателя. В пластмассовый стаканчик с помощью цилиндра поместить 20 мл исследуемого раствора и поместить в ячейку прибора (раствор всасывают в ячейку с помощью резиновой трубочки со стеклянным наконечником).
Все результаты записать в таблицу 11.
Сливают раствор из ячейки в сухой стеклянный стаканчик емкостью 150мл. Разбавляют раствор в 2 раза, добавляя равное количество дистиллированной воды (20 мл), хорошо перемешивают, отбирают цилиндром аликвотную часть (20 мл) в пластмассовый стаканчик и помещают ее в ячейку прибора. Измеряют удельную электрическую проводимость раствора.
Сливают раствор из ячейки в стеклянный стаканчик, где находится разбавленный исследуемый раствор кислоты и разбавляют его еще в 2 раза, добавляя объем дистиллированной воды, равный сумме объемов исходной кислоты и уже добавленной ранее воды, т.е. 40 мл. Раствор хорошо перемешивают, аликвотную часть (20 мл) помещают в ячейку прибора и измеряют его удельную электрическую проводимость. Результаты записывают в таблицу 11. По окончании работы с раствором ячейку промывают несколько раз дистиллированной водой.
Таблица 11
Результаты измерения электрической проводимости растворов
электролитов
| Раствор | С |  | lv | a | K | fэ |
| Исследуемый раствор кислоты, N | C C/2 C/4 | - | ||||
| Н2О водопроводная | - | - | - | - | ||
| KCl | 0,1 н | - | - |
Вычисления:
Для каждого разбавления рассчитать:
1.  Эквивалентную электропроводность
Эквивалентную электропроводность
λv = 1000
 С
С 
2. Степень электролитической диссоциации
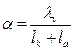
3. Константу электролитической диссоциации
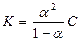
 Сделать выводы об изменении a, К, и lv растворов слабого электролита с изменением концентрации.
Сделать выводы об изменении a, К, и lv растворов слабого электролита с изменением концентрации.
Задание 2. Определение солесодержания водопроводной воды по измеренному значению удельной электрической проводимости.
В ячейку поместить 20 мл водопроводной воды. Измерить удельную электрическую проводимость воды. Для приблизительной оценки солесодержания следует воспользоваться таблицей 12 перевода удельной электрической проводимости в величину эквивалентного содержания NaCl.
Пример:
Измеренное значение удельной электрической проводимости водопроводной воды 195 мкСм/см. По таблице находим величину эквивалентного содержания NaCl – 93 мг/дм3.
Задание 3. Определение коэффициента электропроводности сильного электролита (0,1н раствора КСl).
Ячейку для определения электрической проводимости промыть несколько раз дистиллированной водой. Поместить 20мл 0,1н КСl в ячейку и определить удельную электрическую проводимость раствора. По окончании работы ячейку хорошо промыть и заполнить дистиллированной водой.
 Вычисления:
Вычисления:
