Индукционный и мезомерный эффекты. Их влияние на химические свойства и направления реакций. Сопряжённые системы. Ароматичность правило Хюккеля.
Вопрос 1
Предмет орг. и биоорганической химии, её значение, Основные положения теории Бутлерова.Органическая химия - это раздел химической науки, в котором изучаются соединения углерода - их строение, свойства, способы получения и практического использования.
Соединения, в состав которых входит углерод, называются органическими. Кроме углерода, они почти всегда содержат водород, довольно часто - кислород, азот и галогены, реже - фосфор, серу и другие элементы. Однако сам углерод и некоторые простейшие его соединения, такие как оксид углерода (II), оксид углерода (IV), угольная кислота, карбонаты, карбиды и т.п., по характеру свойств относятся к неорганическим соединениям. Поэтому часто используется и другое определение: Органические соединения - это углеводороды (соединения углерода с водородом) и их производные. Благодаря особым свойствам элемента углерода, органические соединения очень многочисленны. Сейчас известно свыше 10 миллионов синтетических и природных органических веществ, и их число постоянно возрастает. Первоначально Орг.Химия изучала природные соединения, в-ва выделяемые из растительных и животных организмов, затем всё больше преобретал смысл органический синтез.Органическая химия имеет исключительно важное познавательное и народнохозяйственное значение. Природные органические вещества и их превращения лежат в основе явлений Жизни. Поэтому органическая химия является химическим фундаментом биологической химии и молекулярной биологии - наук, изучающих процессы, происходящие в клетках организмов на молекулярном уровне. Исследования в этой области позволяют глубже понять суть явлений живой природы. Множество синтетических органических соединений производится промышленностью для использования в самых разных отраслях человеческой деятельности.
Это - нефтепродукты, горючее для различных двигателей, полимерные материалы (каучуки, пластмассы, волокна, пленки, лаки, клеи и т.д.), поверхностно-активные вещества, красители, средства защиты растений, лекарственные препараты, вкусовые и парфюмерные вещества и т.п. Без знания основ органической химии современный человек не способен экологически грамотно использовать все эти продукты цивилизации. Сырьевыми источниками органических соединений служат: нефть и природный газ, каменный и бурый уголь, горючие сланцы торф, продукты сельского и лесного хозяйства. Биорг. химия изучает вещества, лежащие в основе процессов жизнедеятельности, с непосредственными связями с познаванием биологических функций. Основными объектами являются биополимеры и биорегуляторы. Биополимеры- это высокомолекулярные природные соединения , явл. структурной основой всех живых организмов и играющие роль в процессах жизнедеятельности .Биорегуляторы- это соединения, которые химически регулируют обмен веществ, гормонов, синтетические биохимические соединения. В био.химии были установлены структуры многих сложных биологически активных веществ, включая и биополимеры, белки, нуклеиновые кислоты, полисахариды. И активно развивающийся органический синтез открывает путь к созданию уникальных биологически значимых структур. К середине XIX в. появляются первые теории: Теория радикалов, теория типов (Ш. Жерар, 1851) понятия валентности( Кекуле, Купер 1857-1858) и химической связи. Решающий вклад в создание теории строения орг. соединений (1861) принадлежит великому русскому химику Бутлерову... Свойства соединений зависят не только от природы и числа входящих атомов, но и от химического строения молекул, под которым понимается определённая последовательность связей между атомами. Основные положения Бутлеров сформулировал в 1858-61
1. Атомы в молекулах соединены друг с другом в определенной последовательности согласно их валентностям. Последовательность межатомных связей в молекуле называется ее химическим строением и отражается одной структурной формулой (формулой строения).
2. Химическое строение можно устанавливать химическими методами. (В настоящее время используются также современные физические методы).
3. Свойства веществ зависят от их химического строения.
4. По свойствам данного вещества можно определить строение его молекулы, а по строению молекулы - предвидеть свойства.
5. Атомы и группы атомов в молекуле оказывают взаимное влияние друг на друга. Теория Бутлерова явилась научным фундаментом органической химии и способствовала быстрому ее развитию. Опираясь на положения теории, А.М. Бутлеров дал объяснение явлению изомерии, предсказал существование различных изомеров и впервые получил некоторые из них.
Вопрос 2
Классификация органических соединений и органических реакций (по направлению и характеру реагирующих частиц)  Органические соединения Критерием деления соединений на органические и неорганические служит их элементный состав. К органическим соединениям относятся химические вещества, содержащие в своем составе углерод, например:В основу современной классификации орг. соединений положено 2 признака.:1 Строение углеродного скелета молекулы.2 наличие в молекуде функциональных групп.
Органические соединения Критерием деления соединений на органические и неорганические служит их элементный состав. К органическим соединениям относятся химические вещества, содержащие в своем составе углерод, например:В основу современной классификации орг. соединений положено 2 признака.:1 Строение углеродного скелета молекулы.2 наличие в молекуде функциональных групп.
Классификация соединений по строению углеродной цепи 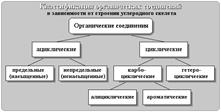 В зависимости от строения углеродной цепи органические соединения делят на ациклические и циклические. Ациклические соединения - соединения с открытой (незамкнутой) углеродной цепью. Эти соединения называются также алифатическими.
В зависимости от строения углеродной цепи органические соединения делят на ациклические и циклические. Ациклические соединения - соединения с открытой (незамкнутой) углеродной цепью. Эти соединения называются также алифатическими. 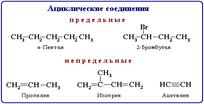 Среди ациклических соединений различают предельные (насыщенные), содержащие в скелете только одинарные связи C-C и непредельные (ненасыщенные), включающие кратные связи C=C и C
Среди ациклических соединений различают предельные (насыщенные), содержащие в скелете только одинарные связи C-C и непредельные (ненасыщенные), включающие кратные связи C=C и C  C. Ациклические соединения подразделяют также на соединения с неразветвленной и разветвленной цепью. В этом случае учитывается число связей атома углерода с другими углеродными атомами. Циклические соединения - соединения с замкнутой углеродной цепью.
C. Ациклические соединения подразделяют также на соединения с неразветвленной и разветвленной цепью. В этом случае учитывается число связей атома углерода с другими углеродными атомами. Циклические соединения - соединения с замкнутой углеродной цепью. 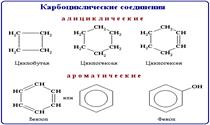 В зависимости от природы атомов, составляющих цикл, различают карбоциклические и гетероциклические соединения.
В зависимости от природы атомов, составляющих цикл, различают карбоциклические и гетероциклические соединения.
Карбоциклические соединения содержат в цикле только атомы углерода. Они делятся на две существенно различающихся по химическим свойствам группы: алифатические циклические - сокращенно алициклические - и ароматические соединения. 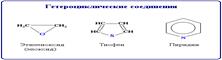 Гетероциклические соединения содержат в цикле, кроме атомов углерода, один или несколько атомов других элементов - гетероатомов (от греч. heteros - другой, иной) - кислород, азот, серу и др. Классификация соединений по функциональным группам Соединения, в состав которых входят только углерод и водород, называются углеводородами. Другие, более многочисленные, органические соединения можно рассматривать как производные углеводородов, которые образуются при введении в углеводороды функциональных групп, содержащих другие элементы. В зависимости от природы функциональных групп органические соединения делят на классы. Некоторые наиболее характерные функциональные группы и соответствующие им классы соединений приведены в таблице:
Гетероциклические соединения содержат в цикле, кроме атомов углерода, один или несколько атомов других элементов - гетероатомов (от греч. heteros - другой, иной) - кислород, азот, серу и др. Классификация соединений по функциональным группам Соединения, в состав которых входят только углерод и водород, называются углеводородами. Другие, более многочисленные, органические соединения можно рассматривать как производные углеводородов, которые образуются при введении в углеводороды функциональных групп, содержащих другие элементы. В зависимости от природы функциональных групп органические соединения делят на классы. Некоторые наиболее характерные функциональные группы и соответствующие им классы соединений приведены в таблице:
 углеводороды - R-H; Галогенопроизводные R-Hal; спирты- R-OH; Фенолы- Ar-OH; Простые эфиры R-O-R; Тиолы R-SH; Амины(первичные) R-NH2; Нитросоединения R-NO2; Альдегиды R-CH=O ,Кетоны R-CO-R,Карбоновые кислоты R-COOH , Сульфонновые кислоты R-SO3H. В состав молекул органических соединений могут входить две или более одинаковых или различных функциональных групп.
углеводороды - R-H; Галогенопроизводные R-Hal; спирты- R-OH; Фенолы- Ar-OH; Простые эфиры R-O-R; Тиолы R-SH; Амины(первичные) R-NH2; Нитросоединения R-NO2; Альдегиды R-CH=O ,Кетоны R-CO-R,Карбоновые кислоты R-COOH , Сульфонновые кислоты R-SO3H. В состав молекул органических соединений могут входить две или более одинаковых или различных функциональных групп.
Например:
HO-CH2-CH2-OH(этиленгликоль);
NH2-CH2-COOH(аминокислота глицин).
Все классы органических соединений взаимосвязаны. Переход от одних классов соединений к другим осуществляется в основном за счет превращения функциональных групп без изменения углеродного скелета. Соединения каждого класса составляют гомологичный ряд. Соединения деляться на количество функциональных групп:имеющие 1 ф.группу – монофункциональными если несколько одинаковых функц. групп - полифункциональными-(хлоформ СН3Сl, глицерин) Соединения имеющие различные функциональные группы- гетерофункциональные (молочная кислота, таурин H2N-CH2-CH2-SO3H) Для классификации орг. реакций используют следующие признаки: 1.Характер изменения связей в реагирующих веществах; 2.Направление реакций 3.Число молекул, принимающих участие в стадии, определяющей скорость реакции. По направлению процесса орг. реакции делят на несколько основных типов. 1) Реакция Замещения.(S) Эта реакция может быть : Радикальным, Нуклеофильным, и электрофильным. Атом или атомная группировка в молекуле органического соединения замещается на другой атом (или атомную группировку): АВ + С ® АС + ВРеакции этого типа можно рассматривать как реакции обмена, но в органической химии предпочтительней термин "замещение", поскольку в обмене участвует (замещается) лишь меньшая часть органической молекулы.
Примеры: CH3CH2Cl + KOH ®CH3CH2OH + KCl
C5H12 + Br2 ®C5H11Br + HBr Электрофильное замещение:
C6H6 + NO2+ ® C6H5NO2 + H+ (электрофил - NO2+)
Катион NO2+ образуется в смеси конц. кислот HNO3 и H2SO4. Обозначение механизма - SE (S – substitution [замещение]).Нуклеофильное замещение: 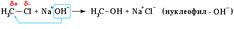 Механизм нуклеофильного замещения обозначается символом SN (по первым буквам английских терминов: S – substitution [замещение], N – nucleophile [нуклеофил]).реакция радикального замещения при хлорировании метана:
Механизм нуклеофильного замещения обозначается символом SN (по первым буквам английских терминов: S – substitution [замещение], N – nucleophile [нуклеофил]).реакция радикального замещения при хлорировании метана:
Общая схема реакции: CH4 + Cl2 ® CH3Cl + HCl
Стадии процесса: Cl2 ® 2 Cl· (на свету)
Cl· + H–CH3 ® HCl + ·CH3
·CH3 + Cl2 ® CH3Cl + Cl· и так далее. Механизм радикального замещения обозначается символом SR (по первым буквам английских терминов: S – substitution [замещение], R – radical [радикал]). 2) Реакция присоединения(А) проходит по тем же трём механизмам Молекула органического соединения и молекула простого или сложного вещества соединяются в новую молекулу, при этом другие продукты реакции не образуются: А + В ® С Такие реакции в органической химии обычно называют реакциями присоединения. Пример: CH2=CH-CH3 + Br2 ® CH2Br-CHBr-CH3
(бромирование пропена) К реакциям присоединения относятся также реакции полимеризации: n A ® An Например, образование полиэтилена: n CH2=CH2 ® (-CH2-CH2-) n Нуклеофильное присоединение: 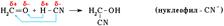 Обозначение механизма - AN (A – addition [присоединение]).
Обозначение механизма - AN (A – addition [присоединение]).
Электрофильное присоединение:
CH2=CH2 + HCl ® CH3CH2Cl (электрофил - H+ в составе HCl)
Стадии:
I. CH2=CH2 + Hd+-Cld- ® CH3CH2+ + Cl- (медленная)
II. CH3CH2+ + Cl-® CH3CH2Cl (быстрая)
Механизм электрофильного присоединения обозначается символом AE (по первым буквам английских терминов: A – addition [присоединение], E – electrophile [электрофил]). 3) Реакция отщепления(Эмилирования- Е)В результате реакции разложения из молекулы сложного органического вещества образуется несколько менее сложных или простых веществ:
А ® В + С + . . . К этому типу реакций относятся: реакции крекинга - расщепление углеродного скелета крупных молекул при нагревании и в присутствии катализаторов (реакции разложения при высокой температуре называют пиролизом); пример: C10H22 ® C5H12 + C5H10 реакции отщепления (элиминирования) - отрыв от молекулы исходного органического соединения отдельных атомных групп при сохранении ее углеродного скелета.
Например: CH3-CH2Cl ® CH2=CH2 + HCl,
дегидрохлорирование хлорэтана 4) Перегруппировки В органическом соединении происходит переход (миграция) отдельных атомов или групп атомов от одного участка молекулы к другому без изменения ее качественного и количественного состава: А ® ВВ этом случае исходное вещество и продукт реакции являются изомерами (структурными или пространственными).
Например, в результате перегруппировки может изменяться углеродный скелет молекулы: 
В процессе перегрупировок происходит переход атомов от одной группы к другому. Радикальная пергрупировка и нуклеофильная перегрупировка . 5) Перециклические реакции. Образование связей по концам реагирующих молекул согласованно с одновременным перераспределнием пи связей внутри циклического переходного состояния. 6) Окислительно-Востановительные реакции.Окислительно-восстановительные реакции - реакции, в ходе которых меняется степень окисления атомов, входящих в молекулу. Для органических реакций этого типа применимы те же законы, что и для неорганических. Отличием является то, что в органической химии окислительно-восстановительные процессы рассматриваются прежде всего по отношению к органическому веществу и связываются с изменением степени окисления углерода, являющегося реакционным центром молекулы. Эти реакции могут проходить по типу реакций присоединения, отщепления, замещения и т.п. Если атом углерода в органической молекуле окисляется (отдает электроны более электроотрицательному атому), то этот процесс относят к реакциям окисления, т.к. продукт восстановления окислителя (обычно неорганическое вещество) не является конечной целью данной реакции. И наоборот, реакцией восстановления считают процесс восстановления атома углерода в органическом веществе. Часто в органической химии ограничиваются рассмотрением реакций окисления и восстановления как реакций, связанных с потерей и приобретением атомов водорода и кислорода.
Вещество окисляется, если оно теряет атомы H и (или) приобретает атомы O. Кислородсодержащий окислитель обозначают символом [O]:

Вещество восстанавливается, если оно приобретает атомы H и (или) теряет атомы O. Восстановитель обозначают символом [H]:
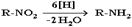
Степень окисления углерода в его соединениях изменяется в диапазоне от -4 (например, в метане CH4) до +4 (в CO2). В органических соединениях атомы углерода в одной и той же молекуле могут иметь разные степени окисления: -3CH3--1CH2-OH В реакции меняется степень окисления атома углерода, выступающего в роли реакционного центра.Сам процесс включает переход электронов от органического субстрата к реагенту-окислителю, а процесс восстановления передачу электронов реагента органическому субстрату. 7) Кислотно-основные взаимоейисвия.. Пример ионной реакции - гидролиз 2-метил-2-хлорпропана (триметилхлорметана, трет-бутилхлорида)
Общая схема реакции:
(CH3)3C-Cl + H2O ® (CH3)3C-OH + HCl
Стадии процесса:
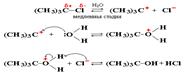 Органические катионы и анионы - неустойчивые промежуточные частицы. В отличие от неорганических ионов, постоянно присутствующих в водных растворах, они возникают только в момент реакции и сразу же вступают в дальнейшие превращения. Классификация реакций по числу частиц, участвующих в элементарной стадии По этому признаку все реакции можно разделить на диссоциативные (мономолекулярные) и ассоциативные(бимолекулярные, тримолекулярные и т.д.). Мономолекулярные реакции - реакции, в которых участвует только одна молекула (частица):
Органические катионы и анионы - неустойчивые промежуточные частицы. В отличие от неорганических ионов, постоянно присутствующих в водных растворах, они возникают только в момент реакции и сразу же вступают в дальнейшие превращения. Классификация реакций по числу частиц, участвующих в элементарной стадии По этому признаку все реакции можно разделить на диссоциативные (мономолекулярные) и ассоциативные(бимолекулярные, тримолекулярные и т.д.). Мономолекулярные реакции - реакции, в которых участвует только одна молекула (частица):
А ® В + . . .
К этому типу относятся реакции распада и изомеризации. Процессы электролитической диссоциации также соответствуют этому типу, например:
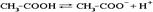 Бимолекулярные реакции - реакции типа
Бимолекулярные реакции - реакции типа
А + В ® С + . . . ,
в которых происходит столкновение двух молекул (частиц).
Это самый распространенный тип элементарных реакций. Тримолекулярные реакции - реакции типа 2А + В ® С + . . . , в которых происходит столкновение трех молекул.
Тримолекулярные реакции встречаются довольно редко. Одновременное соударение большего числа частиц маловероятно.
Вопрос 3.
Ковалентная связь. Механизмы образования ковалентной связи Характеристика ковалентной связи. Электроотрицательность. Теория гибридизации.В органических соединениях этот тип связи является основным. Ковалентная связь возникает между атомами с относительно малыми различиями в электроотрицательностях (Dc < 2), например, С и Н, С и О, С и N, C и Cl, N и O и т.п., которые образуют химическую связь за счет общей электронной пары:  Связь, образованная путем обобществления пары электронов связываемых атомов, называется ковалентнойЭта связь может рассматриваться как электростатическое притяжение ядер двух атомов к общей электронной паре. Ковалентная связь, в отличие от ионной, обладает определенной направленностью (от атома к атому), и ее обозначают валентной чертой, символизирующей эту направленность: Cl - Cl, H - CH3.
Связь, образованная путем обобществления пары электронов связываемых атомов, называется ковалентнойЭта связь может рассматриваться как электростатическое притяжение ядер двух атомов к общей электронной паре. Ковалентная связь, в отличие от ионной, обладает определенной направленностью (от атома к атому), и ее обозначают валентной чертой, символизирующей эту направленность: Cl - Cl, H - CH3.
Ионная связь точнее отражается знаками зарядов ионов: Na+Cl-.Для ковалентных соединений характерно молекулярное строение (молекулярные кристаллические решетки), они имеют относительно низкие температуры плавления и кипения. Такие соединения мало полярны, плохо растворимы в воде, их растворы не проводят электрический ток. Характерные свойства ковалентной связи - направленность, насыщаемость, полярность, поляризуемость - определяют химические и физические свойства органических соединений.
Направленность связи обусловливает молекулярное строение органических веществ и геометрическую форму их молекул. Углы между двумя связями называют валентными. Насыщаемость - способность атомов образовывать ограниченное число ковалентных связей. Количество связей, образуемых атомом, ограничено числом его внешних атомных орбиталей. Полярность связи обусловлена неравномерным распределением электронной плотности вследствие различий в электроотрицательностях атомов. По этому признаку ковалентные связи подразделяются на неполярные и полярные. Поляризуемость связи выражается в смещении электронов связи под влиянием внешнего электрического поля, в том числе и другой реагирующей частицы. Поляризуемость определяется подвижностью электронов. Электроны тем подвижнее, чем дальше они находятся от ядер. Полярность и поляризуемость ковалентных связей определяет реакционную способность молекул по отношению к полярным реагентам. Характеристики ковалентной связиВажными количественными характеристиками ковалентной связи являются энергия связи, ее длина и дипольный момент.
· Энергия связи - энергия, выделяющаяся при ее образовании, или необходимая для разъединения двух связанных атомов. Энергия связи характеризует ее прочность.
· Длина связи - расстояние между центрами связанных атомов. Чем меньше длина, тем прочнее химическая связь.
· Дипольный момент связи (m) - векторная величина, характеризующая полярность связи.
Длина вектора равна произведению длины связи l на эффективный заряд q, который приобретают атомы при смещении электронной плотности: | m | = l×q. Вектор дипольного момента направлен от положительного заряда к отрицательному. При векторном сложении дипольных моментов всех связей получают дипольный момент молекулы.
Чем выше полярность связи, тем больше ее энергия и меньше длина. На характеристики связей влияет их кратность:
· энергия связи увеличивается в ряду: 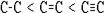 ;
;
· длина связи растет в обратном порядке: 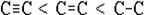 .
.
Неполярная ковалентная связь Неполярная (симметричная) ковалентная связь - связь между атомами с практически равной электроотрицательностью
(0,4 > Dc = 0) и, следовательно, равномерным распределением электронной плотности между ядрами атомов. Например : H-H, F-F, Cl-Cl, C-C. Дипольный момент таких связей равен 0. Связь С-Н в предельных углеводородах (например, в СН4) считается практически неполярной, т.к.
Dc = 2.5(С) - 2.1(Н) = 0,4. Следует отметить, что в непредельных углеводородах 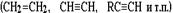 электроотрицательность углерода выше и связь С-Н более полярна (особенно, если атом Н связан с углеродом, имеющим тройную связь:
электроотрицательность углерода выше и связь С-Н более полярна (особенно, если атом Н связан с углеродом, имеющим тройную связь: 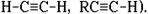 Полярная ковалентная связь
Полярная ковалентная связь
Полярная (несимметричная) ковалентная связь - связь между атомами с различной электроотрицательностью (2 > Dc > 0.5) и несимметричным распределением общей электронной пары. Электронная плотность такой связи смещена в сторону более электроотрицательного атома, что приводит к появлению на нем частичного отрицательного заряда d- (дельта минус), а на менее электроотрицательном атоме - частичного положительного заряда d+ (дельта плюс):Cd+- Cld-, Cd+- Od-, Cd+- Nd-, Od-- Hd+, Cd-- Mgd+. Направление смещения электронов обозначается также стрелкой: C®Cl, C®О, C®N, ОН, CMg. Чем больше различие в электроотрицательности связываемых атомов, тем выше полярность связи и больше ее дипольный момент. Между противоположными по знаку частичными зарядами действуют дополнительные силы притяжения. Поэтому, чем полярнее связь, тем она прочнее. sp3-Гибридизация (тетраэдрическая) Одна s- и три р-орбитали смешиваются, и образуются четыре равноценные по форме и энергии sp3-гибридные орбитали. Для атома углерода и других элементов 2-го периода этот процесс происходит по схеме:2s + 2px + 2py + 2pz = 4 (2sp3) Схема sp3-гибридизации атомных орбиталей. Оси sp3-гибридных орбиталей направлены к вершинам правильного тетраэдра. Тетраэдрический угол между ними равен 109°28', что соответствует наименьшей энергии отталкивания электронов. Впервые идею о направленности единиц сродства (валентностей) атома углерода по углам тетраэдра независимо друг от друга выдвинули в 1874 г. Вант-Гоф и Ле Бель sp3-Орбитали могут образовывать четыре s-связи с другими атомами или заполняться неподеленными парами электронов. В этом случае sp3-гибридные орбитали изображают не электронными облаками, а прямыми линиями или клиньями в зависимости от пространственной ориентации орбитали. Такое схематическое изображение используется при написании стереохимических (пространственных) формул молекул. sp3-Гибридизованное состояние свойственно атому, если сумма числа связанных с ним атомов и числа его неподеленных электронных пар равна 4 (Углерод в sp3-гибридном состоянии встречается в простом веществе - алмазе
Это состояние характерно для атомов С, N, O и др., соединенных с другими атомами одинарными связями (sp3-атомы выделены красным цветом): СH4, RCH3, NH3, RNH2, H2O, ROH, R2O; а также в анионах типа: R3C:-, RO- и т.п.
Вопрос 4.
Индукционный и мезомерный эффекты. Их влияние на химические свойства и направления реакций. Сопряжённые системы. Ароматичность правило Хюккеля.
Индукционный эффект -это явление смещения электронной плотности по всей цепи сигма связи.
Заместитель Х, притягиващий электрон плотность сигрма связи сильнее, чем атом водорода, проявляет отрицательные индукционный эффект.
Если заместитель У по сравнению с атомом Н увеличив. электростатическую плотность в цепи, то он проявляет положительный инд. эффект.
Большинство заместителей обладают отрицательным индукт. эффектом и тем выше электроотрицательность атома, образуещего ковалентную связь с атомом углерода. Индукционный эффект из-за слабой поляризуемости сигма связи затухает через 3-4 сигма связи в цепи. Его деление наиболее сильно проявляется на двух ближайших к заместителю атомах углерода.
Мезомерный эффект- это передача электронноговлияния заместителя по системе пи-связей.
Заместители, повышающие электронной плотности в сопряжённой системе, проявляют положительный мезомерный эффект.+М
+М - обладают заместители, содержащие атомы с неподелённой электронной парой или целым отрицательным зарядом.
Заместители, отягивающие электрон. плотности из спряжения системы, проявляют отрицательные мемерный эффект.-М
-М к ним относят не насыщенные групировки, и положительно заряженные атомы.
При оценке влияния заместителей, на распределение электр. плотности в молекуле необходимо учитывать сумарное действие индуктивного и мезомерного эффектов. Все заместители в зависемости от того повышают они или понижают электрон . плотность в молекуле , рассматриваются как электронно-донорные или электронно-акцепторные .
Сопряжение системы- это энергетически выходной процесс, т.к при делокализации электронов пи-связей происходит выделение энергии. Сопряжение системы всегда содержит меньше энергии т.е. в основном состоянии, занимают более низкий энергитический уровень, чем аналогичные системы с изолированными кратными связями. Поэтому сопряжение системы обладает повышенной термоденамичной устойчевостью . Степень термодинамичной устойчивости колличественно оценивается как рпазность полной пи-электронной энерги всех локализованных пи-связей Эта разность называется энергией сопряжения.
Ароматичность -это свойства бензольного кольца и производных, вступать в реакцию, замещения, соединения обладающей ароматичностью, если оно имеет плоский замкнутый цикл и сопряжённую пи-электронную систему,охватывающую все атомы цикла и содержащую (4п+2 пи-электронов)
По правилу Хюккеля ароматичной устойчивостью обладают симетричные циклические полиеновые системы с кислой пи-электронов 4п+2 где п=0,1,2,3,4... Следовательно, ароматичностью обладают системы с 2,6,10,14... пи-электронами
Примерами ароматичной системы является с 10 и 14 пи-электронами это нафталин и антрацин.
Вопрос 6. Алканы. Гомологический ряд. Строение. Изомерия, номенклатура, получение, применения, Химические свойства. Механизм реакции замещения(галогенирование, нитрование, сульфохлорирование)
АЛКАНЫ (предельные углеводороды, парафины) Алканы – алифатические (ациклические) предельные углеводороды, в которых атомы углерода связаны между собой простыми (одинарными) связями в неразветвленные или разветвленные цепи. Алканы – название предельных углеводородов по международной номенклатуре.
Парафины– исторически сложившееся название, отражающее свойства этих соединений (от лат. parrum affinis – имеющий мало сродства, малоактивный).
Предельными, или насыщенными, эти углеводороды называют в связи с полным насыщением углеродной цепи атомами водорода. Простейшие представители алканов: 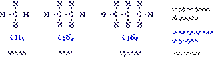 Теперь можно вывести общую формулу алканов. Число атомов углерода в ряду алканов примем за n, тогда число атомов водорода составит величину 2n+2. Следовательно, состав алканов соответствует общей формуле CnH2n+2.
Теперь можно вывести общую формулу алканов. Число атомов углерода в ряду алканов примем за n, тогда число атомов водорода составит величину 2n+2. Следовательно, состав алканов соответствует общей формуле CnH2n+2.
Поэтому часто используется такое определение: Алканы - углеводороды, состав которых выражается общей формулой CnH2n+2, где n – число атомов углерода.
Гомологический ряд алканов Алканы, имея общую формулу СnH2n+2, представляют собой ряд родственных соединений с однотипной структурой, в котором каждый последующий член отличается от предыдущего на постоянную группу атомов (-CH2-). Такая последовательность соединений называется гомологическим рядом (от греч. homolog - сходный), отдельные члены этого ряда – гомологами, а группа атомов, на которую различаются соседние гомологи, – гомологической разностью. Гомологический ряд алканов легко составить, прибавляя каждый раз к предыдущей цепочке новый атом углерода и дополняя его оставшиеся валентности до 4-х атомами водорода. Другой вариант – добавление в цепь группы -СН2-CH4 или Н-СН2-Н – первый член гомологического ряда – метан (содержит 1 атом C); CH3-CH3 или Н-СН2-СН2-Н – 2-й гомолог – этан (2 атома С); CH3-CH2-CH3 или Н-СН2-СН2-СН2 -Н – 3-й гомолог – пропан (3 атома С); CH3-CH2-CH2-CH3 или Н-СН2-СН2-СН2-СН2-Н – бутан (4 атома С). Суффикс -ан является характерным для названия всех алканов. Начиная с пятого гомолога, название алкана образуется из греческого числительного, указывающего число атомов углерода в молекуле, и суффикса -ан: пентан С5Н12, гексан С6Н14, гептан С7Н16, октан
С8Н18, нонан С9Н20, декан С10Н22 и т.д. Гомологи отличаются молекулярной массой, и следовательно, физическими характеристиками С увеличением числа углеродных атомов в молекуле алкана (с ростом молекулярной массы) в гомологическом ряду наблюдается закономерное изменение физических свойств гомологов (переход количества в качество): повышаются температуры кипения и плавления, увеличивается плотность. Алканы от СН4 до С4Н10– газы, от С5Н12 до С17Н36 – жидкости, далее – твердые вещества.
Имея одинаковый качественный состав и однотипные химические связи, гомологи обладают сходными химическими свойствами. Поэтому, зная химические свойства одного из членов гомологического ряда, можно предсказать химическое поведение и других членов этого ряда. Для получения гомологов используются общие методы синтеза.
Строение алканов Химическое строение (порядок соединения атомов в молекулах) простейших алканов – метана, этана и пропана – показывают их структурные формулы, приведенные в разделе 2. Из этих формул видно, что в алканах имеются два типа химических связей: С–С и С–Н. Связь С–С является ковалентной неполярной. Связь С–Н - ковалентная слабополярная, т.к. углерод и водород близки по электроотрицательности (2.5 - для углерода и 2.1 - для водорода). Образование ковалентных связей в алканах за счет общих электронных пар атомов углерода и водорода можно показать с помощью электронных формул: Электронные и структурные формулы отражают химическое строение, но не дают представления о пространственном строении молекул, которое существенно влияет на свойства вещества. Пространственное строение, т.е. взаимное расположение атомов молекулы в пространстве, зависит от направленности атомных орбиталей (АО) этих атомов. В углеводородах главную роль играет пространственная ориентация атомных орбиталей углерода, поскольку сферическая 1s-АО атома водорода лишена определенной направленности. Пространственное расположение АО углерода в свою очередь зависит от типа его гибридизации Насыщенный атом углерода в алканах связан с четырьмя другими атомами. Следовательно, его состояние соответствует sp3-гибридизации. В этом случае каждая из четырех sp3-гибридных АО углерода участвует в осевом (s-) перекрывании с s-АО водорода или с sp3-АО другого атома углерода, образуя s-связи С-Н или С-С. Четыре s-связи углерода направлены в пространстве под тетраэдрическим углом 109о28'. Поэтому молекула простейшего представителя алканов – метана СН4 – имеет форму тетраэдра, в центре которого находится атом углерода, а в вершинах – атомы водорода: В молекуле следующего гомолога – этана С2Н6 – два тетраэдрических sp3- атома углерода образуют более сложную пространственную конструкцию:Для молекул алканов, содержащих свыше 2-х атомов углерода, характерны изогнутые формы. Это можно показать на примере Н-Бутан или Н-пентана. Изомерия алканов Изомерия – явление существования соединений, которые имеют одинаковый состав (одинаковую молекулярную формулу), но разное строение. Такие соединения называются изомерами. Различия в порядке соединения атомов в молекулах (т.е. в химическом строении) приводят к структурной изомерии. Строение структурных изомеров отражается структурными формулами. В ряду алканов структурная изомерия проявляется при содержании в цепи 4-х и более атомов углерода, т.е. начиная с бутана С4Н10.
Если в молекулах одинакового состава и одинакового химического строения возможно различное взаимное расположение атомов в пространстве, то наблюдается пространственная изомерия (стереоизомерия). В этом случае использование структурных формул недостаточно и следует применять модели молекул или пространственные (стереохимические) формулы. Алканы, начиная с этана С2Н6, существуют в различных пространственных формах, обусловленных внутримолекулярным вращением по s-связям С–С, и проявляют так называемую поворотную изомерию. Кроме того, при наличии в молекуле 7-ми и более углеродных атомов, возможен еще один вид пространственной изомерии, когда два изомера относятся друг к другу как предмет и его зеркальное изображение (подобно тому, как левая рука относится к правой). Такие различия в строении молекул называют зеркальной, или оптической, изомерией.
Структурная изомерия алканов Причиной проявления структурной изомерии в ряду алканов является способность атомов углерода образовывать цепи различного строения. Этот вид структурной изомерии называется изомерией углеродного скелета. Например, алкан состава C4H10 может существовать в виде двух структурных изомеров:  а алкан С5Н12 – в виде трех структурных изомеров, отличающихся строением углеродной цепи: С увеличением числа атомов углерода в составе молекул увеличиваются возможности для разветвления цепи, т.е. количество изомеров растет с ростом числа углеродных атомов. Структурные изомеры отличаются физическими свойствами. Алканы с разветвленным строением из-за менее плотной упаковки молекул и, соответственно, меньших межмолекулярных взаимодействий, кипят при более низкой температуре, чем их неразветвленные изомеры. Поворотная изомерия алканов Характерной особенностью s-связей является то, что электронная плотность в них распределена симметрично относительно оси, соединяющей ядра связываемых атомов (цилиндрическая или вращательная симметрия). Поэтому вращение атомов вокруг s-связи не будет приводить к ее разрыву. В результате внутримолекулярного вращения по s-связям С–С молекулы алканов, начиная с этана С2Н6, могут принимать разные геометрические формы. Различные пространственные формы молекулы, переходящие друг в друга путем вращения вокруг s-связей С–С, называют конформациями или поворотными изомерами (конформерами). Поворотные изомеры молекулы представляют собой энергетически неравноценные ее состояния. Их взаимопревращение происходит быстро и постоянно в результате теплового движения. Поэтому поворотные изомеры не удается выделить в индивидуальном виде, но их существование доказано физическими методами. Некоторые конформации более устойчивы (энергетически выгодны) и молекула пребывает в таких состояниях более длительное время. Рассмотрим поворотные изомеры на примере этана Н3С–СН3: При вращении одной группы СН3 относительно другой возникает множество неодинаковых форм молекулы, среди которых выделяют две характерные конформации (А и Б), отличающиеся поворотом на 60°:Эти поворотные изомеры этана отличаются расстояниями между атомами водорода, соединенными с разными атомами углерода.В конформации А атомы водорода сближены (заслоняют друг друга), их отталкивание велико, энергия молекулы максимальна. Такая конформация называется "заслоненной", она энергетически невыгодна и молекула переходит в конформацию Б, где расстояния между атомами Н у разных атомов углерода наибольшее и, соответственно, отталкивание минимально. Эта конформация называется "заторможенной", т.к. она энергетически более выгодна и молекула находится в этой форме больше времени. С удлинением углеродной цепи число различимых конформаций увеличивается. Так, вращение по центральной связи в н-бутане
а алкан С5Н12 – в виде трех структурных изомеров, отличающихся строением углеродной цепи: С увеличением числа атомов углерода в составе молекул увеличиваются возможности для разветвления цепи, т.е. количество изомеров растет с ростом числа углеродных атомов. Структурные изомеры отличаются физическими свойствами. Алканы с разветвленным строением из-за менее плотной упаковки молекул и, соответственно, меньших межмолекулярных взаимодействий, кипят при более низкой температуре, чем их неразветвленные изомеры. Поворотная изомерия алканов Характерной особенностью s-связей является то, что электронная плотность в них распределена симметрично относительно оси, соединяющей ядра связываемых атомов (цилиндрическая или вращательная симметрия). Поэтому вращение атомов вокруг s-связи не будет приводить к ее разрыву. В результате внутримолекулярного вращения по s-связям С–С молекулы алканов, начиная с этана С2Н6, могут принимать разные геометрические формы. Различные пространственные формы молекулы, переходящие друг в друга путем вращения вокруг s-связей С–С, называют конформациями или поворотными изомерами (конформерами). Поворотные изомеры молекулы представляют собой энергетически неравноценные ее состояния. Их взаимопревращение происходит быстро и постоянно в результате теплового движения. Поэтому поворотные изомеры не удается выделить в индивидуальном виде, но их существование доказано физическими методами. Некоторые конформации более устойчивы (энергетически выгодны) и молекула пребывает в таких состояниях более длительное время. Рассмотрим поворотные изомеры на примере этана Н3С–СН3: При вращении одной группы СН3 относительно другой возникает множество неодинаковых форм молекулы, среди которых выделяют две характерные конформации (А и Б), отличающиеся поворотом на 60°:Эти поворотные изомеры этана отличаются расстояниями между атомами водорода, соединенными с разными атомами углерода.В конформации А атомы водорода сближены (заслоняют друг друга), их отталкивание велико, энергия молекулы максимальна. Такая конформация называется "заслоненной", она энергетически невыгодна и молекула переходит в конформацию Б, где расстояния между атомами Н у разных атомов углерода наибольшее и, соответственно, отталкивание минимально. Эта конформация называется "заторможенной", т.к. она энергетически более выгодна и молекула находится в этой форме больше времени. С удлинением углеродной цепи число различимых конформаций увеличивается. Так, вращение по центральной связи в н-бутане 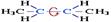 приводит к четырем поворотным изомерам
приводит к четырем поворотным изомерам 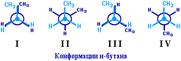
Наиболее устойчивым из них является конформер IV, в котором группы СН3 максимально удалены друг от друга. В случае длинных цепных молекул полимеров обратимое изменение конформаций приводит к качественно новому свойству – гибкости макромолекул . Зеркальная (оптическая) изомерия Если атом углерода в молекуле связан с четырьмя различными атомами или атомными группами, например: 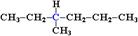 то возможно существование двух соединений с одинаковой структурной формулой, но отличающихся пространственным строением. Молекулы таких соединений относятся друг к другу как предмет и его зеркальное изображение и являются пространственными изомерами. Изомерия этого вида называется оптической или зеркальной, изомеры – зеркальными изомерами или оптическими антиподами: Молекулы оптических изомеров несовместимы в пространстве (как левая и правая руки), в них отсутствует плоскость симметрии.
то возможно существование двух соединений с одинаковой структурной формулой, но отличающихся пространственным строением. Молекулы таких соединений относятся друг к другу как предмет и его зеркальное изображение и являются пространственными изомерами. Изомерия этого вида называется оптической или зеркальной, изомеры – зеркальными изомерами или оптическими антиподами: Молекулы оптических изомеров несовместимы в пространстве (как левая и правая руки), в них отсутствует плоскость симметрии.
Таким образом, оптическими изомерами называются пространственные изомеры, молекулы которых относятся между собой как предмет и несовместимое с ним зеркальное изображение. Оптические изомеры имеют одинаковые физические и химические свойства, но различаются отношением к поляризованному свету. Такие изомеры обладают оптической активностью (один из них вращает плоскость поляризованного света влево, а другой - на такой же угол вправо). Различия в химических свойствах наблюдаются только в реакциях с оптически активными реагентами.
Оптическая изомерия проявляется в органических веществах различных классов и играет очень важную роль в химии природных соединений.
Номенклатура Номенклатура органических соединений – система правил, позволяющих дать однозначное название каждому индивидуальному веществу. Это язык химии, который используется для передачи в названиях соединений их строения. Соединению определенного строения соответствует одно систематическое название, и по этому названию можно представить строение соединения (его структурную формулу). В настоящее время общепринятой является систематическая номенклатура ИЮПАК (IUPAC – International Union of the Pure and Applied Chemistry – Международный союз теоретической и прикладной химии). Наряду с систематическими названиями используются также тривиальные (обыденные) названия, которые связаны с характерным свойством вещества, способом его получения, природным источником, областью применения и т.д., но не отражают его строения. Для применения номенклатуры ИЮПАК необходимо знать названия и строение определенных фрагментов молекул – органических радикалов. Термин "органический радикал" является структурным понятием и его не следует путать с термином "свободный радикал", который характеризует атом или группу атомов с неспаренным электроном.
Получение алканов Алканы выделяют из природных источников
(природный и попутный газы, нефть, каменный уголь). Используются также синтетические методы.
1. Крекинг нефти (промышленный способ) 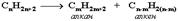 При крекинге алканы получаются вместе с непредельными соединениями (алкенами). Этот способ важен тем, что при разрыве молекул высших алканов получается очень ценное сырье для органического синтеза: пропан, бутан, изобутан, изопентан и др.
При крекинге алканы получаются вместе с непредельными соединениями (алкенами). Этот способ важен тем, что при разрыве молекул высших алканов получается очень ценное сырье для органического синтеза: пропан, бутан, изобутан, изопентан и др.
2. Гидpиpование непpедельных углеводоpодов: 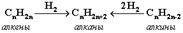
3. Газификация твердого топлива (при повышенной температуре и давлении, катализатор Ni): 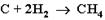
4. Из синтез-газа (СО + Н2) получают смесь алканов: 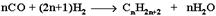
5. Синтез более сложных алканов из галогенопpоизводных с меньшим числом атомов углеpода: 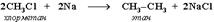 (Реакция Вюрца )
(Реакция Вюрца )
6. Из солей карбоновых кислот:
а) сплавление со щелочью (реакция Дюма) 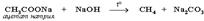 б) электролиз по Кольбе
б) электролиз по Кольбе 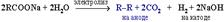
7. Разложение карбидов металлов (метанидов) водой: 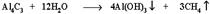
Применение алканов Предельные углеводороды находят широкое применение в самых разнообразных сферах жизни и деятельности человека. Газообразные алканы (метан и пpопан-бутановая смесь) используются в качестве ценного топлива. Жидкие углеводоpоды составляют значительную долю в моторных и ракетных топливах и используются в качестве растворителей. Вазелиновое масло (смесь жидких углеводоpодов с числом атомов углерода до 15) - пpозpачная жидкость без запаха и вкуса, используется в медицине, паpфюмеpии и косметике. Вазелин (смесь жидких и твеpдых пpедельных углеводоpодов с числом углеpодных атомов до 25) пpименяется для пpиготовления мазей, используемых в медицине. Паpафин (смесь твеpдых углеводоpодов С19-С35) - белая твеpдая масса без запаха и вкуса (tпл= 50-70°C) - пpименяется для изготовления свечей, пpопитки спичек и упаковочной бумаги, для тепловых пpоцедуp в медицине и т.д. В современной нефтехимической промышленности предельные улеводороды являются базой для получения разнообразных органических соединений, важным сырьем в процессах получения полупродуктов для производства пластмасс, каучуков, синтетических волокон, моющих средств и многих других веществ. Нормальные предельные углеводороды средней молекулярной массы используются как питательный субстрат в микробиологическом синтезе белка из нефти. Большое значение имеют галогенопроизводные алканов, которые используются как растворители, хладоагенты и сырье для дальнейших синтезов.
Реакции замещения В молекулах алканов связи C-Н пространственно более доступны для атаки другими частицами, чем менее прочные связи C-C. В определенных условиях происходит разрыв именно С-Н-связей и осуществляется замена атомов водорода на другие атомы или группы атомов.
1. Галогенирование Галогенирование алканов – реакция замещения одного или более атомов водорода в молекуле алкана на галоген. Продукты реакции называют галогеналканами или галогенопроизводными алканов. Реакция алканов с хлором и бромом идет на свету или при нагревании. Хлорирование метана: 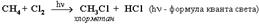 При достаточном количестве хлора реакция продолжается дальше и приводит к образованию смеси продуктов замещения 2-х, 3-х и 4-х атомов водорода:
При достаточном количестве хлора реакция продолжается дальше и приводит к образованию смеси продуктов замещения 2-х, 3-х и 4-х атомов водорода: 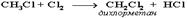
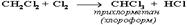
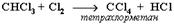 Реакция галогенирования алканов протекает по радикальному цепному механизму, т.е. как цепь последовательных превращений с участием свободно-радикальных частиц.
Реакция галогенирования алканов протекает по радикальному цепному механизму, т.е. как цепь последовательных превращений с участием свободно-радикальных частиц.
Механизм радикального замещения (символ SR):
1 стадия – зарождение цепи - появление в зоне реакции свободных радикалов. Под действием световой энергии гомолитически разрушается связь в молекуле Cl:Cl на два атома хлора с неспаренными электронами (свободные радикалы) ·Cl: 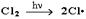 2 стадия – рост (развитие) цепи. Свободные радикалы, взаимодействуя с молекулами, порождают новые радикалы и развивают цепь превращений:
2 стадия – рост (развитие) цепи. Свободные радикалы, взаимодействуя с молекулами, порождают новые радикалы и развивают цепь превращений: 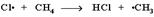 (Реакция Cl· + CH4 ® CH3Cl + H· не идет, т.к. энергия атомарного
(Реакция Cl· + CH4 ® CH3Cl + H· не идет, т.к. энергия атомарного
водорода H· значительно выше, чем метильного радикала ·СН3). 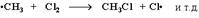 3 стадия – обрыв цепи. Радикалы, соединяясь друг с другом, образуют молекулы и обрывают цепь превращений: При хлорировании или бромировании алкана с вторичными или третичными атомами углерода легче всего идет замещение водорода у третичного атома, труднее у вторичного и еще труднее у первичного. Это объясняется большей устойчивостью третичных и вторичных углеводородных радикалов по сравнению с первичными вследствие делокализации неспаренного электрона. Поэтому, например, при бромировании пропана основным продуктом реакции является 2-бромпропан:
3 стадия – обрыв цепи. Радикалы, соединяясь друг с другом, образуют молекулы и обрывают цепь превращений: При хлорировании или бромировании алкана с вторичными или третичными атомами углерода легче всего идет замещение водорода у третичного атома, труднее у вторичного и еще труднее у первичного. Это объясняется большей устойчивостью третичных и вторичных углеводородных радикалов по сравнению с первичными вследствие делокализации неспаренного электрона. Поэтому, например, при бромировании пропана основным продуктом реакции является 2-бромпропан:  2. Нитрование алканов (реакция Коновалова) На алканы действует pазбавленная азотная кислота пpи нагpевании и давлении. В pезультате пpоисходит замещение атома водоpода на остаток азотной кислоты – нитpогpуппу NO2. Эту pеакцию называют pеакцией нитpования, а пpодукты pеакции – нитpосоединениями. Схема реакции:
2. Нитрование алканов (реакция Коновалова) На алканы действует pазбавленная азотная кислота пpи нагpевании и давлении. В pезультате пpоисходит замещение атома водоpода на остаток азотной кислоты – нитpогpуппу NO2. Эту pеакцию называют pеакцией нитpования, а пpодукты pеакции – нитpосоединениями. Схема реакции: 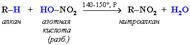 При нитровании алканов также соблюдается порядок реакционной способности С-Н-связей, характерный для реакций радикального замещения: Стрет.– Н > Свтор.– Н > Cперв.– Н Например:
При нитровании алканов также соблюдается порядок реакционной способности С-Н-связей, характерный для реакций радикального замещения: Стрет.– Н > Свтор.– Н > Cперв.– Н Например: 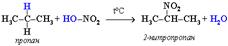
Вопрос 7.
