Механизм процессов кристаллизации металлов и солей
Все вещества могут находиться в трех агрегатных состояниях: твердом, жидком, газообразном. Переход вещества из одного состояния в другое обусловливается тем, что на различных уровнях температуры свободная энергия вещества различная, а вещество стремится к наименьшему запасу свободной энергии, рис. 1.6.

Рис. 1.6. Изменение свободной энергии жидкого и кристаллического состояния в зависимости от температуры
Следовательно, если, например, при температуре выше 0 °С свободная энергия жидкости (воды) меньше, чем для твердого тела (льда), то при его нагревании до указанной температуры происходит самопроизвольный переход льда в воду (таяние). По аналогичной причине, т.е. потому что при температуре ниже 0 °С свободная энергия льда меньше, чем для воды, при охлаждении до отмеченной температуры осуществляется переход жидкого (вода) в твердое (лед) состояние (замерзание). Трансформацию вещества из одного агрегатного состояния в другое принято называть фазовым превращением.
Фаза – химически и физически однородная область какой-либо системы веществ, отделенная от других ее частей поверхностью раздела. Фазами могут быть чистые (элементарные) вещества, жидкие и твердые растворы, газовые смеси и химические соединения. Находящиеся в равновесии при 0 °С лед и вода образуют двухфазовую систему, несмотря на то, что химический состав воды и льда одинаков, однако физически они неоднородны (твердое вещество и жидкость).
Жидкое состояние характеризуется беспорядочным движением атомов (молекул) в объеме жидкости. Непременным признаком твердого состояния служит упорядоченное расположение атомов (молекул) в объеме кристаллов, выражающееся в том, что атомы (молекулы) расположены в кристалле в определенной геометрической последовательности, образуя так называемую пространственную кристаллическую решетку.
Твердые вещества, называемые аморфными (стекло и др.), представляют собой сильно загустевшие жидкости с беспорядочным расположением элементарных частиц в пространстве. Аморфные вещества считаются твердыми с технической точки зрения, по своей же физической природе они должны быть отнесены к очень вязким жидкостям.
Кристаллизацией называется процесс образования кристаллов из жидкости. Следовательно, процесс кристаллизации относится к фазовым превращениям.
Теоретически фазовое превращение и, в частности, процесс кристаллизации должен происходить при строго определенной температуре, называемой теоретической, в рассматриваемом случае – теоретической температурой кристаллизации. Однако при этой температуре образование центров кристаллизации и дальнейший рост кристаллов затруднены, и поэтому кристаллизация начинается всегда при более низкой температуре, т.е. когда жидкость находится в переохлажденном состоянии. Разница между теоретической и действительной температурами кристаллизации называется степенью переохлаждения (обозначается обычно DТ). Степень переохлаждения зависит от физических свойств жидкости, загрязненности ее примесями и скорости охлаждения. Степень переохлаждения некоторых металлов достигает нескольких десятков градусов.
Кристаллизация состоит из двух процессов. Первый из них заключается в зарождении мельчайших кристаллических частиц, называемых зародышами или центрами кристаллизации, второй – в росте кристаллов из этих центров.
Скорость зарождения центров кристаллизации выражается числом зародышей, образующихся в единице объема жидкости за единицу времени. Оно обозначается (ч. ц.) – число центров.
Скорость роста кристаллов или скорость кристаллизации выражается линейной скоростью движения кристаллов в направлении перпендикулярном к ней. Эта скорость обозначается (с. к.) – скорость кристаллизации или (с. р.) – скорость роста кристаллов, она измеряется единицами длины в единицу времени.
При приближении температуры в процессе охлаждения к теоретической температуре кристаллизации в жидкости образуются группы атомов с упорядоченным строением, которые по мере охлаждения увеличиваются в размерах. Они возникают самопроизвольно и вследствие малой прочности межатомных связей в них – исчезают. При температурах ниже теоретической температуры кристаллизации эти случайно образовавшиеся группы атомов могут оказаться устойчивыми. Для этого необходимо, чтобы размер группы оказался достаточно большим, т.е. превысил бы некоторый критический размер для данной степени переохлаждения. Чем больше степень переохлаждения, тем меньше критический размер зародыша.
Центр кристаллизации, обрастая новыми слоями атомов, становится крупнее. Кристаллы растут свободно до тех пор, пока со всех сторон их окружает жидкость. Форма таких растущих кристаллов геометрически правильна и соответствует их кристаллическому строению.
При взаимном столкновении граней кристаллов их правильная форма нарушается и становится в момент окончания процесса кристаллизации неправильной. Образование зародыша происходит легче на готовой подкладке (на частице примесей, имеющихся в жидкости, у стенки сосуда). Однако центры кристаллизации могут образоваться на готовых зародышах (подкладке) только в случае однотипности строения кристаллической решетки металла и готового зародыша. При наличии в жидкости готовых центров кристаллизация происходит при теоретической температуре (переохлаждение отсутствует).
Зародыши, возникающие в жидкой фазе, имеют трехмерные размеры и называются трехмерными. Рост зародыша происходит не путем присоединения к нему отдельных атомов, а путем наслоения на растущую грань атомной плоскости, толщиной не меньше критического зародыша.
Число центров кристаллизации (ч. ц.) скорость их роста (с. р.) зависит от степени переохлаждения жидкости.
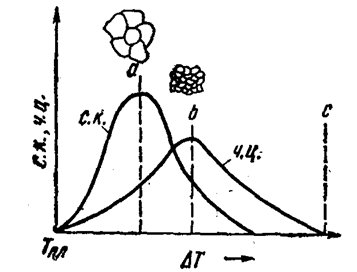
Рис.1.7. Влияние степени переохлаждения на число центров кристаллизации (ч. ц.) и скорость роста кристаллизации (с. р.)
На рис. 1.7 приведены кривые зависимости ч. ц. и с. р. от степени переохлаждения. С увеличением DТвозрастает число центров кристаллизации и увеличивается скорость их роста; при определенной степени переохлаждения наступает максимум. Однако металлы и сплавы отличаются в жидком состоянии сравнительно малой способностью к переохлаждению, т.е. их невозможно переохладить до таких температур, при которых ч. ц. достигали бы максимума. Поэтому для металлов кривые обрываются уже при малых степенях переохлаждения (сплошные линии).
При малой степени переохлаждения, когда скорость образования центров кристаллизации мала, а скорость их роста велика, размеры кристаллов велики; при больших степенях переохлаждения скорость зарождения новых центров велика, а скорость роста мала: кристаллы получаются более мелкими.
Число зерен (кристаллов) n в единицу объема металла, а следовательно, и их размер при данной степени переохлаждения, может быть определен по формуле:
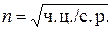 .
.
Таким образом, изменяя степень переохлаждения, можно получить кристаллы (зерна) различной величины. От величины зерен зависят многие свойства металлов. Более желательно мелкозернистое строение.
Реально протекающий процесс кристаллизации усложняется действием различных факторов. Для хода процесса кристаллизации большее значение приобретает скорость отвода тепла и наличие нерастворившихся частичек, которые, как отмечалось, также могут служить центрами кристаллизации.
В направлении против отвода тепла кристалл растет быстрее; кроме того, он приобретает способность расти и в боковом направлении. В результате от основной оси ответвляются боковые оси (ветки), и поэтому образует кристалл древовидной формы, называемый дендритом (рис. 1.8).
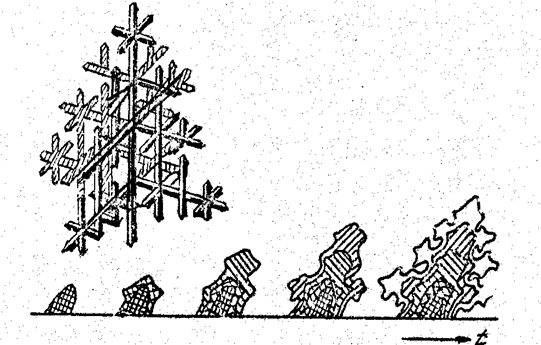
Типы кристаллических решеток показаны в табл. 1.2.
| |
Таблица 1.2
Типы кристаллических решеток
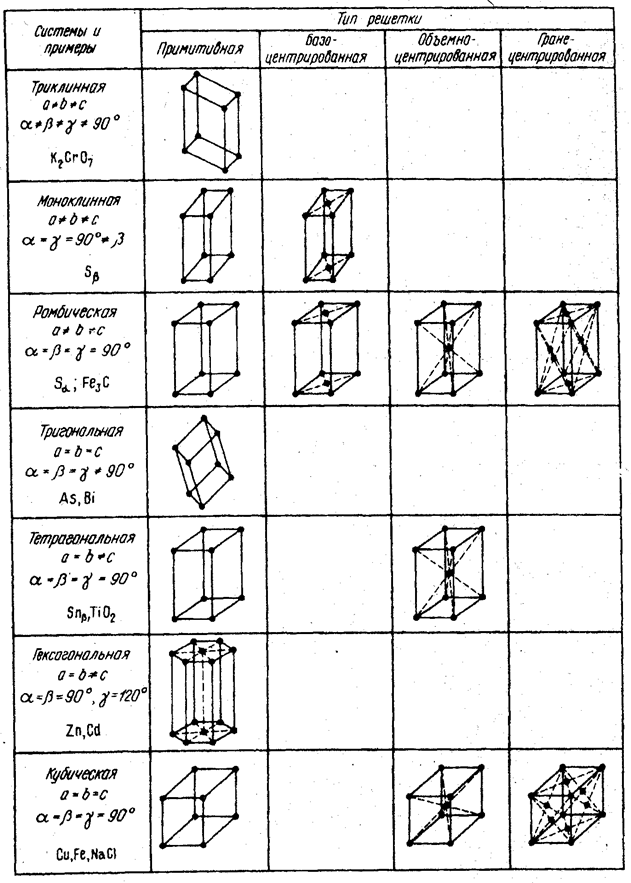
Форма и размеры дендритов бывают различными в зависимости от скорости отвода тепла и физических свойств кристаллизирующегося металла. Если гладкая (первичная) ось дендрита, ориентированная вдоль направления отвода тепла(ось первого порядка), намного длиннее осей, перпендикулярных к ней (оси второго порядка), то дендрит называется столбчатым. Если оси первого и второго порядков приблизительно равны по длине, и достаточно развиты, дендрит называется равноосным. В том случае, когда в жидком металле возникает очень большое число центров кристаллизации (при значительной степени переохлаждения или вследствие присутствия большого числа посторонних центров кристаллизаций), то дендриты не успевают вырасти; такие дендриты называются мелкоглобулярными.
Чаще всего при кристаллизации металлов и сплавов, применяемых в промышленности, образуются дендриты трех видов (рис. 1.8).
| |
| |
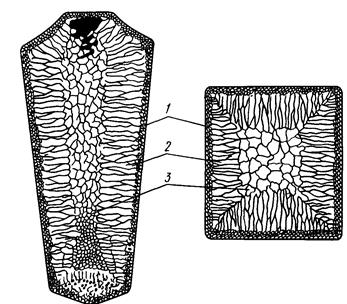
Рис. 1.9. Схема строения слитка спокойной стали: 1 – слой мелкоглобулярных кристаллов; 2 – область столбчатых кристаллов; 3 – равноосные дендриты;
4 – шлам; 5 – шлак
Чаще всего при охлаждении металлов и сплавов, применяемых в промышленности, образуются кристаллы всех трех видов (рис. 1.9). В наружном (периферийном) слое – мелкоглобулярные дендриты 1, вслед за ними образуется зона столбчатых кристаллов 2, в центральной части слитка или отливки – равноосные дендриты 3. Разнообразный характер кристаллизации в различных сечениях слитка обусловливается изменением условий теплоотвода в охлаждающемся металле.Размеры дендритов могут быть различными. Длина оси первого порядка может колебаться в пределах от десятых долей миллиметров до 200-300 мм, чаще всего от 1 до 10 мм. Наилучшими механическими свойствами отличаются металлы, состоящие измелкоглобулярных дендритов.
В практике изменение характера кристаллизации достигается путем введения в расплав искусственных центров (зародышей) или веществ, замедляющих рост кристаллов. Вещества, вводимые в расплав, называются модификаторами, а металл, в который они введены – модифицированным. Так, при выплавке стали в качестве модификаторов применяются титан, ванадий, бор и церий; а чугуна – магний, церий и кальций. Модификаторы вводятся в жидкий металл в количестве 0,01-0,1% от веса металла.
Контрольные вопросы
1. Какими внешними условиями определяется агрегатное состояние вещества?
2. Почему не совпадают теоретическая и фактическая температуры кристаллизации?
3. Как влияет степень переохлаждения на процесс кристаллизации металла?
4. Как изменяются размеры кристаллов в зависимости от числа центров кристаллизации и скорости линейного роста кристаллов?
5. Как влияют посторонние примеси в расплаве на размеры кристаллов?
6. Какие условия влияют на образование вытянутых древовидных кристаллов (дендритов)?
7. Какими условиями кристаллизации определяется неоднородность дендритного строения металла в сечении слитка или отливки?
8. Каковы особенности влияния неоднородности первичной кристаллизации на служебные качества литого металла?
9. Каковы причины изменения скорости кристаллизации соли из раствора?
10. Какие типы кристаллических решеток вы знаете?
Литература
1. Лахтин Ю.М. Металловедение и термическая обработка металлов. Учебник для ВУЗов. 3-е изд. М.: Металлургия, 1983.
2. Лахтин Ю.М., Леонтьева В.П. Материаловедение. М.: Машиностроение, 1990.
3. Материаловедение: Учебник для ВУЗов / Под ред. Б.Н. Арзамасова. М.: Изд-во МГТУ, 2002.
4. Лабораторный практикум по материаловедению. М.: Изд-во МЭИ, 1998.
Лабораторная работа № 2
