В реакции, протекающей в соответствии с термохимическим уравнением
3H2 + N2 = 2 NH3 + 92 кДж
выделилось 23 кДж теплоты. Объём полученного (при н.у.) аммиака
2) 11,2л
24) По термохимическому уравнению С2Н4+Н2О↔С2Н5ОН+46 кДж
вычислите объём взятого этилена (н.у.), если известно, что выделившаяся в этом процессе теплота составила 138 кДж.
3) 67,2л
25) В реакцию, протекающую в соответствии с термохимическим уравнением 2Al + 3S = Al2S3 +509 кДж вступило 108 г алюминия. Количество выделившейся теплоты равно
3) 1018 кДж
26) В результате реакции, термохимическое уравнение которой 2Al +Fe2O3 = Al2O3 + 2 Fe +848 кДж, выделилось 169,6 кДж теплоты. Масса образовавшегося железа равна:
2) 22,4 г
27) По термохимическому уравнению реакции горения ацетилена 2С2Н4 + 5О2 = 4СО2 + 2Н2О +2610 кДж рассчитайте, сколько выделится теплоты, если в реакцию вступило 67, 2 л ацетилена (н.у.)
2) 3915 кДж
28) Уравнение константы равновесия гетерогенной химической реакции 2H2S(г) + SO2(г) ↔ 2S(к) + 2Н2O (г)…
1) 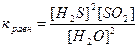 2)
2) 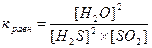
3) 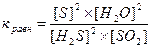 4 )
4 ) 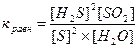
29) Уравнение константы равновесия гетерогенной химической реакции
2СО(г)↔С (графит) +СО2(г) имеет вид…
1) 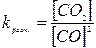 2)
2) 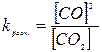
3) 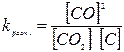 4)
4) 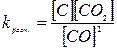
30) Как нужно изменить давление, чтобы реакция гемоглобина с кислородом Hb + O2 « HbO2 была смещена вправо
2) увеличить давление
31) Какое значение константы равновесия соответствует данной реакции 2NO +O2 « 2NO2
2) Kc= [NO2]2 / [NO]2[O2]
32) Как нужно изменить давление реакции N2+3H2 « 2 NH3, чтобы сместить равновесие вправо
2) увеличить
Будет ли влиять давление на смещение равновесия данной реакции
H2 + Cl2 = 2 HCl
2) нет
34) Какие значения должна принимать энергия Гиббса, чтобы процесс шёл в обратном направлении
2) DG0 > 0
35) Равновесие в реакции, уравнение которой СН4(г) + 4S(ж) ↔ СS2(г) + 2Н2S(г), ΔH<0, сместиться влево при
4) увеличении концентрации H2S
36) Будет ли проходить реакция в прямом направлении, если DG = 18 кДж/моль
1) нет
Система, в которой повышение давления и повышение температуры приведут к смещению равновесия в противоположных направления
4) С2Н2(г) + 2Н2(г) ↔ С2Н6 (г), ΔН<0
38) Как нужно изменить давление, чтобы реакция гемоглобина с кислородом была смещена влево Hb + O2 « HbO2
1) уменьшить давление
39) В реагирующей системе, уравнение которой NO(г) + Cl2(г) ↔ NOCl2(г) ΔH > 0, равновесие сместиться вправо при:
1) повышении давления
40) Какие значения должна принимать энергия Гиббса, чтобы процесс шёл в прямом направлении
1) DG < 0
Как нужно изменить давление, чтобы сместить равновесие реакции
N2 + 3H2 «2 NH3 влево
1) уменьшить
42) Для смещения равновесия в системе SO2(г)+Cl2(г) 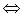 SO2Cl2(г), ΔH < 0 в сторону продуктов реакции необходимо
SO2Cl2(г), ΔH < 0 в сторону продуктов реакции необходимо
1) понизить температуру
На состояние химического равновесия в системе
2SO2(г) + О2 (г) ↔2 SO3, ΔH0 < 0 не влияет
1) катализатор
44) Какое выражение соответствует константе химического равновесия для данной реакции N2+3H2 = 2NH3
2) Кс = [NH3]2 / [N2][H2]3
45) Будет ли влиять давление на смещение равновесия данной реакции H2 + Cl2 = 2 HCl
2) нет
