Высшие карбоновые (жирные) кислоты
Напомним, что высшим карбоновым кислотам относят такие карбоновые кислоты, молекулы которых содержат сравнительно большое число атомов углерода (С9-С26).
По причине того, что высшие карбоновые кислоты входят в состав животных и растительных жиров их называют высшими жирными кислотами.
Примеры предельных высших жирных кислот:
1. Каприновая кислота - C9H19COOH,
2. Лауриновая кислота - С11Н23СООН,
3. Миристиновая кислота - С13Н27СООН,
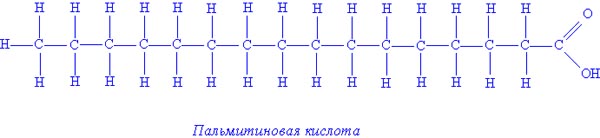
4. Пальмитиновая кислота - С15Н31СООН,
5. Стеариновая кислота – С17Н35СООН.
Примеры непредельных высших жирных кислот:
1. Олеиновая кислота - С17Н33СООН – имеет одну двойную связь,
2. Линолевая кислота – С17Н31СООН - имеет две двойных связи,
3. Линоленовая кислота – С17Н29СООН – имеет три двойных связи.
Структурные формулы соединений, в которых присутствуют длинные углеводородный радикалы, часто изображают следующим образом:
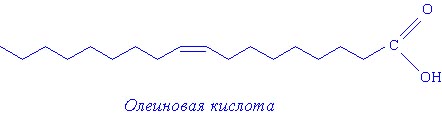
В углеводородной цепи атомы углерода расположены не по прямой линии, а виде «змейки». Угол между двумя соседними отрезками такой «змейки» 109 градусов 28 минут. В случае двойной связи угол другой.
В структурной формуле каждая вершина такой «змейки» означает атом углерода, соединённый с двумя атомами водорода. Последний атом углерода соединён с тремя атомами водорода. При этом сами символы углерода (С) и водорода(Н) не изображаются.
Предельные и непредельные жирные кислоты имеют в значительной степени различные свойства.
Высшие предельные кислоты – воскообразные вещества, непредельные – жидкости (напоминающие растительное масло).
Натриевые и калиевые соли высших жирных кислот называют мылами.
Например:
C17H35COONa – стеарат натрия,
С<sub15< sub="">Н31СООК</sub15<> – пальмитат калия.
Натриевые мыла – твёрдые, калиевые – жидкие.
Примеры карбоновых кислот
Уксусная кислота
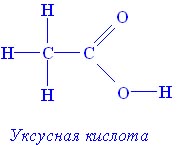
Уксусная кислота – жилкость с острым раздражающим запахом.
Температура кипения 118,5 градусов С, при +16,6 градусах С застывает в кристаллическую массу, похожую на лёд.
Смешивается с водой в любых соотношениях.
Широко применяется как прправа к пище и консервирующее средство. В продаже встречается в виде уксусной эссенции (80%) и уксуса (9,3%).
Натуральный или винный уксус – продукт, содержащий уксусную кислоту и получающийся при скисании виноградного вина.
Уксусная кислота используется также при синтезе многих органических веществ и в качестве растворителя.
Уксусную кислоту получают преимущественно синтезом из ацетилена – присоединением к нему воды и окислением образующегося уксусного альдегида.
Бензойная кислота
Бензойная кислота простейшая одноосновная кислота ароматического ряда. ФормулаС6Н5-СООН.
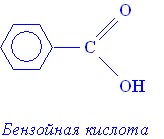
На вид – бесцветные кристаллы.
Бензойная кислота – антисептик. Применяется для консервирования пищевых продуктови во многих органических синтезах.
Щавелевая кислота
Щавелевая кислота – простейшая двухосновная карбоновая кислота.
Формула НООС-СООН.
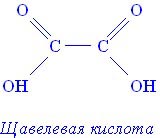
Щавелевая кислота – кристаллическое вещество, растворяется в воде, ядовита.
В виде кислой калиевой соли содержится во многих растениях.
Применяется для крашения тканей.
Терефталевая кислота
Терефталевая кислота НООС-С6Н4-СООН
Двухосновная карбоновая кислота ароматического ядра.
Её структурная формула:
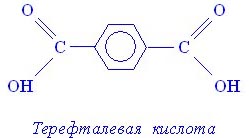
Из терефталевой кислоты и этиленгликоля получают синтетическое волокно лавсан.
Молочная кислота
Молочная кислота может служить примером соединения со смешанными функциями – проявляет свойства кислоты и спирта (спиртокислота)
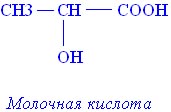
Она образуется при молочнокислом брожении сахаристых веществ, вызываемых особыми бактериями. Содержится в кислом молоке, рассоле квашеной капусты, силосе.
Салициловая кислота
Салициловая кислота – аналог молочной кислоты в ароматическом ряду. Имеет строение:
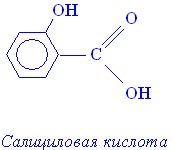
Относится к соединениям со смешанными функциями – проявляет свойства кислоты и фенола (фенолокислота).
Салициловая кислота – антисептик. Её используют (особенно её соли и эфиры) как лекарственное вещество.
Также салициловую кислоту используют при синтезе других продуктов.
Сложные эфиры. Жиры.
Раньше мы уже рассмотрели класс веществ, называемых простыми эфирами. Теперь рассмотрим эфиры сложные.
Между простыми и сложными эфирами есть общее.
Простые эфиры
И те и другие – это органические соединения, молекулы которых состоят из углеводородных радикалов, связанных атомами кислорода.
Для простых эфиров верна формула: R-O-R или R1-O-R2.
В простых эфирах в качестве углеводородных радикалов (R, R1, R2) всегда выступают остатки спиртов.
Пример простого эфира - диэтиловый эфир С2Н5-О-С2Н5, состоит из двух остатков этилового спирта, связанных атомом кислорода.
Сложные эфиры
В случае сложных эфиров, одним из радикалов также является остаток спирта (илифенола). А вторым радикалом является остаток какой-либо кислоты. Кислота может быть как органической, так и минеральной.
Спирты и фенолы взаимодействуют с кислотами, образуя сложные эфиры:
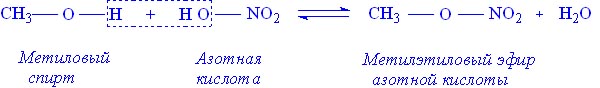
Реакция образования сложного эфира из кислоты и спирта (или фенола) называетсяреакцией этерификации.
