Основные классы неорганических соединений
К основным классам неорганических соединений относятся оксиды, кислоты, основания и соли.
Задания по теме «Основные классы неорганических соединений» предполагают запись названий и химических формул (в том числе графических формул) кислот, оснований, солей и уравнений их электролитической диссоциации.
При записи уравнений электролитической диссоциации необходимо учитывать следующее. Вещества, способные в растворах и расплавах распадаться на ионы называются электролитами. Электролитами являются кислоты, основания и соли. По характеру диссоциации в водных растворах различают сильные и слабые электролиты.
Кислоты диссоциируют, отщепляя ионы H+, при этом сильные кислоты (HCl, HBr, HI, HMnO4, HClO4, HClO3, HNO3, H2SO4, H2CrO4) диссоциируют полностью и необратимо:
HNO3 ® H+ + NO3–;
HClO4 ® H+ + ClO4–;
H2SO4 ® 2 H+ + SO42– (в разбавленных растворах)1
Слабые кислоты (HF, HNO2, HClO, HClO2, H2S, H2Se, H2Te, H2SO3, H2SeO3, H2TeO3, H2CO3, H2SiO3, H3PO4, H3AsO4, CH3COOH) диссоциируют обратимо и неполностью:
HClO2 ⇆ H+ + ClO2–
CH3COOH ⇆ CH3COO– + H+ .
Многоосновные слабые кислоты диссоциируют ступенчато:
H3PO4 ⇆ H+ + H2PO4–
H2PO4– ⇆ H+ + HPO42–
HPO42– ⇆ H+ + PO43– .
Следует обратить внимание, что отрицательный заряд на анионе кислотного остатка равен числу отщепившихся от молекулы кислоты ионов водорода.
Сильные основания (к ним относятся гидроксиды щелочных и щелочноземельных металлов) диссоциируют полностью и необратимо:
NaOH → Na++ OH–
Ba(OH)2 → Ba2+ + 2 OH–.
Слабые основания диссоциируют неполностью, процесс их диссоциации обратим; слабые многокислотные основания диссоциируют ступенчато:
Al(OH)3 ⇆ Al(OH)2+ + OH–
Al(OH)2+ ⇆ AlOH2+ + OH–
AlOH2+ ⇆ Al3+ + OH– .
Слабым основанием традиционно считается гидроксид аммония.2
NH4OH ⇆ NH4+ + OH–.
Составляя названия кислородсодержащих кислот и их солей необходимо учитывать, что если степень окисления3 элемента, образовавшего кислоту равна номеру группы (высшая степень окисления), то название этой кислоты производят от названия элемента с добавлением окончания -ная или -овая (-евая): HClO4 – хлорная, H2SO4 – серная, H2SeO4 – селеновая, HNO3 – азотная, H2CO3 – угольная, H2SiO3 – кремниевая. Если данный элемент может иметь ещё одну (более низкую) степень окисления, то в названии кислородсодержащей кислоты, образованной элементом в более низкой степени окисления появляется суффикс -истая:
 |
Примечания
1. Строго говоря, серная кислота диссоциирует как сильный электролит только по первой стадии: H2SO4 ® H+ + HSO4–; диссоциация по второй стадии протекает по типу слабого электролита: HSO4– ⇄ H+ + SO42–. Однако в разбавленных растворах вторая стадия диссоциации протекает практически полностью, и уравнение диссоциации можно записать в виде H2SO4 ® 2 H+ + SO42–.
2. Существует альтернативная точка зрения, согласно которой аммиак частично взаимодействуют с водой NH3 + HOH ⇆ NH3×HOH, а образующийся гидрат NH3×HOH далее диссоциирует необратимо, т.е. по типу сильного электролита: NH3×HOH ® NH4+ + OH–.
3. Понятие степени окисления более подробно рассматривается в разделе 3 «Окислительно-восстановительные реакции» (стр. 20).
H2SO4 – серная кислота (S+6), H2SO3 – сернистая кислота (S+4);
HNO3 – азотная кислота (N+5), HNO2 – азотистая кислота (N+3);
H3AsO4 – мышьяковая кислота (As+5), H3AsO3 – мышьяковистая кислота (As+3);
H3PO4 – фосфорная кислота (P+5), H3PO3 – фосфористая кислота (P+3).
Названия солей кислородсодержащих кислот имеют суффикс -ат, если кислота образована элементом в высшей степени окисления; если данный элемент может иметь ещё одну (более низкую) степень окисления, то название соли в этом случае имеет суффикс -ит:
H2SO4 – сульфаты (S+6); H2SO3 – сульфиты (S+4);
HNO3 – нитраты (N+5); HNO2 – нитриты (N+3);
H3AsO4 – арсенаты (As+5); H3AsO3 – арсениты (As+3);
H3PO4 – фосфаты (P+5); H3PO3 – фосфиты (P+3).
Если элемент в кислородсодержащих кислотах может иметь более двух степеней окисления, то по мере понижения степени окисления суффиксы меняются в следующем порядке: -ная (-овая), -оватая, -истая, -оватистая.
|
хлорная хлорноватая хлористая хлорноватистая


|
|
|
|
|
|
|
 соли гипохлориты соли хлориты соли хлораты соли перхлораты
соли гипохлориты соли хлориты соли хлораты соли перхлораты

 |  | ||||
 |
 приставка гипо- суффикс -ит суффикс -ат приставка пер-
приставка гипо- суффикс -ит суффикс -ат приставка пер-
указывает на понижение (более низкая (более высокая указывает на повышение
степени окисления степень окисления) степень окисления) степени окисления
Если элемент в одной и той же степени окисления образует несколько кислородсодержащих кислот с разным содержанием молекул воды, то к названию кислоты с меньшим её содержанием добавляется приставка мета-, а при наибольшем её содержании – приставка орто- :
HBO2 – метаборная кислота, H3BO3 – ортоборная кислота;
HAlO2 – метаалюминиевая кислота, H3AlO3 – ортоалюминиевая кислота;
H2SiO3 – метакремниевая кислота, H4SiO4 – ортокремниевая кислота
HPO3 – метафосфорная кислота, H3PO4 – ортофосфорная кислота
Названия бескислородных кислот состоят из двух частей: названия элемента, образовавшего кислоту и слова «водородная»: HF – фтороводородная, HCl – хлороводородная, HBr – бромоводородная, H2S – сероводородная, H2Se – селеноводородная, H2Te – теллуроводородная.
Названия солей бескислородных кислот образуются от названия элемента и содержат суффикс -ид: соли HF – фториды, HCl – хлориды, HBr – бромиды, HI – иодиды, H2S – сульфиды, H2Se – селениды, H2Te – теллуриды. Следует обратить внимание, что суффикс -ид характерен для названий бинарных соединений.
При выполнении заданий, связанных с написанием формул солей, следует учитывать, что любую соль можно рассматривать как продукт замещения атомов водорода в молекуле кислоты на атомы металла. При полном замещении, например, H3PO4 ® Na3PO4 образуются средние соли; при неполном H3PO4 ® Na2HPO4; H3PO4 ® NaH2PO4 – кислые соли.
Любую соль можно также рассматривать, как продукт, образующийся в результате замены гидроксогрупп основания на кислотный остаток; при полной замене получаются средние соли: Fe(OH)3 ® Fe(NO3)3; при неполной замене – основные соли: Fe(OH)3 ® FeOH(NO3)2; Fe(OH)3 ® Fe(OH)2NO3.
Подавляющее большинство солей являются сильными электролитами и в водных растворах диссоциируют на катионы и анионы необратимо и полностью:
Fe2(SO4)3 → 2 Fe3+ + 3 SO42–
Ca(H2PO4)2 → Ca2+ + 2 H2PO4–
AlOH(NO3)2 → AlOH2+ + 2 NO3–
Анионы кислых и катионы основных солей далее диссоциируют по типу слабых электролитов:
H2PO4– ⇆ H+ + HPO42–
HPO42– ⇆ H+ + PO43–
AlOH2+ ⇆ Al3+ + OH–
Для того чтобы правильно составить название соли, следует сначала назвать анион, а затем катион в родительном падеже. Примеры названий средних солей: Na2SO4 – сульфат натрия, AlCl3 – хлорид алюминия, Fe2(SO4)3 – сульфат железа (III), KMnO4 – перманганат калия.
В состав аниона кислой соли входят незамещённые на металл атомы водорода. Если в составе аниона кислой соли присутствует один атом водорода, то в названии этого аниона появляется приставка гидро-, если два атома водорода – дигидро-, три атома водорода – тригидро- и т.д. Например, NaHSO4 – гидросульфат натрия, Al(H2PO4)3 – дигидрофосфат алюминия, Ca(HCO3)2 – гидрокарбонат кальция.
В состав катиона основной соли входят гидроксогруппы, не замещённые на кислотный остаток. Если в составе катиона основной соли присутствует одна гидроксогруппа, то в названии катиона появляется приставка гидроксо-, если две гидроксогруппы – дигидроксо-, три гидроксогруппы – тригидроксо- и т.д. Например, FeOHSO4 – сульфат гидроксожелеза (III), (FeOH)2CO3 – карбонат гидроксожелеза (II), ZnOHCl – хлорид гидроксоцинка, (Al(OH)2)2SO4 – сульфат дигидроксоалюминия.
Для того чтобы правильно записать формулу соли по её названию, необходимо:
1) записать химические символы катиона и аниона;
2) определить заряд катиона и заряд аниона;
3) расставить в формуле соли индексы, таким образом, чтобы число положительных зарядов равнялось числу отрицательных.
Пример 1.1 Ортофосфат кальция
1) Ca PO4
2) Ca+2 PO4–3
3) условие электронейтральности будет выполнено, если взять 3 иона Ca2+ и 2 иона PO43–: формула соли – Ca3(PO4)2.
Пример 1.2 Фосфат дигидроксоалюминия.
1) Al(OH)2 PO4
2) ион алюминия имеет заряд +3, каждый из двух гидроксид-ионов имеет заряд минус 1, поэтому катион дигидроксолюминия имеет заряд +1; заряд фосфат иона – минус 3: Al(OH)2+ PO43–
3) условие электронейтральности будет выполнено, если взять 3 иона Al(OH)2+ и 1 ион PO43–; формула соли: (Al(OH)2)3PO4.
Пример 1.3 Гидрокарбонат магния
1) Mg HCO3
2) ион магния имеет заряд +2; отрицательный заряд аниона кислотного остатка равен числу отщеплённых от молекулы кислоты ионов водорода: гидрокарбонат-ион образуется в результате отрыва от молекулы кислоты H2CO3 одного иона H+, следовательно, заряд гидрокарбонат иона – минус 1: Mg2+ HCO3–
3) условие электронейтральности будет выполнено, если взять 1 ион Mg2+ и 2 иона HCO3–; формула соли: Mg(HCO3)2.
Ниже приводится примеры построения графических формул веществ.
Пример 1.4 Написать графическую формулу ортофосфорной кислоты (H3PO4).
При построении графических формул кислородсодержащих кислот рекомендуется придерживаться определённой последовательности действий:
1) Записать символ элемента, которым образована кислота: P
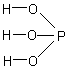 2) Определить основность кислоты, т.е. число атомов водорода, способных заместиться на металл (3 атома H)
2) Определить основность кислоты, т.е. число атомов водорода, способных заместиться на металл (3 атома H)
3) Каждый атом водорода, способный заместиться на металл, соединить химическими связями с атомом элемента через атом кислорода.
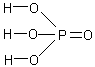 4) Соединить химическими связями оставшиеся атомы (кислорода и/или водорода) непосредственно с атомом элемента, образующим кислоту, учитывая, что водород одновалентен, а кислород двухвалентен.
4) Соединить химическими связями оставшиеся атомы (кислорода и/или водорода) непосредственно с атомом элемента, образующим кислоту, учитывая, что водород одновалентен, а кислород двухвалентен.
При записи графических формул солей необходимо:
1) записать графическую формулу аниона (эту формулу легко получить из графической формулы кислоты, удалив атомы водорода); если в состав соли входит несколько анионов, то их удобно записывать друг под другом;
2) записать графическую формулу катиона (эту формулу можно получить из графической формулы основания, удалив гидроксогруппы); если в состав соли входит несколько катионов, то их удобно записывать друг под другом;
3) соединить свободные валентности анионов и катионов.
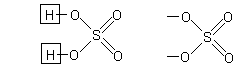 Пример 1.5 Fe2(SO4)3
Пример 1.5 Fe2(SO4)3
 1) Графическая формула аниона получается из графической формулы серной кислоты, удалением всех атомов водорода (т.к. соль средняя).
1) Графическая формула аниона получается из графической формулы серной кислоты, удалением всех атомов водорода (т.к. соль средняя).
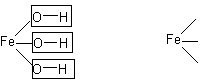 2) Графическая формула катиона получается из графической формулы гидроксида железа (III), удалением всех гидроксогрупп (т.к. соль средняя).
2) Графическая формула катиона получается из графической формулы гидроксида железа (III), удалением всех гидроксогрупп (т.к. соль средняя).

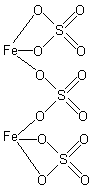 3) В состав соли входит 2 катиона и 3 аниона; расположив катионы и анионы друг под другом, и, соединив свободные химические связи катионов со свободными химическими связями анионов, получим графическую формулу соли.
3) В состав соли входит 2 катиона и 3 аниона; расположив катионы и анионы друг под другом, и, соединив свободные химические связи катионов со свободными химическими связями анионов, получим графическую формулу соли.
Пример 1.6 Ba(HCO3)2

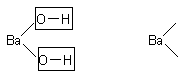
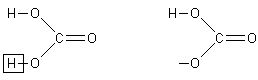 1) Графическая формула аниона получается из графической формулы угольной кислоты, удалением только одного атома водорода (т.к. соль кислая).
1) Графическая формула аниона получается из графической формулы угольной кислоты, удалением только одного атома водорода (т.к. соль кислая).
 2) Графическая формула катиона получается из графической формулы гидроксида бария удалением всех гидроксогрупп (т.к. соль кислая, а не основная).
2) Графическая формула катиона получается из графической формулы гидроксида бария удалением всех гидроксогрупп (т.к. соль кислая, а не основная).
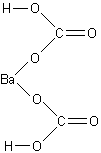 3) В состав соли входит 1 катион и 2 аниона; расположив анионы друг под другом и соединив свободные химические связи катиона со свободными химическими связями анионов, получим графическую формулу соли.
3) В состав соли входит 1 катион и 2 аниона; расположив анионы друг под другом и соединив свободные химические связи катиона со свободными химическими связями анионов, получим графическую формулу соли.
Пример 1.7 (Al(OH)2)3PO4
 1) Графическая формула аниона
1) Графическая формула аниона 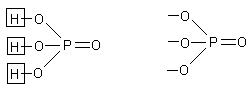 получается из графической формулы фосфорной кислоты, удалением всех атомов водорода (т.к. соль основная, а не кислая).
получается из графической формулы фосфорной кислоты, удалением всех атомов водорода (т.к. соль основная, а не кислая).

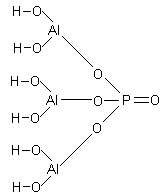
 2) Графическая формула катиона получается из графической формулы гидроксида алюминия удалением только одной гидроксогруппы (т.к. соль основная).
2) Графическая формула катиона получается из графической формулы гидроксида алюминия удалением только одной гидроксогруппы (т.к. соль основная).
3) В состав соли входит 3 катиона и 1 анион; расположив катионы друг под другом и соединив свободные химические связи катионов со свободными химическими связями аниона, получим графическую формулу соли.
Пример 1.8 Написать химические формулы и названия всех солей, которые могут быть образованы гидроксидом алюминия и ортомышьяковой кислотой.
При выполнении этого задания следует учитывать, что в состав любой соли входят анионы кислотного остатка и катионы. Формулы анионов кислотного остатка можно получить, удаляя ионы водорода из молекулы кислоты:
H3AsO4 ® H2AsO4– ® HAsO42– ® AsO43– .
Формулы катионов можно получить, удаляя гидроксогруппы из формулы гидроксида:
Al(OH)3 ® Al(OH)2+ ® AlOH2+ ® Al3+ .
Соединяя формулы катионов с формулами анионов Al3+ и AsO43–; Al3+ и HAsO42–; Al3+ и AsO43–; Al(OH)2+ и AsO43– AlOH2+ и AsO43– (соблюдая при этом правило электронейтральности: число положительных и отрицательных зарядов одинаково), получаем формулы солей:
Al(OH)3 H3AsO4
¯ ¯
(Al(OH)2)3AsO4  основная сольAl(OH)2+ H2AsO4– Al2(HAsO4)3 кислая соль
основная сольAl(OH)2+ H2AsO4– Al2(HAsO4)3 кислая соль
 ¯ ¯
¯ ¯
(AlOH)2(AsO4)3 основная соль 
 AlOH2+ HAsO42– Al(H2AsO4)3 кислая соль
AlOH2+ HAsO42– Al(H2AsO4)3 кислая соль
¯ ¯
 Al3+ AsO43– AlAsO4 средняя соль
Al3+ AsO43– AlAsO4 средняя соль
AlAsO4 – ортоарсенат алюминия
Al2(HAsO4)3 – гидроортоарсенат алюминия;
Al(H2AsO4)3 – дигидроортоарсенат алюминия;
(AlOH)2(AsO4)3 – ортоарсенат гидроксоалюминия
(Al(OH)2)3AsO4 – ортоарсенат дигидроксоалюминия
