Получение и применение этилового спирта.
Предельные одноатомные спирты - это производные алканов, в которых один из атомов водорода заменён на гидроксильную группу 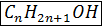 .
.
Гомологический ряд: CH3OH – метанол (метиловый спирт)
C2H5OH – этанол (этиловый спирт)
C3H7OH – пропанол (пропиловый спирт)
C4H9OH – бутанол (бутиловый спирт)
Изомерия:
1. Строение углеродного скелета
2. Положение ОН-группы
Физические и химические свойства определяются строением молекулы спирта, то есть наличием ОН-групп. Атомы кислорода обладают более высокой электроотрицательностью, чем С – О и ОН в сторону атома кислорода, таким образом на атоме кислорода образуется δ–, а на водороде δ+. СН3 → Оδ– ⟵ Нδ+
СН3− Оδ–
Нδ+… Оδ–−СН3
Нδ+
Физические свойства:
Из-за наличия большого количества водородных связей низшие спирты – жидкости и растворимы в воде, высшие (>12 С) нерастворимы и твёрдые. Метанол − наркотическое вещество и очень ядовит!
Химические свойства определяются функциональной группой-ОН:
| Получение |
1) сбраживание сахаристых веществ C6H12O6 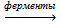 2C2H5OH + 2CO2↑ 2) гидролиз целлюлозы и последующее сбраживание глюкозы; 3) из этилена (гидратация) CH2=CH2 + H2O 2C2H5OH + 2CO2↑ 2) гидролиз целлюлозы и последующее сбраживание глюкозы; 3) из этилена (гидратация) CH2=CH2 + H2O 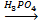 C2H5OH C2H5OH |
| Применение |
| Этанол используют: 1) для производства синтетических каучуков; 2) в качестве растворителей лаков, красок, медикаментов, душистых веществ; 3) для получения уксусной кислоты и различных сложных эфиров; 4) в медицине в качестве дезинфицирующего средства; |
1) с активными металлами
C2H5OH + 2Na → 2C2H5ONa + H2
2) окисление частичное O
C2H5OH + CuO 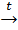 CH3C−H + Cu + H2O
CH3C−H + Cu + H2O
этанол этаналь
3) окисление полное – горение
C2H5OH + 3O2 → 2CO2 + 3H2O + Q
4) реакция дегидратации (отщепление воды)
C2H5OH 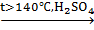 CH2=CH2 + H2O
CH2=CH2 + H2O
этилен
внутримолекулярное отщепление:
C2H5OH + HOC2H5 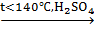 C2H5OC2H5 + H2O
C2H5OC2H5 + H2O
диэтиловый эфир
5) взаимодействие с карбоновыми кислотами
(реакция этерефикации)
O O
CH3−C−OH + HOC2H5 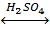 CH3−C−OC2H5 + H2O
CH3−C−OC2H5 + H2O
уксусная кислота этанол этилацетат
Билет №11 (1)
Электрохимический ряд металлов.
Вытеснение металлов из растворов солей другими металлами.
Все металлы по активности расположены в электрохимическом ряду. Его впервые составил Н.Н. Бекетов ещё в XIX веке.
1) Восстановительная активность металлов уменьшается слева направо, а окислительная активность ионов слева направо увеличивается.
2) Металлы, стоящие до водородв вытесняют водород из растворов кислот (кроме азотной кислоты − HNO3).
Fe + 2HCl → FeCl2 + H2
Mg + 2HCl → MgCl2 + H2 – реакция протекает активнее
Mg + 2H+ + 2Cl− → Mg2+ + 2Cl− + H2
3) Более активный металл вытесняет менее активный металл из растворов его солей
Fe + CuSO4 → FeSO4 + Cu
в-ль ок-ль
Fe + Cu2+ + SO42− → Fe2+ + SO42− + Cu
Fe + Cu2+ → Fe2+ + Cu
Fe0 – 2ē → Fe2+ |1
Cu2+ + 2ē → Cu |1
4) Более активный металл вытесняет менее активный металл из его оксида (метод алюминотермии):
6ē
2Al0 + 3Mn2+O 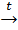 3Mn + Al2O3
3Mn + Al2O3
в-ль ок-ль
Билет №11 (2)
