Реакции полимеризации диенов. Натуральный и синтетический каучуки. Строение, получение и применение их в промышленности
Химические свойства. Для алкадиенов характерны обычные реакции электрофильного присоединения АE, свойственные алкенам. Особенность сопряженных диенов состоит в том, что две двойные связи в их молекулах функционируют как единое целое, поэтому реакции присоединения могут протекать в двух направлениях: а) к одной из двойных связей (1,2-присоединение) или б) в крайние положения сопряженной системы с образованием новой двойной связи в центре системы (1,4-присоединение). Так, присоединение брома к бутадиену может привести к двум продуктам:
| 1,2 | ||
| СН2=СН-СН=СН2 + Вr2 | → | СН2=СН-СНВr-СН2Вr |
или
| 1,4 | ||
| СН2=СН-СН=СН2 + Вr2 | → | ВrСН2-СН=СН-СН2Вr |
Подбор реагентов и условий реакций позволяет направлять присоединение по любому из двух направлений.
Важнейшее свойство диенов — их способность к полимеризации, которая используется для получения синтетических каучуков. При полимеризации бутадиена-1,3, которая протекает как 1,4-присоединение, получают бутадиеновый каучук:
nСН2=СН-СН=СН2 → (-СН2-СН=СН-СН2-)n.
Использование металлоорганических катализаторов в этой реакции позволяет получить каучук с регулярным строением, в котором все звенья цепи имеют цис-конфигурацию. Аналогичная реакция с изопреном дает синтетический изопреновый каучук, который по строению и свойствам близок к природному каучуку:
nСН2=С(СН3)-СН=СН2 → (-СН2-С(СН3)=СН-СН2-)n.
Природный (натуральный) каучук (из гевеи) - полиизопрен (С5Н8)n=1000-3000эластичен. Его молекулы свернуты в цис-положении, разворачиваются и возвращаются при снятии нагрузки, а транс-полимер - гуттаперча - неэластична.
Синтетический каучук- полимер изопрена или бутадиена (по Лебедеву, SU), уступает природному из-за меньшей стереорегулярности, стереорегулярный (с цис-СН2-)- дивиниловый и полиизопреновый каучук близок к природному, износоустойчив.
Каучук - лишь один из изопреноидов формулы (С5Н8)n, включающих биологически активные терпены, каротин, провитамины (А,Д), гормоны, стероиды и другие, в организме получаемых как и жиры, из ацетата 1а Диены определяются как углеводороды с 1- общей формулой СnН2n-2 2- двумя сопряженными связями 3- кратными связями 4- двумя двойными связями.2а Изопрен С5Н8НЕ является 1- основой множества природных соединений 2- сопряженным диеном 3- жидкостью 4- цис-изомером.3а Бутадиен-1,3 при гидрировании дает 1) бутен-1 2) бутен-2 3) бутин-2 4) смесь бутенов.
Строение каучука было доказано методом озонирования (Гарриес). Получение при озонолизе левулинового альдегида подтверждает упорядоченное 1,4-строение:
Строение:
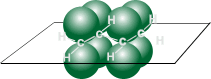
Атомы углерода в молекуле бутадиена-1,3 находятся в sp2 - гибридном состоянии, что означает расположение этих атомов в одной плоскости и наличие у каждого из них одной p - орбитали, занятой одним электроном и расположенной перпендикулярно к упомянутой плоскости.
 a) a) | 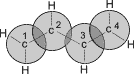 б) б) |
| Схематическое изображение строения молекул бутадиена -1,3 (а) и вид модели сверху (б). Перекрывание электронных облаков между С1–С2 и С3–С4 больше, чем между С2–С3. |
p - Орбитали всех атомов углерода перекрываются друг с другом, т.е. не только между первым и вторым, третьим и четвертым атомами, но и также между вторым и третьим. Отсюда видно, что связь между вторым и третьим атомами углерода не является простой σ - связью, а обладает некоторой плотностью p - электронов, т.е. слабым характером двойной связи. В молекуле отсутствуют в классическом понимании одинарные и двойные связи, а наблюдается делокализация p - электронов, т.е. равномерное распределение p - электронной плотности по всей молекуле с образованием единого p - электронного облака. Взаимодействие двух или нескольких соседних p - связей с образованием единого p - электронного облака, в результате чего происходит передача взаимовлияния атомов в этой системе, называется эффектом сопряжения. Таким образом, молекула бутадиена -1,3 характеризуется системой сопряженных двойных связей.
Такая особенность в строении диеновых углеводородов делает их способными присоединять различные реагенты не только к соседним углеродным атомам (1,2- присоединение), но и к двум концам сопряженной системы (1,4- присоединение) с образованием двойной связи между вторым и третьим углеродными атомами. Отметим, что очень часто продукт 1,4- присоединения является основным.
Получение.Основной промышленный способ получения диенов — дегидрирование алканов. Бутадиен-1,3 (дивинил) получают из бутана:
| t,Сr2О3 | ||
| СН3-СН2-СН2-СН3 | → | СН2=СН-СН=СН2 + 2Н2, |
а изопрен (2-метилбутадиен-1,3) — из 2-метилбутана:
| t, Сr2О3 | ||
| СН3-СН(СН3)-СН2-СН3 | → | СН2=С(СН3)-СН=СН2+2Н2. |
Бутадиен-1,3 можно также получать по реакции Лебедева путем одновременного дегидрирования и дегидратации этанола:
| t, ZnO, Al2O3 | ||
| 2С2Н5ОН | → | СН2=СН-СН=СН2 + Н2 + 2Н2О. |
Применение. Основная область применения алкадиенов - синтез каучуков.
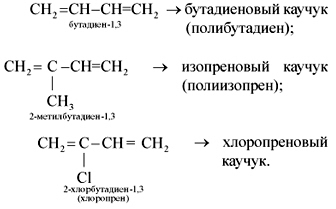
Получение каучуков
Одно дерево бразильской гевеи в среднем, до недавнего времени, было
способно давать лишь 2-3 кг каучука в год; годовая производительность
одного гектара гевеи до Второй Мировой войны составляла 300—400 кг технического каучука. Такие объёмы натурального каучука не удовлетворяли растущие потребности промышленности. Поэтому возникла необходимость получить синтетический каучук. Замена натурального каучука синтетическим даёт огромную экономию труда.
Первый синтетический каучук, был получен по методу С.В. Лебедева из спирта:
2CH3-CH2-OH t=425,ZnO,Al2O3→ CH2=CH-CH=CH2 + H2 + 2H2O
при полимеризации дивинила под действием металлического натрия, представлял собой полимер нерегулярного строения со смешанным типом звеньев 1,2- и 1,4-присоединения:
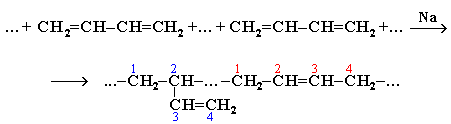
В присутствии органических пероксидов (радикальная полимеризация) также образуется полимер нерегулярного строения со звеньями 1,2- и 1,4- присоединения. Каучуки нерегулярного строения характеризуются невысоким качеством при эксплуатации. Избирательное 1,4-присоединение происходит при использовании металлорганических катализаторов (например, бутиллития C4H9Li, который не только инициирует полимеризацию, но и определенным образом координирует в пространстве присоединяющиеся молекулы диена):

Таким способом получен стереорегулярный 1,4-цис-полиизопрен – синтетический аналог натурального каучука. Данный процесс идет как ионная полимеризация.
Реакция получения каучуков реакцией полимеризации:
nCH2=C-CH=CH2 t,kat → (-CH2-C=CH-CH2-)n
│ │
СH3 CH3
изопрен изопреновый каучук
Реакция получения каучуков реакцией сополимеризации:
CH2=CH-CH=CH2 + CH=CH2 + CH2=CH-CH=CH2 + CH=CH2 + … t,kat →
│ │
C6H5 C6H5
бутадиен стирол
t,kat → [-CH2-CH=CH-CH2 -CH-CH2-]n
│
C6H5
бутадиен-стирольный каучук
Наиболее массовое применение каучуков — это производство резин для автомобильных, авиационных и велосипедных шин.
Из каучуков изготавливаются специальные резины огромного разнообразия уплотнений для целей тепло-, звуко-, воздухо- игидроизоляции разъёмных элементов зданий, в санитарной и вентиляционной технике, в гидравлической, пневматической и вакуумной технике.
Каучуки применяют для электроизоляции, производства медицинских приборов и средств контрацепции.
В ракетной технике синтетические каучуки используются в качестве полимерной основы при изготовлении твёрдого ракетного топлива, в котором они играют роль горючего, а в качестве наполнителя используется порошок селитры (калийной или аммиачной) или перхлората аммония, который в топливе играет роль окислителя.
6. Сопряженные диены. Химические свойства: реакции присоединения, окисления, димеризации, диеновый синтез. Полимеризация.
В сопряженных диенах p-электронные облака двойных связей перекрываются между собой и образуют единое p-электронное облако. В сопряженной системе p-электроны уже не принадлежат определенным связям, они делокализованы по всем атомам, поэтому структуру диенов можно изобразить следующим образом (на примере бутадиена):
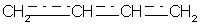
Пунктирные линии показывают область делокализации электронов и обозначают промежуточный порядок связи между С-С и С = С. Цепь сопряжения может включать большое число двойных связей. Чем она длиннее, тем больше делокализация p-электронов и тем устойчивее
Наибольшее значение имеют диеновые углеводороды с сопряжёнными двойными связями, в их молекулах двойные связи разделены одной одинарной связью. Например, дивинил СН2=СН–СН=СН2, изопрен СН2=С(СН3)–СН=СН2 и др.
