Константа и коэффициент распределения
Процесс экстракции почти всегда можно описывать как обычную, хотя и двухфазную, химическую реакцию. Большинство реакций экстракции обратимо, поэтому к экстракционным процессам можно приложить закон действия масс. Константу равновесия реакции экстракции в данном случае называют константой экстракцииК:
К= 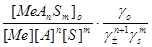 . 8.11
. 8.11
где gо- коэффициент активности Ме в органической фазе; g± - средний моляльный коэффициент активности соли; gs – коэффициент активности экстрагента.
Количественно экстракция характеризуется константой распределения - Кр.Исходя, из равенства химических потенциалов растворенного вещества в органической и водной фазах при равновесии, константа распределения равна:
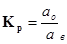 =
= 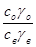 , 8.12
, 8.12
где ао и ав – термодинамические активности растворенного вещества в органической и водной фазах; со и св – его молярные( моляльные) концентрации; 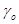 и
и 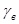 – соответствующие коэффициенты термодинамической активности. Константа распределения, как и всякая другая константа равновесия, зависит лишь от природы вещества и условий равновесия (давления, температуры).
– соответствующие коэффициенты термодинамической активности. Константа распределения, как и всякая другая константа равновесия, зависит лишь от природы вещества и условий равновесия (давления, температуры).
Коэффициент распределения Dхарактеризует распределение вещества между двумя фазами и является отношением концентрации распределяющегося вещества в водной и органической фазах:
D = 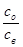 (8.13)
(8.13)
Из (8.12 ) и (8.13) получим:
Кр=D 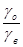 (8.14)
(8.14)
Для идеального раствора (трехкомпонентной системы), в которой нет диссоциации и ассоциации, нет взаимного растворения фаз, а также отсутствует взаимодействие растворенного вещества с растворителем, 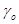 =
= 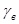 =1 и при постоянном давлении и температуре уравнение (8.14) превращается в следующее:
=1 и при постоянном давлении и температуре уравнение (8.14) превращается в следующее:
Кр = 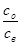 =D (8.15)
=D (8.15)
Избирательность процесса экстракции при разделении данной пары элементов определяется величиной коэффициента разделения R, равной отношению коэффициентов распределения.
Часто используют для количественного описания экстракции фактор извлечения.
R = 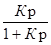 ,
,
при Vв = Vорг эти величины характеризуют эффективность извлечения элемента.
Концентрации радиоактивного элемента в органической и водной фазах пропорциональны объемным удельным активностям элемента в водной и органической фазах:
I уд орг = 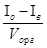 ; Iуд в =
; Iуд в = 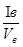 , (8.16)
, (8.16)
где Io – общая радиоактивность активность раствора, тогда
Кр = 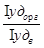 (8.17)
(8.17)
Величина Кр в общем случае зависит не только от свойств экстрагента, но и от многих других факторов: концентрации распределяемого вещества в исходном водном растворе, наличия кислот и солей, природы разбавителя, состава экстрагируемого комплекса и т. д.
Так, при больших концентрациях извлекаемого элемента в водном растворе коэффициент распределения может уменьшаться благодаря насыщению органической фазы.
Состав раствора также существенно влияет на коэффициент распределения. Так, коэффициент распределения возрастает с увеличением концентрации аниона (катиона), вводимого в раствор в форме неэкстрагируемой соли или кислоты. Коэффициент распределения пропорционален коэффициентам активности катиона и аниона в водной фазе, которыеувеличиваются с ростом концентрации посторонней соли. Добавление в водный раствор таких солей и кислот, называемых высаливателями,является удобным практическим приемом увеличения коэффициента распределения. При этом уменьшается активность воды и растет g±..
Значительное влияние на коэффициенты распределения оказывает концентрация водородных ионов в водных растворах. При экстракции кислородсодержащими органическими растворителями это влияние обусловлено участием ионов водорода в образовании экстрагируемого соединения, а также связыванием части экстрагента в соединение с кислотой. Влияние рН раствора на коэффициенты распределения особенно существенно при экстракции внутрикомплексных соединений.
Помимо перечисленных факторов, практическое значение имеет и присутствие в водном растворе посторонних ионов, не входящих в состав экстрагируемого соединения, но способных, например, участвовать в образовании комплексных соединений с катионом экстрагируемого металла. Эффективность влияния этих посторонних ионов определяется константами устойчивости соответствующих комплексных соединений. Это обстоятельство часто используют в экстракционных процессах для разделения элементов путем связывания элемента, от которого необходимо освободиться, в неэкстрагируемое комплексное соединение.
Одной из наиболее важных характеристик процесса распределения элемента между двумя несмешивающимися фазами является его зависимость от состава и природы органической фазы.
В качестве экстрагентов применяют различные кислородсодержащие органические растворители, такие как эфиры, кетоны, спирты. Однако в настоящее время большое значение приобрели фосфороорганические соединения и амины с высокой молекулярной массой.
Выбор экстрагента для промышленного применения, кроме того, определяется его химической и радиационной устойчивостью, вязкостью, воспламеняемостью, растворимостью в воде, токсичностью и стоимостью. В последнее время в экстракционной практике начинают использовать системы на основе водорастворимых полимеров и неорганических солей в качестве высаливателей. Эти системы нетоксичны и сравнительно дешевы. В настоящее время они только изучаются.
