Дайте определение аминам. Первичные, вторичные и третичные амины. Химические свойства аминов.
АМИНЫ– класс соединений, представляющий собой органические производные аммиака, в котором один, два или три атома водорода замещены органическими группами. Отличительный признак – наличие фрагмента R–N<, где R – органическая группа.
Классификация аминов разнообразна и определяется тем, какой признак строения взят за основу.
В зависимости от числа органических групп, связанных с атомом азота, различают:
первичные амины – одна органическая группа у азота RNH2
вторичные амины – две органических группы у азота R2NH, органические группы могут быть различными R'R"NH
третичные амины – три органических группы у азота R3N или R'R"R"'N
По типу органической группы, связанной с азотом, различают алифатические СH3 – N< и ароматические С6H5 – N< амины, возможны и смешанные варианты.
По числу аминогрупп в молекуле амины делят на моноамины СH3 – NН2, диамины H2N(СH2)2NН2, триамины и т.д.
Химические свойства аминов.Отличительная способность аминов – присоединять нейтральные молекулы (например, галогеноводороды HHal, с образованием органоаммониевых солей, подобных аммонийным солям в неорганической химии. Для образования новой связи азот предоставляет неподеленную электронную пару, исполняя роль донора. Участвующий в образовании связи протон Н+ (от галогеноводорода) играет роль акцептора (приемника), такую связь называют донорно-акцепторной (рис. 1). Возникшая ковалентная связь N–H полностью эквивалентна имеющимся в амине связям 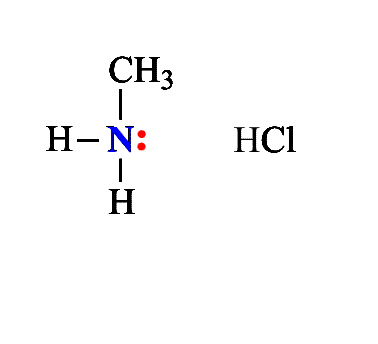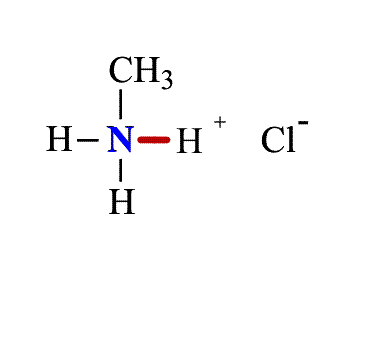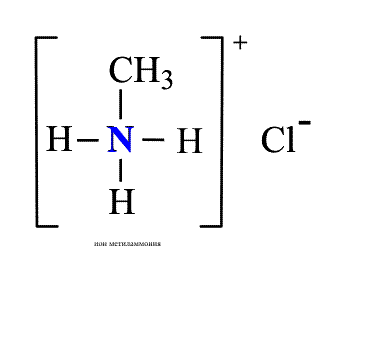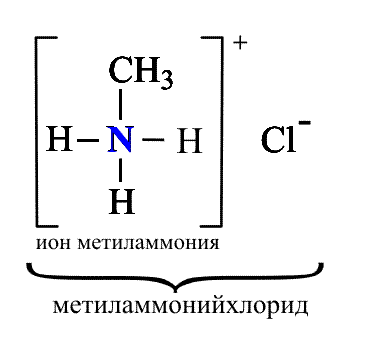
Третичные амины также присоединяют HCl, но при нагревании полученной соли в растворе кислоты она распадается, при этом R отщепляется от атома N:
(C2H5)3N + HCl [(C2H5)3NH]Сl
[(C2H5)3NH]Сl (C2H5)2NH + C2H5Сl
При сравнении этих двух реакций видно, что C2H5-группа и Н, как бы меняются местами, в итоге из третичного амина образуется вторичный.
Растворяясь в воде, амины по такой же схеме захватывают протон, в результате в растворе появляются ионы ОН–, что соответствует образованию щелочной среды, ее можно обнаружить с помощью обычных индикаторов.
C2H5NH2 + H2O [C2H5NH3]+ + OH–
С образованием донорно-акцепторной связи амины могут присоединять не только HCl, но и галогеналкилы RCl, при этом образуется новая связь N–R, которая также эквивалентна уже имеющимся. Если в качестве исходного взять третичный амин, то получается соль тетраалкиламмония (четыре группы R у одного атома N):
(C2H5)3N + C2H5I [(C2H5)4N]I
Эти соли, растворяясь в воде и некоторых органических растворителях, диссоциируют (распадаются), образуя ионы:
[(C2H5)4N]I [(C2H5)4N]+ + I–
Такие растворы, как и все растворы, содержащие ионы, проводят электрический ток. В тетраалкиламмониевых солях можно заменить галоген НО-группой:
[(CH3)4N]Cl + AgOH [(CH3)4N]OH + AgCl
Получающийся гидроксид тетраметиламмония представляет собой сильное основание, по свойствам близкое к щелочам.
Первичные и вторичные амины взаимодействуют с азотистой кислотой HON=O, однако реагируют они различным образом. Из первичных аминов образуются первичные спирты:
C2H5NH2 + HNO2 C2H5OH + N2 +H2O
В отличие от первичных, вторичные амины образуют с азотистой кислотой желтые, трудно растворимые нитрозамины – соединения, содержащие фрагмент >N–N = O:
(C2H5)2NH + HNO2 (C2H5)2N–N=O + H2O
Третичные амины при обычной температуре с азотистой кислотой не реагируют, таким образом, азотистая кислота является реагентом, позволяющим различить первичные, вторичные и третичные амины.
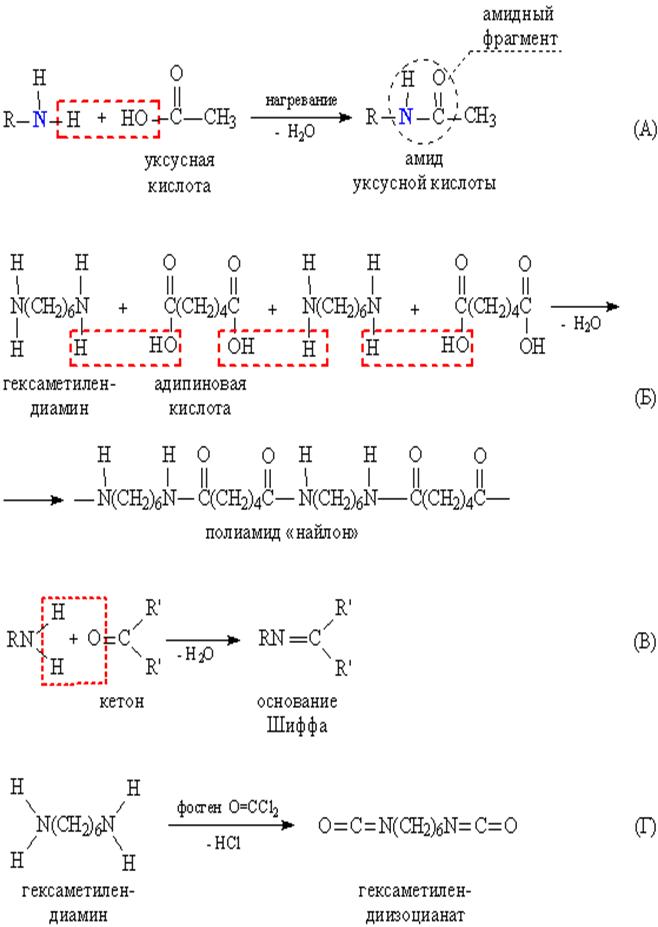
При конденсации аминов с карбоновыми кислотами образуются амиды кислот – соединения с фрагментом –С(О)N< (рис. 2А). Если в качестве исходных соединений взять диамин и дикарбоновую кислоту (соединения, содержащие соответственно две амино- и две карбоксильные группы, соответственно), то они взаимодействуют по такой же схеме, но поскольку каждое соединение содержит две реагирующие группы, то образуется полимерная цепь, содержащая амидные группы (рис. 2Б). Такие полимеры называют полиамидами.
Конденсация аминов с альдегидами и кетонами приводит к образованию так называемых оснований Шиффа – соединений, содержащих фрагмент –N=C< (рис. 2В). На схеме В видно, что для образования двойной связи между N и С азот должен предоставить два атома Н (для образования конденсационной воды), следовательно, в такой реакции могут участвовать только первичные амины RNH2.
При взаимодействии первичных аминов с фосгеном Cl2С=O образуются соединения с группировкой –N=C=O, называемые изоцианатами (рис. 2Г, получение соединения с двумя изоцианатными группами).
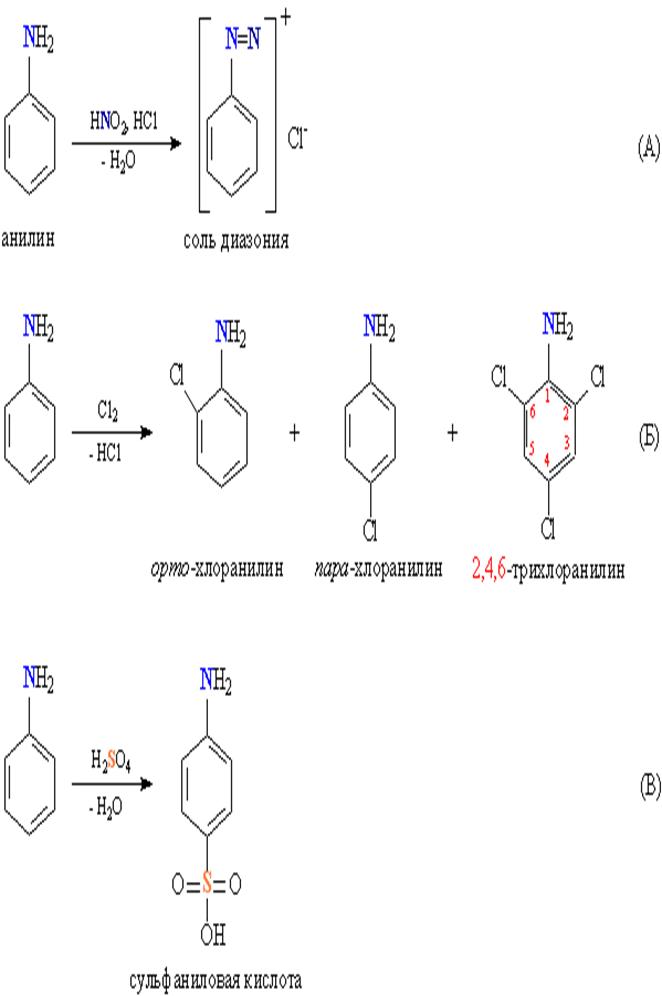
Среди ароматических аминов наиболее известен анилин (фениламин) С6Н5NH2. По свойствам он близок к алифатическим аминам, но его основность выражена слабее – в водных растворах он не образует щелочную среду. Как и алифатические амины, с сильными минеральными кислотами он может образовывать аммониевые соли [С6Н5NH3]+Сl–. При взаимодействии анилина с азотистой кислотой (в присутствии HCl) образуется диазосоединение, содержащее фрагмент R–N=N, оно получается в виде ионной соли, называемой солью диазония (рис. 3А). Таким образом, взаимодействие с азотистой кислотой идет не так, как в случае алифатических аминов. Бензольное ядро в анилине обладает реакционной способностью, характерной для ароматических соединений (см. АРОМАТИЧНОСТЬ), при галогенировании атомы водорода в орто- и пара-положениях к аминогруппе замещаются, получаются хлоранилины с различной степенью замещения (рис. 3Б). Действие серной кислоты приводит к сульфированию в пара-положение к аминогруппе, образуется так называемая сульфаниловая кислота (рис. 3В).