Где f - фрикционный коэффициент , v – скорость движения молекулы.
Фрикционный коэффициент макромолекул зависит от их формы и размеров. Для молекул сферической формы (например, для глобулярных белков, ) f = 6 ηπr
Тогда, сила сопротивления при дфижении сферических макромолекл в жидкости выражается законом Стокса
F = - 6 ηπr v
На поведение макромолекул в растворе основное влияние оказывают столкновение с молекулами растворителя. Подсчитано, молекула белка средних размеров в разбавленном растворе испытывает 1013 - 1015 столкновений в секунду, обусловленные тепловыми движениями. Это определяет статистическое поведение макромолекул- хаотичность движения (броуновское движение).
Согласно законам статистической физики, параметром, описывающим хаотическое движение молекул, является среднеквадратичное смещение х־2
х־2 = 2 К0ТΔ t/ f
где – время наблюдения за хаотическим движением макромолекул. Таким образом, измерив х־2 можно определить значение f,следовательно, и размеры макромолекулы. Однако, невозможно следить за поведением отдельной молекулы, и следовательно, невозможно прямо определить значениех־2.Поэтому определение значений х־2 и f проводят косвенными способами. Один из таких способов – это определение коэффициента диффузии D. Диффузия – это самопроизвольное перемещение молекул из области с высокой концентрацией в область с низкой концентрацией в результате хаотического движения. Поток вещества ( количество молекул в единицу времени) при поступательной диффузии описывается первым законом Фика:
dn/dt = - DAdc/dx,
где n – число молекул; А – площадь перемещения; с – концентрация вещества; D - коэффициент диффузии (м2 с-1). Знак минус означает, что поток направлен в сторону уменьшения концентрации вещества.
Коэффициент диффузии связан с х־2 и f следующей формулой :
D = х־2 / 2 Δ t = К0Т/ f
Таким образом, измерив D можно вычислить значение f и, соответственно, можно сделать заключение о форме макромолекулы.
Для сферических макромолекул радиусом r f = 6 ηπr = К0Т/ D,
тогдаr = К0Т/ 6 ηπ D.
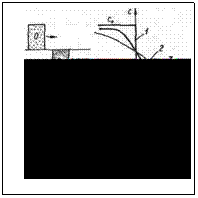
Рис. 5. Измерение коэффициента диффузии макромолекул:
a - диффузия макромолекул на границе раздела раствор-растворитель; б - изменение во времени концентрации (с) макромолекул и градиента концентраций 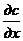 границе раздела раствор–растворитель; 1 – t = 0; 2 – t2; 3– t2; H – высота пика
границе раздела раствор–растворитель; 1 – t = 0; 2 – t2; 3– t2; H – высота пика
Отсюда следует, что для сферических макромолекул молекулярная масса обратно пропорциональна коэффициенту диффузии в кубе:
М ~1/D3
Величину Dможно определить экспериментально. Для этого растворитель наслаивают на концентрированный раствор макромолекул и измеряют размывание границы между растворителем и раствором. Размывание границы можно регистрировать оптическими методами: по измерению оптической плотности в УФ- области; по измерению показателя преломления растворов.
Таблица 1
Зависимость физических параметров от молекулярной массы белков (константа седиментации 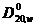 , коэффициент диффузии
, коэффициент диффузии 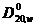 , парциальный удельный объем V и молекулярная масса М
, парциальный удельный объем V и молекулярная масса М
| Белок | S0 1013, с | 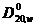 1011, м2 ·с-1 1011, м2 ·с-1 | V, л·кг-1 | М, кДа |
| Цитохром с1 | 1,71 | 11,40 | 0,728 | 13,3 |
| Лизоцим | 1,91 | 11,20 | 0,703 | 13,9 |
| Рибонуклеаза | 2,00 | 13,10 | 0,707 | 12,6 |
| Миоглобин | 2,04 | 11,3 | 0,74 | 16,9 |
| Сывороточный альбумин | 4,60 | 6,10 | 0,733 | 68,45 |
| Каталаза печени | 11,2 | 4,10 | 0,735 | 250,0 |
| Уреаза | 18,6 | 3,46 | 0,73 | 480,0 |
| Гемоцианин | 98,9 | 1,38 | 0,738 | 6,6·103 |
Установленную экспериментальным путем величину коэффициента диффузии обычно приводят к стандартным условиям (бесконечное разбавление в воде w, при 293 К) По формуле
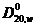 =
= 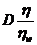 .
.
В таблице 1 приведены некоторые физические параметры ряда белков с разными молекулярными массами, с различными формами и размерами молекул. Как видно из таблицы, соотношение М ~1/D3, полученный для сферических макромолекул не всегда выполняется. Например, при увеличении молекулярной массы белка в 450 раз (сравниваем гемоцианин с цитохромом с1) коэффициент диффузии уменьшается всего в 9 раз. Это свидетельствует о том, что коэффициент Dзависит не только от массы молекул, но и от их формы.
