Основы биоорганической химии
О.А. Журавская
ОСНОВЫ БИООРГАНИЧЕСКОЙ ХИМИИ
Учебно-методическое пособие
для студентов медицинских вузов
Самара 2010
УДК
Ж 91
Рецензенты:
– кандидат химических наук, доцент А.А. Данилин;
– кандидат химических наук, доцент О.К. Шаховкина.
Журавская О.А. Основы биоорганической химии:Учебно-методическое пособие для студентов медицинских вузов. – Самара, НОУ ВПО «Самарский медицинский институт «РеаВиЗ», 2010 − 52 с.
Изучение биоорганической химии в медицинских вузах связано с усвоением большого объема материала при малом количестве аудиторных часов.
В учебном пособии изложены ключевые моменты биоорганической химии, материал представлен в текстуальной форме, таблицах, схемах и рисунках, что позволяет оптимизировать процесс запоминания.
Пособие предназначено для студентов медицинских вузов, обучающихся по специальностям «Лечебное дело» и «Стоматология» очной и очно-заочной формы обучения.
© НОУ ВПО СМИ «РеаВиЗ», 2010
Раздел 1. Основы строения и факторы, определяющие реакционную способность органических соединений
1.1. Введение в биоорганическую химию.
Основные понятия и термины
Биоорганическая химия изучает строение и свойства веществ, участвующих в процессах жизнедеятельности, в непосредственной связи с познанием их биологических функций.
 Объекты биоорганической химии
Объекты биоорганической химии
| Биополимеры | Биорегуляторы − |
| (их структурные компоненты) – Высокомолекулярные природные соединения, служащие структурной основой живых организмов (пептиды, белки, углеводы, нуклеиновые кислоты, липиды). | Соединения, регулирующие обмен веществ (витамины, гормоны, синтетические БАВ, лекарственные средства). |
Некоторые понятия и термины
Метаболизм (обмен веществ) – совокупность химических реакций, протекающих в организме; дает энергию и вещества, необходимые для функционирования организма.
Катаболизм – реакции распада (выделение энергии, окисление [O]).
Анаболизм – реакции биосинтеза (затрата энергии, восстановление [H]).
Биосинтез – химические реакции, приводящие в условиях организма к получению конкретного класса соединений.
Для обозначения химического процесса, протекающего вне организма используется латинское название – in vitro, внутри организма – in vivo.
Ациклические углеводороды
Алканы – ациклические углеводороды, содержащие максимальное количество атомов водорода. Первые четыре представителя имеют полусистематические названия – метан, этан, пропан, бутан. Остальные алканы называют с помощью корня соответствующего греческого числительного с добавлением суффикса – ан:
| n | CnH2n+2 | n | CnH2n+2 |
| CH4 - метан | C12H26 - додекан | ||
| C2H6 - этан | C15H32 - пентадекан | ||
| C3H8 - пропан | C18H38 - октадекан | ||
| C4H10 - бутан | C20H42 - эйкозан | ||
| C5H12 - пентан | C21H44 - генэйкозан | ||
| C6H14 - гексан | C28H58 - октакозан | ||
| C7H16 - гептан | C30H62 - триаконтан | ||
| C8H18 - октан | |||
| C9H20 - нонан | |||
| C10H22 - декан |
Одновалентные радикалы, производимые от насыщенных ациклических углеводородов, называют путем замены окончания –ан на –ил:
CH3 – метил-
C2H5 – этил-
CH3–CH2–CH2 – пропил-
H3  C
C
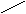 CH– изопропил-
CH– изопропил-
H3C
CH3–CH2–CH–CH3 – втор-бутил-
|
H3  C
C
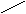 CH– CH2– изобутил- и т.д.
CH– CH2– изобутил- и т.д.
H3C
Наиболее длинная С-цепь (родоначальная структура) нумеруется так, чтобы номера были наименьшими:
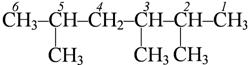 2,3,5 – триметилпентан 2,3,5 – триметилпентан | 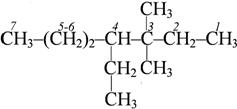 3,3 – диметил – 4 – этилгептан 3,3 – диметил – 4 – этилгептан |
Непредельные ациклические углеводороды содержат кратные связи, наличие которых обозначают путем замены суффикса -ан на -ен(при двойной связи С=С), на -ин (при тройной связи С≡С).
Соединения, имеющие как двойные, так и тройные связи, получают названия путем замены суффикса –ан в названии соответствующего алкана на -енин, -адиенин, -атриенин, -ендин и т.п. Кратным связям должны соответствовать низкие цифровые обозначения, а двойным связям присваивают наименование номера:
|
| ||
|
Одновалентные радикалы непредельных ациклических углеводородов:
CH2=CH– винил-
CH2=CH–CH2– аллил-
HC≡C– этенил
Циклопропан
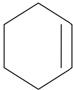 циклогексен циклогексен |
Одновалентные радикалы, образованные из циклоалканов, называют, заменяя суффикс –ан на –ил. Атом углерода, несущий свободную валентность, обозначают номером 1.
 циклопропил- циклобутил- циклопентил- циклопропил- циклобутил- циклопентил- |
Моноциклические и полициклические ароматические углеводороды (арены) имеют тривиальные названия, использование которых разрешено правилами ИЮПАК:
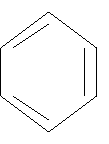 бензол бензол | CH3 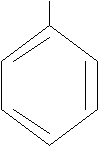 толуол толуол | 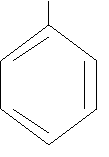 CH3 ксилол CH3 ксилол | 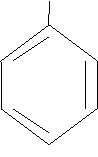 CH=CH2 стирол CH=CH2 стирол |
Прочие моноциклические ароматические углеводороды называют как производные бензола. Положения заместителей указывают цифрами, за исключением случаев, когда при наличии двух заместителей вместо
1,2-; 1,3- и 1,4- могут быть использованы обозначения о- (орто-); м- (мета-); п- (пара-) соответственно:
CH3 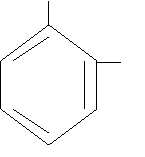 CH3 1,2 – диметилбензол (о-ксилол) CH3 1,2 – диметилбензол (о-ксилол) | 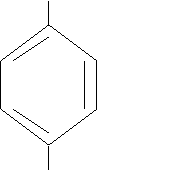 CH=CH2 CH2–CH3 4-этилстирол (п-этилстирол) CH=CH2 CH2–CH3 4-этилстирол (п-этилстирол) |
Одновалентные радикалы моноциклических ароматических углеводородов:
|
| ||
|
| ||
| и т.д. |
Спирты и фенолы
При назывании спиртов по заместительной номенклатуре группа –OH рассматривается как главная и обозначается суффиксом –ол (-диол, -триол, -тетраол и т.д.), нумерация осуществляется с таким расчетом, чтобы группа –OH получила меньший номер:
|
|
|
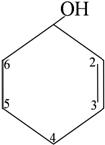 циклогексен-2-ол-1 циклогексен-2-ол-1 |
Для некоторых спиртов сохранены тривиальные названия:
CH2=CH–CH2OH - аллиловый спирт
C6H5–CH2OH - бензиловый спирт
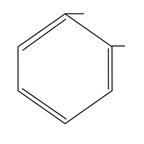 OH CH2OH - салициловый спирт OH CH2OH - салициловый спирт |
CH2 (OH)–CH2OH - этиленгликоль
CH2 (OH) – CH (OH)–CH2OH - глицерин
Для простых фенолов сохранены тривиальные названия:
OH 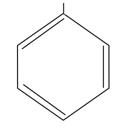 фенол фенол | OH 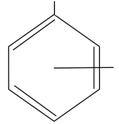 CH3 о- ,м-, н-крезолы CH3 о- ,м-, н-крезолы | CH3 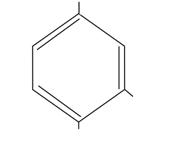 OH OH 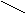 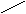 CH CH3 CH3 тимол CH CH3 CH3 тимол |
OH 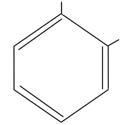 OH пирокатехин OH пирокатехин | OH 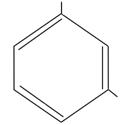 OH резорцин OH резорцин | OH 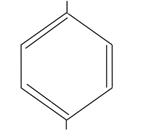 OH гидрохинон OH гидрохинон |
OH 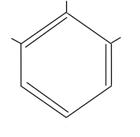 HO OH пирогаллол HO OH пирогаллол | OH 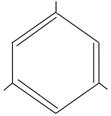 HO OH флороглюцин HO OH флороглюцин |
Карбоновые кислоты
Карбоксильная группа в молекулах алифатических кислот должна получать наименьший номер и обозначается она суффиксом –овая кислота:
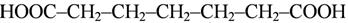 гептандиовая кислота гептандиовая кислота |
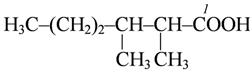 2,3-диметилгексановая кислота 2,3-диметилгексановая кислота |
Если группа –COOH рассматривается как заместитель (и не входит в родоначальную структуру), то она получает название –карбоновая кислота:
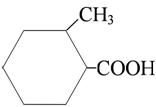 2-метилциклогексанкарбоновая кислота 2-метилциклогексанкарбоновая кислота |
Карбоксигруппу обозначают приставкой карбокси- если в соединении присутствует другая группа, имеющая преимущество в перечислении:
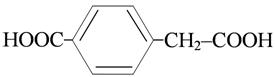 п-карбоксифенилуксусная кислота п-карбоксифенилуксусная кислота |
1.3. Электронное строение органических соединений
В составе органических соединений чаще всего находят следующие элементы: C, O, H, N, S, P, которые получили название элементов – органогенов.
Электронное состояние углерода (невозбужденное) – 1S2 2S2 2P2, при переходе в возбужденное состояние - 1S2 2S1 2P3.
Интерес представляют S и P орбитали, поскольку валентные электроны углерода и элементов-органогенов находятся на них.
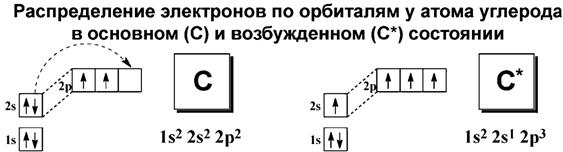
Гибридизация орбиталей – смешение нескольких атомных орбиталей различной формы и близкой энергии с образованием такого же числа новых гибридных орбиталей, расположение которых в пространстве соответствует геометрии молекулы. Гибридные орбитали за счет более эффективного перекрывания образуют более прочные связи по сравнению с негибридными.
В органических соединениях углерод может находиться в одном из трех валентных состояний:
I валентное состояние – sp3-гибридизация, при которой происходит смешивание I S и 3 p-орбиталей, с возникновением 4-х гибридизованных орбиталей, расположенных в пространстве под углом 109º28´ по отношению друг к другу. Углерод в таком состоянии получил название тетрагонального атома углерода и встречается в предельных органических соединениях.
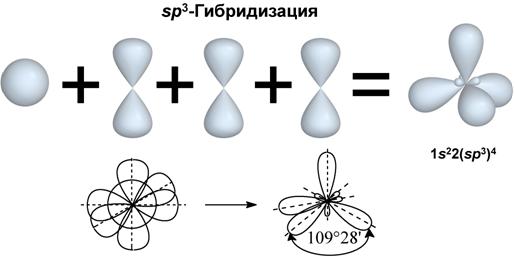
sp3-гибридные орбитали направлены в пространстве к вершинам тетраэдра (тетраэдрическая конфигурация).
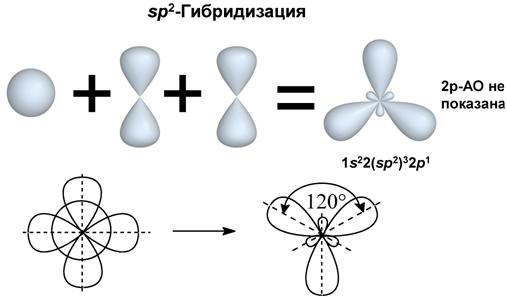
II валентное состояние – sp2-гибридизация, при которой происходит смешивание I S и 2 p-орбиталей, с возникновением 3-х гибридизованных орбиталей, расположенных в одной плоскости под углом 120º по отношению друг к другу. Негибридизованная p-орбиталь расположена перпендикулярно плоскости гибридизованных орбиталей. Углерод в таком состоянии называют тригональным и встречается он в соединениях с двойными связями (атом C в алкенах, карбонильной и карбоксильной группах).
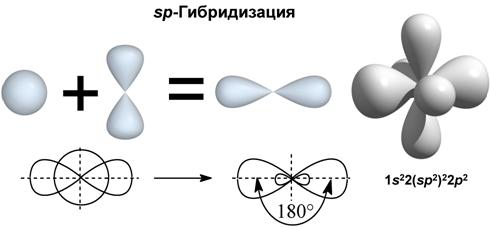
III валентное состояние – sp-гибридизация, при которой происходит смешивание I S и 1p-орбитали с возникновением 2-х гибридизованых орбиталей, расположенных в пространстве под углом 180º (линейно), а две негибридизованые p-орбитали расположены взаимно перпендикулярно друг другу. Sp-гибридизация характерна для углерода, связанного тройной связью или двумя двойными связями.
Если углерод образует одну углерод-углеродную связь, то его называют первичным, если две углерод-углеродные связи − то вторичным; если три углерод-углеродные связи – то третичным; если четыре углерод-углеродные связи – то четвертичным.
Например:
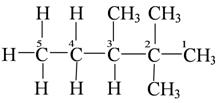 |
1-й и 5-й углероды – первичные; 4-й – вторичный; 3-й – третичный;
2-ой – четвертичный.
Кратные связи
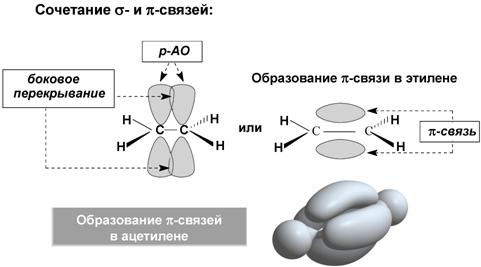
Сопряжение
Молекулы с чередующимися двойными π и простыми σ связями называют сопряженными системами.
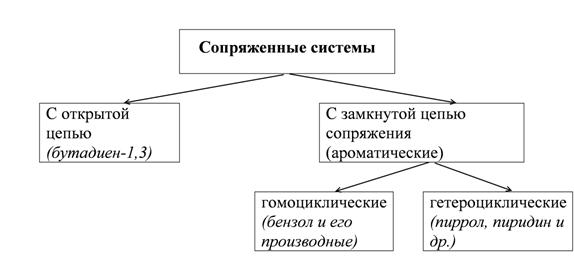
Сопряжение – это перераспределение электронной плотности в системе π – связей, приводящее к стабилизации молекулы.
Энергия сопряжения – это уменьшение энергии молекулы благодаря сопряжению.
Открытые системы сопряжения
Бутадиен-1,3, каждый из четырех углеродов в состоянии sp2-гибридизации, у каждого углерода – по одной свободной p-орбитали. В результате бокового перекрывания орбиталей происходит сопряжение двух локализованных двойных связей с образованием делокализованной четырехцентровой молекулярной орбитали. Этот вид сопряжения называют π-π-сопряжение. Есопряж. = 250 кДж/моль – 235 кДж/моль = 15 кДж/моль. Наблюдается выравненность электронных плотностей в результате делокализации электронов, создание единого электронного облака.
Делокализация электронов в циклических соединениях приводит к возникновению ароматических систем.
Правила ароматичности.
1. Наличие плоского цикла (кольца), состоящего из sp2-гибридизованных атомов, образующих σ-скелет (молекула копланарна).
2. Делокализация электронов, приводящая к образованию единого электронного облака (π-секстет).
3. Подчинение правилу Э. Хюккеля, т.е. электронное облако должно насчитывать (4n+2) π-электронов, где n=1,2,3,4…
4. Высокая степень термодинамической устойчивости (энергия сопряжения).
Гомоциклические ароматические системы.
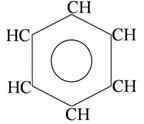 бензол n=1 6ē делокализовано в π- секстет бензол n=1 6ē делокализовано в π- секстет | 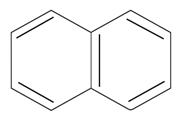 нафталин n=2 10ē делокализовано нафталин n=2 10ē делокализовано | |
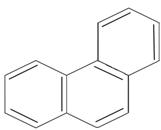 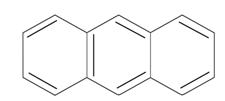 антрацен фенантрен n=3 14ē делокализовано антрацен фенантрен n=3 14ē делокализовано |
Виды изомерии
| структурная | пространственная | |
| · цепи (скелета) · положения заместителей или кратных связей · взаимного расположения заместителей в кольце · межклассовая | · геометрическая · оптическая (стереоизомерия) · поворотная |
Пространственная изомерия
· геометрическая – обусловлена различным расположением заместителей вокруг двойных связей или относительно плоскости циклов).
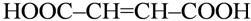   бутен-2-диовая кислота бутен-2-диовая кислота |
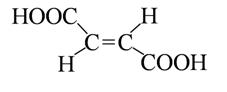 транс-форма (фумаровая кислота) транс-форма (фумаровая кислота) |
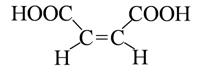 цис-форма (малеиновая кислота) цис-форма (малеиновая кислота) |
Это конфигурационные изомеры, которые не могут быть превращены друг в друга без разрыва ковалентных связей.
· Оптическая изомерия
Стереоизомерия связана с различным расположением в пространстве атомов и атомных групп вокруг асимметрического углеродного атома.
Асимметрический атом углерода – это углерод, все четыре валентности которого замещены различными заместителями.
Хиральность – свойство предмета быть неидентичным своему зеркальному отображению (от греч. cheir – рука). Молекулы тоже могут быть хиральными и ахиральными.
Простейший случай хиральности – наличие в молекуле центра хиральности, которым является асимметрический атом углерода.
Вследствие хиральности некоторые молекулы существуют в виде пары стереоизомеров – энантиомеров.
Энантиомеры – это стереоизомеры, относящиеся друг к другу как предмет и его зеркальное отражение, различные по абсолютной и относительной конфигурации, биологическим свойствам, но обладающие одинаковыми физическими и химическими свойствами.
Гомолиз связи
v Образующиеся промежуточные частицы – свободные радикалы
Гетеролитический (ионный)

Гетеролиз связи
v Образующиеся органические промежуточные частицы
- карбокатионы (с положительным зарядом на атоме углерода) или
- карбоанионы (с отрицательным зарядом на атоме углерода)
Классификация реакций
1. По характеру изменения связей в субстрате и реагенте
(а) Гомолитические реакции
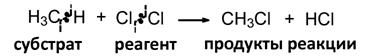
(б) Гетеролитические реакции
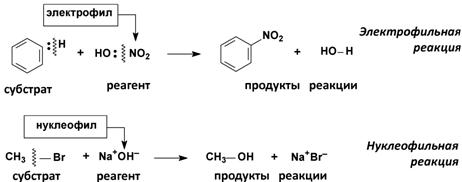
2. По направлению (конечному результату)
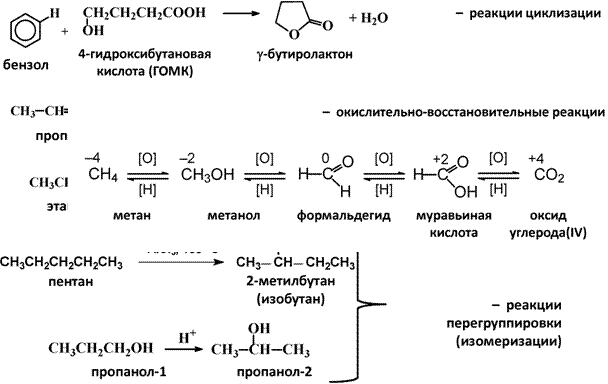 |
v Изменение степени окисления углерода, выступающего в роли
реакционного центра
3. По числу молекул (частиц), участвующих в стадии, определяющей общую скорость реакции
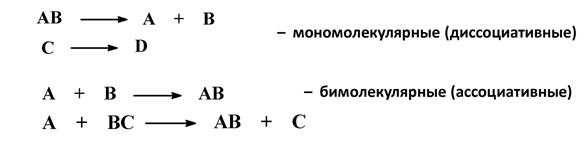
Методики выполнения общих качественных реакций
на функциональные группы
Бромирование бромной водой
В пробирку поместите 2 капли бромной воды, добавьте 2–3 капли исследуемого раствора, встряхните пробирку.
Внешние признаки:
Наблюдается обесцвечивание желтого раствора бромной воды.
2. Реакция гидроксилирования (реакция Вагнера)
В пробирку поместите 2 капли 0,1н KMnO4, добавьте 2–3 капли исследуемого раствора, встряхните пробирку.
Внешние признаки:
Наблюдается обесцвечивание розового раствора KMnO4 и выпадение бурого осадка MnO2.
Углеводы. Моносахариды.
40. Классификация, биологическая роль углеводов. Моносахариды. Стереоизомерия моносахаридов. D- и L-ряды, формулы Фишера. Энантиомерия, диастереомерия, эпимерия. Структура важнейших представителей пентоз и гексоз, производных моносахаридов: дезоксисахаров, аминосахаров.
41. Цикло-оксо (окси- оксо-) − таутомерия моносахаридов. На примере D-глюкозы и D-фруктозы формулы Хеуорса (пиранозы, фуранозы). Аномерия. Конформации моносахаридов, наиболее устойчивые конформации гексоз.
42. Реакционные центры ациклических и циклических форм моносахаридов, нуклеофильное замещение у аномерного центра в циклических формах моносахаридов. Механизм SN. O- и N- гликозиды. Гидролиз гликозидов.
43. Реакции нуклеофильных центров моносахаридов: алкилирование и ацилирование. Гидролиз продуктов. Значение реакций для структурных исследований. Биологически важные фосфаты моносахаридов.
44. Окисление моносахаридов, в кислой нейтральной и щелочной средах, восстановительные свойства альдоз. Гликоновые, гликаровые, гликуроновые кислоты. Реакция эпимеризации моносахаридов, ендиольная форма. Восстановление моносахаридов в глициты (ксилит, сорбит, маннит).
Природные a-аминокислоты.
49. Классификация, стереохимия и строение природных a-аминокислот. Структура природных аминокислот: гидрофобных, гидрофильных, отрицательно и положительно заряженных.
50. Биосинтетические пути образования a-аминокислот из кетонокислот, реакции восстановительного аминирования и переаминирования. Пиридоксалевый катализ. Незаменимые аминокислоты.
51. Кислотно-основные свойства аминокислот, биполярный ион, ионные формы аминокислот в растворах, в зависимости от значения рН, изоэлектрическая точка. (Примеры).
52. Характерные и качественные реакции аминокислот, образование внутрикомплексных солей, нингидриновая, ксантопротеиновая реакции.
53. Реакции, лежащие в основе количественного анализа аминокислот: образование сложных эфиров, реакции с азотистой кислотой, формальдегидом, фенилизотиоцианатом. Реакционные центры, вступающие во взаимодействие, тип и механизм реакции.
54. Метаболизм аминокислот в организме: декарбоксилирование и переход к биогенным аминам, неокислительное и окислительное дезаминирование, трансаминирование. Реакции гидроксилирования.
Омыляемые липиды.
66. Классификация липидов, их биологическое значение. Простые липиды. Нейтральные жиры. Насыщенные и ненасыщенные природные высшие жирные кислоты, входящие в состав липидов. Особенности ненасыщенных жирных кислот. b-окисление высших жирных кислот.
67. Реакционные центры и свойства омыляемых простых и сложных липидов. Щелочной и кислотный гидролиз, реакции присоединения, окисления.
68. Сложные липиды. Фосфолипиды. Глицерофосфолипиды: фосфатидовая кислота, фосфатидилхолины, фосфатидилсерины. Сфингомиелины. Липидный бислой в структуре биологических мембран.
69. Пероксидное окисление фрагментов ненасыщенных жирных кислот в клеточных мембранах, его механизм. Роль пероксидного окисления липидов мембран в действии малых доз радиации на организм. Системы антиоксидантной защиты.
70. Сложные липиды. Гликолипиды: цереброзиды, ганглиозиды, их строение. Свойства, биологическая роль.
Библиографический список
1. Грандберг И. И. Органическая химия: учебник для студентов, обучающихся по агрохимическим специальностям. – М.: Дрофа, 2002. - 672 с.
2. Зурабян С. Е. Основы органической химии. М.: Дрофа, 2006. - 576 с.
3. Оганесян Э. Т. Важнейшие понятия и термины химии: справочное пособие. – М.: Высшая школа, 1993. - 352 с.
4. Проскурина И. К. Биохимия: учебное пособие для студентов высших учебных заведений. – М.: Издательство Владос-Пресс, 2004. - 70 с.
5. Солдатенков А. Т. Основы органической химии лекарственных веществ. М.: Мир; БИНОМ. Лаборатория занятий, 2007. - 191 с.
6. Сорочинская Е. И. Биоорганическая химия. Поли- и гетерофункциональные соединения. Биополимеры и их структурные компоненты. Учебное пособие. – СПб.: Издательство С.Петербургского университета, 1998. - 148 с.
7. Сорочинская Е. И. Биоорганическая химия. Биологически важные классы соединений. Учебное пособие. – СПб: Издательство С.Петербургского университета. - 1998.
8. Тюкавкина Н. А. Биоорганическая химия: учебник для вузов. – М.: Дрофа, 2005. – 542 с.
9. Тюкавкина Н. А. Органическая химия. – м.: Дрофа, 2003. – Кн.1: Основной курс. – 640 с.
О.А. Журавская
ОСНОВЫ БИООРГАНИЧЕСКОЙ ХИМИИ
Учебно-методическое пособие
для студентов медицинских вузов
Самара 2010
УДК
Ж 91
Рецензенты:
– кандидат химических наук, доцент А.А. Данилин;
– кандидат химических наук, доцент О.К. Шаховкина.
Журавская О.А. Основы биоорганической химии:Учебно-методическое пособие для студентов медицинских вузов. – Самара, НОУ ВПО «Самарский медицинский институт «РеаВиЗ», 2010 − 52 с.
Изучение биоорганической химии в медицинских вузах связано с усвоением большого объема материала при малом количестве аудиторных часов.
В учебном пособии изложены ключевые моменты биоорганической химии, материал представлен в текстуальной форме, таблицах, схемах и рисунках, что позволяет оптимизировать процесс запоминания.
Пособие предназначено для студентов медицинских вузов, обучающихся по специальностям «Лечебное дело» и «Стоматология» очной и очно-заочной формы обучения.
© НОУ ВПО СМИ «РеаВиЗ», 2010

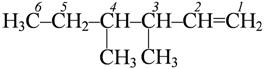 3,4 – диметилгексен -1
3,4 – диметилгексен -1 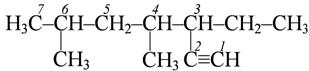 4,6-диметил-3-этилгептин-1
4,6-диметил-3-этилгептин-1 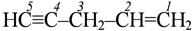 пентен-1-ин-4
пентен-1-ин-4 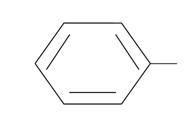 фенил-
фенил- 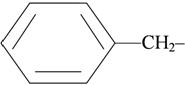 бензил-
бензил- 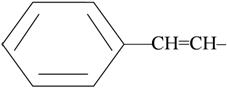 стирил-
стирил- 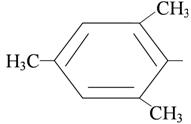 мезитил-
мезитил- 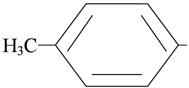 n-толил-
n-толил- 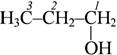 пропанол-1
пропанол-1 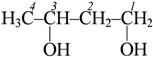 бутандиол-1,3
бутандиол-1,3 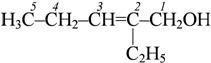 2-этилпентен-2-ол-1
2-этилпентен-2-ол-1