Лабораторно-практическое занятие № 34. «Карбоновые кислоты: строение, свойства, получение и идентификация» (2ч)
Цель:сформировать знания о строении и свойствах карбоновых кислот, их получении и идентификации
Вопросы для обсуждения:
1. Карбоновые кислоты, их реакционные центры и свойства.
2. Кислотные свойства.
3. Реакции нуклеофильного замещения.
4. Декарбоксилирование.
5. Галогенирование алифатических карбоновых кислот.
6. Получение и химическая идентификация карбоновых кислот.
Материалы и примеры для самостоятельного изучения
Пример 1. Как осуществляется образование галогенангидридов, каковы их свойства?
Гидроксил карбоксильной группы может быть замещен галогеном; при этом образуются галогенангидриды карбоновых кислот. Наиболее часто применяются хлорангидриды; они образуются, например, при действии на кислоты пятихлористого фосфора PCl5:
R—C—OH + PCl5 ® R—C—Cl + POCl3 + HCl
II II
O O
В галогенангидридах галоген соединен с радикалом кислоты – ацилом, поэтому их иначе называют галогенацилами или ацилгалогенидами. В частности, хлорангидрид уксусной кислоты называется хлористым ацетилом или ацетилхлоридом. Он представляет собой бесцветную дымящую на воздухе жидкость с Ткип. 55 оС; d420= 1.105
Галогенангидриды – очень реакционноспособные вещества; их применяют для разнообразных синтезов, при которых галоген обменивается на различные группы и образуются другие производные кислот. При действии воды происходит гидролиз галогенангидридов и они разлагаются, образуя карбоновую кислоту и галогеноводород:
R—C—Cl + HOH ® R—C—OH + HCl
II II
O O
С хлорангидридами низших кислот реакция протекает уже на холоду, обычно бурно, с выделением тепла.
Задачи для самостоятельного решения
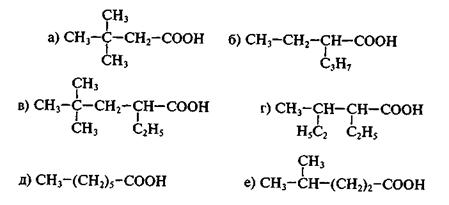
Задача 34. 1.Назовите согласно систематической номенклатуре соединения, формулы которых приведены:
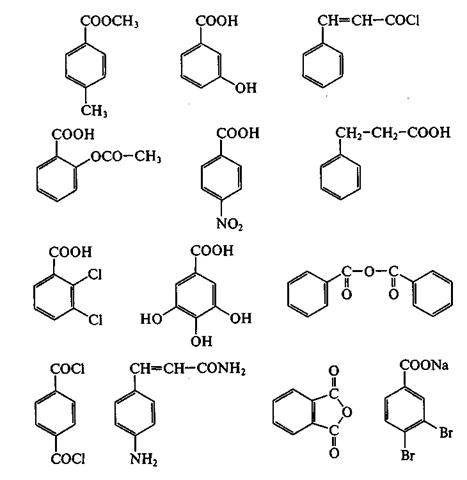
Задача 34. 2. Назовите согласно систематической номенклатуре следующие соединения:
Задача 34. 3. Сравните кислотные свойства следующих веществ: этилен, ацетилен, этанол, муравьиная кислота, уксусная кислота, изомасляная кислота, вода. Дайте объяснение, пользуясь представлениями об электронных эффектах. Укажите, какие значения констант кислотности (Ка), приведенные в произвольном порядке, соответствуют этим веществам: 1,75 ∙ 10-5; 1 ∙ 10-18, 1∙ 10-16; 1 ∙ 10-22; 1,77 ∙10-4; 1,4∙10-5.
Задача 34. 4.Расположите в ряд по усилению кислотных свойств следующие кислоты: уксусная, фторуксусная, хлоруксусная, бромуксусная, иодуксусная. Ответ обоснуйте.
Задача 34. 5. Расположите в ряд по усилению кислотных свойств следующие соединения: пара-нитробензойная кислота, пара-гидроксибензойная кислота, пара-фторбензойная кислота, пара-иодбензойная кислота, пара-бромбензойная кислота, пара-хлорбензойная кислота, пара-метилбензойная кислота. Дайте объяснение с точки зрения электронных эффектов, действующих в указанных веществах.
Задача 34. 6. Расположите в порядке усиления кислотных свойств следующие вещества: уксусная кислота, щавелевая кислота, этанол, акриловая кислота, хлоруксусная кислота. Приведите объяснение.
Задача 34. 7.Напишите уравнения реакций:
а) масляной кислоты с гидроксидом магния;
б) пропионовой кислоты с оксидом кальция;
в) уксусной кислоты с цинком;
г) пропионовой кислоты с гидроксидом натрия;
д) муравьиной кислоты с карбонатом магния;
е) хлоруксусной кислоты с аммиачным раствором гидроксида серебра;
ж) муравьиной кислоты с серной кислотой;
з) пропионовой кислоты с аммиаком (на холоду).
Задача 34. 8.Напишите уравнения реакций прямого хлорирования пропионовой, масляной и валериановой кислот. Объясните преимущественное замещение атома водорода хлором в 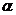 -положении с точки зрения электронной теории.
-положении с точки зрения электронной теории.
Задача 34. 9.Напишите уравнения реакций декарбоксилирования следующих кислот: а) трихлоруксусная; б) нитроуксусная; в) цианоуксусная. Назовите продукты. Объясните легкость отщепления карбоксильной группы от этих соединений при нагревании.
Задача 34. 10.Напишите уравнения реакций янтарной кислоты со следующими веществами:
а) РС15;
б) СН3ОН (Н+);
в) NН3(избыток) при нормальных условиях.
Задача 34. 11. Напишите схему этерификации пропионовой кислоты метиловым спиртом в присутствии серной кислоты. Приведите механизм и с его помощью объясните следующие факты: а) в отсутствие минеральной кислоты реакция практически не идет; б) высокая концентрация серной кислоты приводит к снижению скорости этерификации.
Задача 34. 12.Напишите уравнения реакций превращения:
а) этана в пропионовую кислоту;
б) углерода в муравьиную кислоту;
в) пропилена в пропионовую кислоту;
г) пропионата натрия в уксусную кислоту;
д) пропанола-1 в изомасляную кислоту;
е) пропанола-1 в масляную кислоту;
ж) 2,2-дихлорбутана в пропионовую кислоту;
з) 2-метил-пентанола-3 в 3-метил-2-этилбутановую кислоту;
и) ацетона в триметилуксусную кислоту.
Задача 34. 13.Какие вещества образуются в результате следующих превращений:
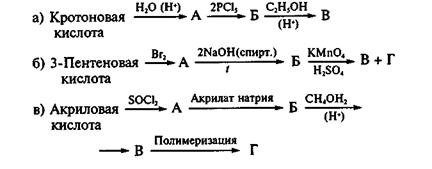
Задача 34. 14.Соединение состава С6Н12О2 взаимодействует с гидроксидом натрия Noah с образованием вещества С6Н11О2Nа. Последнее при нагревании с натронной известью дает углеводород C5H12 нормального строения. Установите строение исходного соединения, если известно, что оно оптически активно.
Задача 34. 15.Вещество, имеющее формулу С6Н8О4, обесцвечивает бромную воду, при озонолизе образует только пировиноградную кислоту СН3—С(О)—СООН, при нагревании подвергается внутримолекулярной дегидратации с образованием ангидрида состава С6Н6О3. Определите строение исследуемого вещества; напишите уравнения реакций перечисленных превращений.
Задача 34. 16.Осуществите следующие превращения: