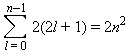Заполнения атомных орбиталей.
Заселение электронами атомных орбиталей (АО) осуществляется согласно принципу наименьшей энергии, принципу Паули и правилу Гунда.
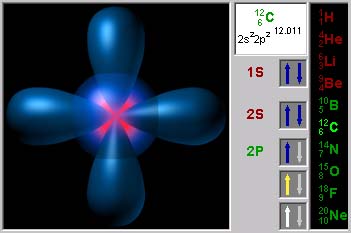 |
| Модель 2.3. Электронная конфигурация атома. Эта модель позволяет пронаблюдать электронные конфигурации атомов элементов первого и второго периодов. На правом краю модели имеется колонка, в которой перечислены названия атомов. В основном окне модели будет показана форма электронных орбиталей данного атома, а в колонке, находящейся слева от колонки с названиями атомов, будут отмечены занятые и не занятые электронные состояния для данного атома. Синими стрелками отмечены занятые состояния, желтой стрелкой отмечен электрон, отличающий электронную конфигурацию данного атома от предыдущего, белой стрелкой отмечено состояние, в которое надо добавить электрон, чтобы электронная конфигурация совпала с таковой для следующего атома. Направление стрелки характеризует спин электрона. Над колонкой с видом электронной конфигурации размещено маленькое окно, в котором показана клетка из таблицы Менделеева, соответствующая данному атому. Там приведены: символ элемента с указанием его номера и атомной массы наиболее распространенного изотопа в качестве нижнего и верхнего левых индексов; атомная масса элемента; краткая запись электронной конфигурации элемента. Обратите внимание на порядок заполнения p-орбиталей. По мере увеличения атомного номера на каждой из трех возможных p-орбиталей по очереди появляется сначала по одному электрону. Только когда не останется более свободных p-орбиталей, на уже занятые орбитали начинают добавляться электроны с противоположными спинами. Это означает, что существование двух электронов на двух различных p-орбиталях энергетически более выгодно, чем их существование на одной и той же p-орбитали. Причина этого кроется в кулоновском отталкивании электронов – одноименно заряженных частиц. |
Принцип наименьшей энергии требует, чтобы электроны заселяли АО в порядке увеличения энергии элекронов на этих орбиталях. Это отражает общее правило – максимуму устойчивости системы соответствует минимум ее энергии.
Принцип Паули запрещает в многоэлектронном атоме находиться электронам с одинаковым набором квантовых чисел. Это означает, что два любых электрона в атоме (или молекуле, или ионе) должны отличаться друг от друга значением хотя бы одного квантового числа, то есть на одной орбитали может быть не более двух электронов с различными спинами (спаренных электронов). Каждый подуровень содержит 2l + 1 орбитали, на которых размещаются не более 2(2l + 1) электронов. Отсюда следует, что емкость s-орбиталей – 2, p-орбиталей – 6, d-орбиталей – 10 и f-орбиталей – 14 электронов. Если число электронов при заданном l просуммировать от 0 до n – 1, то получим формулу Бора–Бьюри, определяющую общее число электронов на уровне с заданным n:
|
Эта формула не учитывает межэлектронное взаимодействие и перестает выполняться при n ≥ 3.
Орбитали с одинаковыми энергиями (вырожденные) заполняются в соответствии с правилом Гунда: наименьшей энергией обладает электронная конфигурация с максимальным спином. Это означает, что если на p-орбитали три электрона, то они располагаются так: 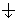
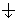
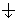 , и суммарный спин S = 3/2, а не так:
, и суммарный спин S = 3/2, а не так: 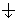
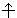
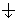 , S = 1/2.
, S = 1/2.