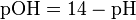Основные положения теории Аррениуса
1 Соли, кислоты и основания при растворении в воде и некоторых других полярных растворителях диссоциируют на ионы.
2 Ионы существуют в растворе независимо от того, проходит через раствор электрический ток или нет. Вследствие этого число независимо движущихся частиц растворенного вещества больше, чем при отсутствии диссоциации, и коллигативные свойства электролитов возрастают в i раз.
3 Процесс диссоциации описывается законом действующих масс (протекает обратимо). При уменьшении концентрации диссоциация становится практически полной
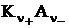 ↔ ν+Kz+ + ν –Az-
↔ ν+Kz+ + ν –Az-
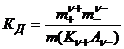
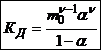
В частном случае при ν+=ν–=1
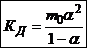 (*)
(*)
Здесь ν=ν++ν– - общее число ионов, образующихся при диссоциации одной молекулы,
m+, m– - моляльности ионов,
m(Kν+Aν–) – моляльность недиссоциированных молекул,
m0 – моляльность раствора при расчете на полностью недиссоциированное вещество,
α – степень диссоциации – доля диссоциированных молекул,
КД – практическая константа диссоциации.
4 Коэффициент Вант-Гоффа i – изотонический коэффициент – связан со степенью электролитической диссоциации. i – среднее суммарное число частиц (ионов и молекул), образующихся при диссоциации одной молекулы
i = ν +α + ν-α + (1-α) = 1 + (ν++ν–-1)α = 1 + (ν – 1)α i = 1+(ν-1)α
По мере увеличения разведения коэффициент Вант-Гоффа приближается к простому целому числу (2,3,4 – в зависимости от числа ионов, образующихся при растворении молекул вещества):
NaCl = Na+ + Cl- i→2
K2SO4 = 2K+ + SO 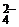 i→3
i→3
AlCl3 = Al3+ + 3Cl- i→4
K4[Fe(CN)6] = 4K+ + [Fe(CN)6]2- i→5
Билет 30. Диссоциация воды. Водородный и гидроксидный показатель.
Диссоциация воды
Диссоциация воды - разложение воды на составляющие химические элементы, иногда происходящая с созданием новых элементов, изначально в разлагаемом растворе не содержащихся, или содержащихся до начала разложения в меньшем количестве, чем после завершения процесса диссоциации.
Диссоциация воды является эндотермической реакцией (см.эндотермическая реакция), т.е. идущей с поглощением теплоты из окружающей среды.
Известные способы диссоциации воды:
1. Электролиз водных растворов-электролитов. - наименее эффективный из известных на сегодня способов разложения воды, так как в этом случае энергия затрачивается, в основном, на нагрев проводника - электролита, настолько, что диссциируемый раствор не только не охлаждается, но, напротив, подвергается значительному нагреву. В промышленности XX века именно этот способ получил наибольшее распространение, в силу того, что обеспечивает спрос и позволяет поддерживать высокие цены на такой товар, как невосполнимые энергоресурсы, из которых получают электричество, таких как нефть, газ, каменный угль и т.п.
2.Модель процесса разложения воды в центробежном поле Например, во вращающийся барабан заливается подогретый электролит, в котором при вращении в результате начинающегося электрохимического процесса происходит разложение воды на водород и кислород. Этот процесс разлагает воду с помощью кинетической энергии внешнего источника и тепловой энергии подогретого электролита. На основе данного процесса имеется ряд патентов, один из которых (RU 98/00190 (22.06.1998)) авторы - Кудымов Г.И и Студенников В.В. позиционируют, в том числе, и как и тепловой насос, поглощающий теплоту окружающей среды, таким образом, получение водородно-кислородной смеси здесь производится, в значительной мере за счет энергии окружающей среды или за счет обычно безвозвратно теряемого тепла, например выхлопных газов двигателей внутреннего сгорания.
Водоро́дный показа́тель, pH (произносится «пэ аш», английское произношение англ. pH — piː'eɪtʃ «Пи эйч») — мера активности (в очень разбавленных растворах она эквивалентна концентрации)ионов водорода в растворе, и количественно выражающая его кислотность, вычисляется как отрицательный (взятый с обратным знаком) десятичный логарифм активности водородных ионов, выраженной в молях на литр:
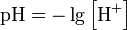
Когда концентрации обоих видов ионов в растворе одинаковы, говорят, что раствор имеет нейтральную реакцию. При добавлении к воде кислоты концентрация ионов водорода увеличивается, а концентрация гидроксид-ионов соответственно уменьшается, при добавлении основания — наоборот, повышается содержание гидроксид-ионов, а концентрация ионов водорода падает. Когда [H+] > [OH−] говорят, что раствор является кислым, а при [OH−] > [H+] — щелочным.
Для удобства представления, чтобы избавиться от отрицательного показателя степени, вместо концентраций ионов водорода пользуются их десятичным логарифмом, взятым с обратным знаком, который собственно и является водородным показателем — pH.
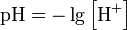
POH
Несколько меньшее распространение получила обратная pH величина — показатель основности раствора, pOH, равная отрицательному десятичному логарифму концентрации в растворе ионов OH−:
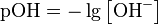
как в любом водном растворе при 22 °C 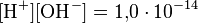 , очевидно, что при этой температуре:
, очевидно, что при этой температуре: