Основные положения теории электролитической диссоциации Сванте Аррениуса
Основные положения теории электролитической диссоциации Сванте Аррениуса
Электролиты – вещества, водные растворы и расплавы которых проводят электрический ток. Эти вещества имеют ионную и ковалентную сильнополярную связи. Электролитами являются кислоты, основания, соли. Поведение электролитов в растворе объясняет теория электролитической диссоциации, сформулированная Сванте Аррениусом в 1887 году:
Растворы сильных электролитов
В водных растворах сильные электролиты обычно полностью диссоциированы. В несильно разбавленных растворах сильных электролитов среднее расстояние между ионами вследствие значительной концентрации мало. В таких растворах ионы не вполне свободны, движение их стеснено взаимным притяжением друг другу.
Вследствие этого притяжения каждый ион как бы окружен шарообразным роем противоположно заряженных ионов, получившим название «ионной атмосферы».
В отсутствие внешнего электрического поля ионная атмосфера симметрична и силы, действующие на центральный ион, взаимно уравновешиваются. Если же приложить к раствору постоянное электрическое поле, то разноименно заряженные ионы будут перемещаться в противоположных направлениях. При этом каждый ион стремится двигаться в одну сторону, а окружающая его ионная атмосфера – в противоположную, вследствие чего уменьшается сила тока.
Чем больше концентрация раствора, тем сильнее проявляется тормозящее действие ионной атмосферы на электропроводность раствора, о чем свидетельствуют следующие данные:
| СKCl, н | 0,01 | 0,1 | ||
| α, % | 94,2 | 86,2 | 75,6 | 71,2 |
Однако падение α объясняется не образованием молекул, а увеличением тормозящего действия ионной атмосферы. В связи с этим α сильных электролитов называется кажущейся степенью диссоциации.
Для оценки состояния ионов в растворе пользуются величиной, называемой активностью.
Под активностью иона понимают ту эффективную концентрацию его, соответственно которой он действует при химических реакциях. Активность иона а равна произведению его моляльной концентрации (Сm) на коэффициент активности (f):
a = f∙Cm
Коэффициенты активности различных ионов различны. Они изменяются с изменением концентрации растворов. В концентрированных растворах f<1, а с разбавлением раствора f→1. Если f<1, то это указывает на сильное межионное взаимодействие, если f≈1, то это свидетельствует о слабом межионном взаимодействии (приложение, табл. 2).
Коэффициенты активности ионов зависят от состава и концентрации раствора, от заряда и природы иона и от других условий.
В разбавленных растворах природа иона мало влияет на значение f. Поэтому приближенно можно считать, что в разбавленных растворах коэффициент активности иона в данном растворителе зависит только от заряда иона и ионной силы раствора I, которая равна полусумме произведений концентрации Cm каждого иона на квадрат его заряда z :
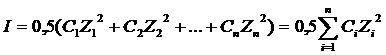
Приближенно коэффициент активности иона в разбавленном растворе можно также вычислить по формуле
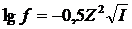 (табл. 2).
(табл. 2).
Произведение растворимости
Абсолютно нерастворимых веществ нет. Твердые вещества отличаются своей растворимостью. Очевидно, что труднорастворимый электролит легко образует насыщенный раствор. Рассмотрим равновесия, наблюдаемые в насыщенном растворе какого-нибудь труднорастворимого вещества, например, CaSO4. В этой системе осадок находится в равновесии с насыщенным раствором этого вещества:
СaSO4  Ca2+ + SO42–
Ca2+ + SO42–
осадок раствор
Константа равновесия для процесса растворения осадка имеет следующий вид:
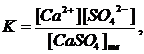
откуда K∙[CaSO4]тв = [Ca2+]∙[SO42-].
Концентрация твердого вещества есть величина постоянная:
[CaSO4]тв = const.
Учитывая это, K∙[CaSO4]тв как произведение двух постоянных величин также можно считать величиной постоянной, некоторой константой, характерной для данного вещества. Эту константу называют произведением растворимости. Её обозначают через ПР:
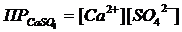 .
.
Для насыщенного раствора сульфата кальция произведение растворимости при 25оС найдено равным 3,72∙10-5 г-ион2/л2.
Таким образом, ПР – это произведение концентраций ионов малорастворимого сильного электролита, содержащихся в свободном виде в его насыщенном растворе. Величина ПР означает, что в насыщенном растворе труднорастворимого электролита произведение концентраций его ионов есть величина постоянная (при данной температуре).
Произведение растворимости характеризует растворимость электролитов. Растворимость численно равна 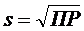 (для бинарных электролитов).
(для бинарных электролитов).
В общем случае для труднорастворимого электролита состава AnBm в растворе наблюдается равновесие:
AnBm = nAa++ mBb–.
Тогда
ПР = [Aa+]n [Вb–]m
Сравнивая значения произведений растворимости труднорастворимых солей, можно видеть, какая из них растворяется лучше (приложение, табл. 3).
Из величины ПР вытекает условие образования и растворения осадка:
1. Если [Aa+]n [Вb–]m = ПР, то осадок находится в равновесии с раствором.
2. Если [Aa+]n [Вb–]m > ПР, то осадок выпадает.
3. Если [Aa+]n [Вb–]m < ПР, то осадок растворяется.
Таким образом, если при той или иной химической реакции произведение концентраций участвующих в ней ионов станет больше произведения растворимости, то выпадает осадок труднорастворимого вещества. И обратно, если произведение концентраций ионов данного электролита в насыщенном его растворе в результате той или иной реакции становится меньше произведения растворимости для ионов этого электролита, то осадок переходит в раствор.
Индикаторы
Вещества, изменяющие окраску при изменении реакции среды, - индикаторы – чаще всего сложные органические соединения – слабые кислоты или слабые основания. Схематично состав индикаторов можно выразить формулами НInd или IndOH, где Ind – сложный органический анион или катион индикатора.
Принцип применения индикаторов основан на том, что недиссоциированные молекулы индикатора и его Ind–ионы имеют в растворе разную окраску, и окраска раствора изменяется в зависимости от пложения равновесия диссоциации индикатора. Например, фенолфталеин (кислотный индикатор) имеет молекулы бесцветные, а анионы малиновые; метилоранж (основной индикатор) – желтые молекулы и красные катионы.
фенолфталеин метилоранж
HInd  H+ + Ind– IndOH
H+ + Ind– IndOH  Ind+ + OH–
Ind+ + OH–
бесцв. малинов. желт. красн.
Индикаторы, как слабые электролиты, имеют малые величины констант диссоциации. Например, Кд фенолфталеина равна 2∙10-10 и в нейтральных средах он находится преимущественно в виде своих молекул вследствие очень малой концентрации ионов, почему и остается бесцветным. При добавлении щелочи Н+-ионы фенолфталеина связываются, «стягиваются» с ОН–-ионами щелочи, образуя молекулы воды, и положение равновесия диссоциации индикатора смещается вправо – в сторону увеличения концентрации Ind–-ионов, появляется малиновое окрашивание. При добавлении в этот же раствор кислоты одновременно с нейтрализацией щелочи – при достаточной концентрации Н+-ионов – положение равновесия диссоциации индикатора смещается влево, в сторону моляризации, раствор снова обесцвечивается. Аналогично происходит изменение окраски метилоранжа: желтая в нейтральной среде переходит в красную в кислой среде при добавлении H+-ионов и снова в желтую при добавлении OH–-ионов.
Таким образом, окраска индикаторов зависит от рН-среды.
Раствор, содержащий индикатор, непрерывно изменяет свою окраску при изменении рН. Человеческий глаз, однако, не очень чувствителен к таким изменениям. Диапазон, в котором наблюдается изменение окраски индикатора, определяется физиологическими пределами восприятия цвета человеческим глазом. При нормальном зрении глаз способен различить присутствие одной окраски в смеси ее с другой окраской только при наличии как минимум некоторой пороговой плотности первой окраски: изменение окраски индикатора воспринимается только в той области, где имеется 5-10-кратный избыток одной формы по отношению к другой. Рассматривая в качестве примера HInd и характеризуя состояние равновесия
HInd  H+ + Ind–
H+ + Ind–
соответствующей константой
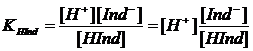 ,
,
можно написать, что индикатор проявляет свою чисто кислотную окраску, обычно улавливаемую наблюдателем, при
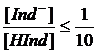 ,
,
а чисто щелочную окраску при
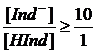 .
.
Внутри интервала, определяемого этими величинами, проявляется смешанная окраска индикатора.
Таким образом, глаз наблюдателя различает изменение окраски лишь при изменении реакции среды в интервале около 2-х единиц рН. Например, у фенолфталеина этот интервал рН от 8,2 до 10,5: при рН=8,2 глаз наблюдает начало появления розовой окраски, которая все усиливается до значения рН=10,5, а при рН=10,5 усиление красной окраски уже незаметно. Этот интервал значений рН, в котором глаз различает изменение окраски индикатора, называют интервалом перехода окраски индикатора.
Указанный диапазон рН величиной приблизительно в 2 единицы для различных индикаторов не приходится на одну и ту же область шкалы рН, так как его положение зависит от конкретного значения константы диссоциации каждого индикатора. В табл.4 приложения приведены интервалы перехода и цвета наиболее распространенных кислотно-основных индикаторов.
ЛАБОРАТОРНЫЕ РАБОТЫ ПО ТЕМЕ
«РАСТВОРЫ ЭЛЕКТРОЛИТОВ»
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ
Слабые электролиты
Примеры решения задач
Задача 1.1. Степень диссоциации уксусной кислоты в 0,1 М растворе равна 1,32∙10–2. Найти константу диссоциации кислоты и значение рК.
Решение. Подставим данные задачи в уравнение закона разбавления Оствальда
К = α2CM/(1–α) = 1,77∙10–5 pK = -lg K = 4,75
Задача 1.2.Вычислить концентрацию ионов водорода в 0,1 М растворе хлорноватистой кислоты HClO (K=5∙10-8).
Решение: Найдем степень диссоциации HClO
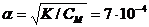 . Отсюда [H+] = α∙CM = 7∙10–5 моль.
. Отсюда [H+] = α∙CM = 7∙10–5 моль.
Задачу можно решить и другим способом, используя соотношение
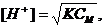 тогда [H+] = 7∙10–5 моль/л.
тогда [H+] = 7∙10–5 моль/л.
Задача 1.3. Во сколько раз уменьшится концентрация ионов водорода в 0,2 М растворе HCOOH (K = 0,8∙10–4), если к 1 л этого раствора добавить 0,1 моль HCOONa? Считать, что соль полностью диссоциирована.
Решение: HCOOH  H+ + НCOO–
H+ + НCOO–
HCOONa → HCOO– + Na+
Исходная концентрация ионов водорода:
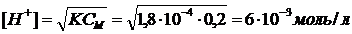 .
.
Концентрацию ионов водорода в растворе после добавления соли обозначим х. Тогда концентрация недиссоциированных молекул кислоты равна (0,2-х). Концентрация же ионов HCOO– слагается из двух величин: из концентрации, создаваемой диссоциацией молекул кислоты, и концентрации, обусловленной присутствием в растворе соли. Общая концентрация ионов HCOO– равна, следовательно, (0,1+х)
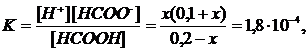 откуда х = 3,6∙10–4 моль/л.
откуда х = 3,6∙10–4 моль/л.
Сравнивая исходную концентрацию ионов водорода с найденной, находим, что прибавление соли HCOONa вызвало уменьшение концентрации ионов [H+] в 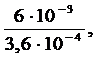 т.е. в 16,6 раза.
т.е. в 16,6 раза.
Задачи для самостоятельной работы:
1.4. Нужно приготовить раствор, содержащий в 1 л 0,5 моля NaCl, 0,16 моля KCl и 0,24 моля K2SO4. Как это сделать, имея в своем распоряжении только NaCl, KCl и Na2SO4?
1.5. Константа диссоциации масляной кислоты C3H7COOH 1,5∙10–5. Вычислить степень её диссоциации в 0,005 М растворе.
1.6. Найти степень диссоциации хлорноватистой кислоты HOCl в 0,2 н. растворе.
1.7. Степень диссоциации муравьиной кислоты HCOOH в 0,2 н. растворе равна 0,03. Определить константу диссоциации кислоты и значение рК.
1.8. Степень диссоциации угольной кислоты H2CO3 по первой ступени в 0,1 н. растворе равна 2,11∙10–3. Вычислить К1.
1.9. При какой концентрации раствора степень диссоциации азотистой кислоты HNO2 будет равна 0,2?
1.10. В 0,1 н. растворе степень диссоциации уксусной кислоты равна 1,32∙10–2. При какой концентрации азотистой кислоты HNO2 ее степень диссоциации будет такой же?
1.11. Сколько воды нужно прибавить к 300 мл 0,2 М раствора уксусной кислоты, чтобы степень диссоциации кислоты удвоилась?
1.12. Чему равна концентрация ионов водорода H+ в водном растворе муравьиной кислоты, если α = 0,03?
1.13. Вычислить [H+] в 0,02 М растворе сернистой кислоты. Диссоциацией кислоты по второй ступени пренебречь.
1.14. Вычислить [H+], [HSe–] и [Se2–] в 0,05 М растворе H2Se.
1.15. Во сколько раз уменьшится концентрация ионов водорода, если к 1 л 0,005 М раствора уксусной кислоты добавить 0,05 моля ацетата натрия?
1.16. Рассчитать концентрацию ионов CH3COO– в растворе, 1 л которого содержит 1 моль CH3COOH и 0,1 моля HCl, считая диссоциацию последнего полной.
Сильные электролиты
Пример решения задач
Задача 2.1. Вычислить ионную силу и активность ионов в растворе, содержащем 0,01 моль/л MgSO4 и 0,01 моль/л MgCl2.
Решение: Ионная сила раствора равна
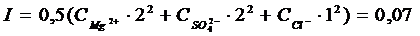
Коэффициент активности иона Mg2+ (и равный ему коэффициент активности иона SO42–) найдем по формуле
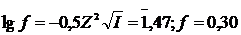
Аналогично находим f для Cl–:
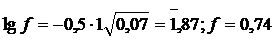
Теперь, пользуясь соотношением а = f∙CM, находим активность каждого иона:
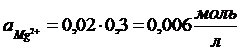
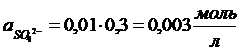
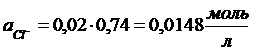
Задачи для самостоятельной работы:
2.2. Вычислить приближенное значение активности ионов K+ и SO42– в 0,01 М растворе K2SO4.
2.3. Вычислить приближенное значение активности ионов Ba2+ и Cl– в 0,002 н. растворе BaCl2.
2.4. Найти приближенное значение коэффициентов активности иона водорода в 0,0005 М растворе H2SO4, содержащем, кроме того, 0,0005 моль/л HCl. Считать, что серная кислота полностью диссоциирует по обеим ступеням.
2.5. Вычислить ионную силу и активность ионов в растворе, содержащем 0,01 моль/л Ca(NO3)2 и 0,01 моль/л CaCl2.
2.6. Вычислить ионную силу и активность ионов в 0,1 %-ном (по массе) растворе BaCl2. Плотность раствора принять равной единице.
2.7. Рассчитать активность иона водорода в 0,005 н. растворе HCl, содержащем, кроме того, 0,15 моль/л NaCl.
2.8. Найти приближенные значения коэффициентов активности ионов Cl–, SO42–, PO43– и [Fe(CN)6]4– в растворе с ионной силой 0,0001.
Произведение растворимости
Примеры решения задач
Задача 3.1. Растворимость гидроксида магния Mg(OH)2 при 18 оС равна
1,7∙10 –4 моль/л. Найти ПР Mg(OH)2 при этой температуре.
Решение: При растворении каждого моля Mg(OH)2 в раствор переходит 1 моль ионов Mg+2 и вдвое больше ионов ОН–.
Mg(OH)2 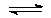 Mg2+ + 2 OH–
Mg2+ + 2 OH–
Следовательно, в насыщенном растворе Mg(OH)2
[Mg2+] = 1,7∙10-4 моль/л; [OH–] = 3,4∙10– 4 моль/л.
Отсюда 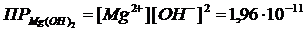 .
.
Задача 3.2. 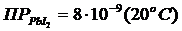 . Вычислить растворимость соли (в моль/л и в г/л) при указанной температуре.
. Вычислить растворимость соли (в моль/л и в г/л) при указанной температуре.
Решение: Обозначим растворимость соли через s (моль/л). Тогда в насыщенном растворе PbI2 cодержится s моль/л ионов Pb2+ и 2s моль/л ионов I–.
PbI2  Pb+2+2I–
Pb+2+2I–
s s 2s
ПР=[Pb2+][I–]2 = 4s3
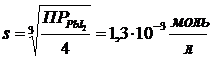 ;
; 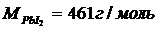 .
.
Растворимость PbI2, выраженная в г/л, составляет 1,3∙10-3∙461 = 0,6 г/л.
Задача 3.3. Во сколько раз растворимость CaC2O4 в 0,1 М растворе (NH4)2C2O4 меньше, чем в воде?
Решение: Вычислим растворимость CaC2O4 в воде. Пусть концентрация соли в растворе будет s (моль/л), поэтому можем записать
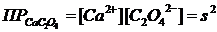
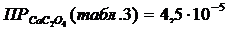
Отсюда
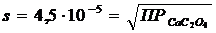
Найдем растворимость этой соли в 0,1 М растворе (NH4)2C2O4; обозначим её через s′. Концентрация ионов Ca2+ в насыщенном растворе тоже будет s′, а концентрация [C2O42–] составит (0,1+s′), т.к. s′<0,1, то можно считать, что [C2O42–] = 0,1моль/л. Тогда 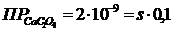 ; s′=2∙10–8 моль/л. Следовательно, в присутствии (NH4)2C2O4 растворимость СaC2O4 уменьшилась в
; s′=2∙10–8 моль/л. Следовательно, в присутствии (NH4)2C2O4 растворимость СaC2O4 уменьшилась в 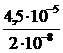 раз, т.е. в 2200 раз.
раз, т.е. в 2200 раз.
Задача 3.4. Смешаны равные объемы 0,02 н. растворов CaCl2 и Na2SO4; образуется ли осадок CaSO4?
Решение: Найдем произведение концентраций ионов Ca+2 и SO42– сравним его с 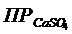 . Условием выпадения осадка является [Ca2+][SO42–] >
. Условием выпадения осадка является [Ca2+][SO42–] > 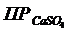 .
.
Исходные молярные концентрации растворов CaCl2 и Na2SO4 одинаковы и равны 0,01 моль/л, т.к. при смешении исходных растворов общий объем раствора вдвое больше, то концентрация каждого из ионов вдвое уменьшается по сравнению с исходными. Поэтому [Ca2+] = [SO42–] = 5∙10–3, находим [Ca2+][SO42–] = 2,5∙10–5
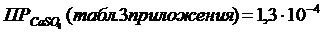
2,5∙10-5 < 1,3∙10-4.
Поэтому осадок не образуется.
Задача 3.5. Произведение растворимости CaC2O4 = 2∙10–9. Найти растворимость этой соли в 0,1 М растворе (NH4)2C2O4.
Решение: Выразим ПР 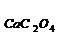 через активность ионов:
через активность ионов:
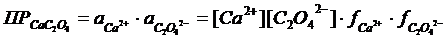 .
.
Обозначив искомую растворимость соли через s, находим, что
[Ca2+] = s моль/л, [C2O42–] = 0,1 моль/л. Таким образом,
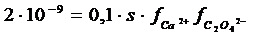
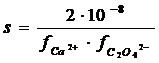
Вычислим ионную силу раствора (I) 0,1 М раствора (NH4)2C2O4
I = 0,5(0,2∙12+0,1∙22) = 0,3
Согласно табл. 2 приложения, при этой ионной силе коэффициенты активности двухзарядных ионов равны 0,42. Тогда
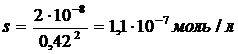 .
.
Задачи для самостоятельной работы:
3.6. Растворимость CaCO3 при 35оС равна 6,9∙10–5 моль/л. Вычислить произведение растворимости этой соли.
3.7. Вычислить произведение растворимости PbBr2 при 25 оС, если растворимость соли при этой температуре равна 1,32∙10–2 моль/л.
3.8. В 500 мл воды при 18 оС растворяется 0,0166 г AgCrO4. Чему равно произведение растворимости этой соли?
3.9. Для растворения 1,16 г PbI2 потребовалось 2 л воды. Найти произведение растворимости соли.
3.10. Исходя из произведения растворимости карбоната кальция, найти массу CaCO3, содержащуюся в 100 мл его насыщенного раствора.
3.11. Найти массу серебра, находящегося в виде ионов в 1 л насыщенного раствора AgBr.
3.12. Вычислить объем воды, необходимый для растворения при 25 оС 1 г BaSO4.
3.13. В каком объеме насыщенного раствора Ag2S содержится 1 мг растворенной соли?
3.14. Во сколько раз растворимость (в моль/л) Fe(OH)2 в воде больше растворимости Fe(OH)3 при 25 оС?
3.15. Образуется ли осадок сульфата серебра, если к 0,02 М раствору AgNO3 добавить равный объем 1 н. раствора H2SO4?
3.16. К 50 мл 0,001 н. раствора HCl добавили 450 мл 0,0001 н. раствора AgNO3. Выпадет ли осадок хлорида серебра?
3.17. Образуется ли осадок хлорида свинца, если к 0,1 н. раствору Pb(NO3) добавить равный объем 0,4 н. раствора NaCl?
3.18. Во сколько раз уменьшится концентрация ионов серебра в насыщенном растворе AgCl, если прибавить к нему столько соляной кислоты, чтобы концентрация ионов Cl- в растворе стала равной 0,03 моль/л?
3.19. Вычислить растворимость (в моль/л) CaF2 в воде и в 0,05 М растворе CaCl2. Во сколько раз растворимость во втором случае меньше, чем в первом?
3.20. Во сколько раз растворимость AgCl в 0,001 н. растворе NaCl меньше, чем в воде? Расчет произвести с учетом коэффициентов активности, пользуясь данными табл. 2 приложения.
3.21. В каком из указанных случаев раствор электролита МХ ненасыщен: а) [Mz+][Xz-] < ПР; б) [Mz+][Xz-] = ПР; в) [Mz+][Xz-] > ПР?
3.22. Обозначим растворимость AgCl в воде, в 0,01 М CaCl2, в 0,01 M NaCl и в 0,05 М AgNO3 соответственно через so, s1, s2 и s3. Какое соотношение между этими величинами правильно: а) so > s1 > s2 > s3; б) so > s2 > s1 > s3; в) so > s1 = s2 > s3; г) so > s2 > s3 > s1?
3.23. К 0,01 н. раствору H2SO4 медленно добавляют раствор, содержащий 0,01 моль/л CaCl2 и 0,01т моль/л SrCl2. Какой осадок начнет выпадать раньше: а) SrSO4; б) CaSO4?
3.24. Произведения растворимости солей NiC2O4 и Na3AlF6 одинаковы (4∙10-10). Какое соотношение между растворимостями (моль/л) этих солей правильно:
а) 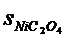 >
> 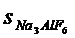 ; б)
; б) 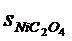 =
= 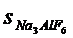 ; в)
; в) 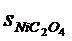 <
< 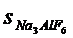 ?
?
3.25. Произведения растворимости AgBrO3 и Ag2SO4 равны соответственно 5,5∙10-5 и 2∙10-5. укажите правильное соотношение между растворимостями (s, моль/л) этих солей:
а) 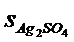 <
< 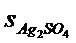 ; б)
; б) 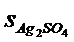 ≈
≈ 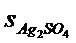 ; в)
; в) 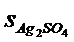 >
> 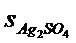 .
.
3.26. Как изменится растворимость CaF2 в 0,1 М растворе KNO3 по сравнению с его растворимостью в воде:
а) возрастет; б) уменьшится; в) останется неизменной?
Продолжение
Таблица 4
Интервалы перехода и окраска в различных средах
наиболее распространенных кислотно-основных индикаторов
| Название | Цвет индикатора в различных средах | ||
| Фенолфталеин | бесцветный рН < 8 | бледно- малиновый 8.0 < pH < 9.8 | малиновый pH > 9.8 |
| Лакмус | красный рН < 5 | фиолетовый 5 < рН < 8 | синий рН > 8 |
| Метиловый оранжевый | красный рН < 3.1 | оранжевый | желтый |
| 3.1< рН < 4.4 | рН > 4.4 | ||
| Метиловый фиолетовый | жёлтый рН = 0 | фиолетовый рН > 3 | |
| Бромкрезоловый зелёный | жёлтый рН < 3,8 | синий рН > 5,6 | |
| Бромтимоловый | жёлтый | синий pH > 7,7 | |
| рН < 6 | |||
| Тимоловый синий | красный рН < 0,5 | жёлтый 2,5 < pH < 7,9 | синий pH > 7,9 |
СПИСОК ЛИТЕРАТУРЫ
1. Некрасов Б.З. Курс общей химии.–М., 1948.–1004 с.
2. Глинка Н.Л. Задачи и упражнения по общей химии.–М.: Интеграл-Пресс, 2001.–240 с.
3. Латыпова Ф.Н., Сыркин А.М. Методическое руководство к лабораторным работам по теме «Растворы электролитов».–Уфа: УНИ, 1987.–29 с.
СОДЕРЖАНИЕ
1. Основные положения теории электролитической диссоциации Сванте
Аррениуса ………………………………………………………………………1
2. Механизм диссоциации …………………………………………………….....1
3. Диссоциация солей, оснований и кислот …………………………………….3
4. Степень диссоциации электролита. Закон разбавления Оствальда ………..4
5. Растворы сильных электролитов ……………………………………………...7
6. Ионно-обменные реакции в растворах ……………………………………….8
7. Произведение растворимости ………………………………………………...9
8. Ионное произведение воды и водородный показатель …………………….10
9. Индикаторы …………………………………………………………………...12
Лабораторные работы по теме «Растворы электролитов» …………………...14
Задания для самостоятельной работы …………………………………………16
Варианты домашних заданий ………………………………………………….26
Приложение ……………………………………………………………………..27
Список литературы………………………………………………………………29
Основные положения теории электролитической диссоциации Сванте Аррениуса
Электролиты – вещества, водные растворы и расплавы которых проводят электрический ток. Эти вещества имеют ионную и ковалентную сильнополярную связи. Электролитами являются кислоты, основания, соли. Поведение электролитов в растворе объясняет теория электролитической диссоциации, сформулированная Сванте Аррениусом в 1887 году:
