Факторы влияющие на скорость хим реакции.
Основные факторы – это концентрация реагирующих веществ, температура, наличие катализатора.
Кинетические уравнения реакции первого второго и третьего порядка. Период полураспада.
Реакции первого порядка.
Рассмотрим в общем виде реакцию первого порядка:
А  продукты
продукты
Уравнение скорости для этого типа реакций имеет вид:
ω = - 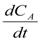 = kCА
= kCА
После разделения переменных получим:
- 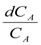 = kdt
= kdt
Интегрирование уравнения в пределах С0 – С и 0 – t даёт:
ln 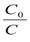 = kt
= kt
где С0 – концентрация вещества А на начало реакции при t = 0;
С - концентрация вещества А ко времени протекания реакции t;
k –константа скорости химической реакции.
Это уравнение часто используется в виде
lnC = lnC0 – kt
Реакции второго порядка
Рассмотрим в общем виде реакцию второго порядка типа
А + В  продукты
продукты
Уравнение скорости дя реакций подобного типа можно записать в виде
ω = -  = kCACB
= kCACB 
Если начальные концентрации (t = 0) веществ А и В одинаковы и равны С0,А = С0,В = С0, то:
ω = - 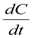 = kC2,
= kC2,
где С – концентрация вещества А и В ко времени t.
После разделения переменных и интегрирования в пределах С0 – С и 0 – t получим:
 + kt
+ kt
или
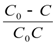 = kt
= kt
Период полураспада для реакций подобного типа определяется уравнением:
t1/2 = 
Рассмотрим в общем виде реакцию третьего порядка:
3А  продукты
продукты
Уравнение скорости для этого типа реакций имеет вид:
ω = - 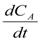 = kC
= kC 
После разделения переменных получим:
- 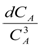 = kdt
= kdt
Интегрирование уравнения в пределах С0 – С и 0 – t даёт:
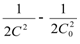 = kt
= kt
или 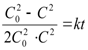
где С0 – концентрация вещества А на начало реакции при t = 0;
С - концентрация вещества А ко времени протекания реакции t;
k –константа скорости химической реакции.
ПЕРИОД ПОЛУРАСПАДА.
Важной характеристикой радиоактивного вещества является период полураспада — время, за которое распадается половина количества исходного вещества. Например, если половина его распадается за четыре дня, то и период полураспада принимается равным четырем дням. Через следующие четыре дня распадается половина оставшегося количества, через восемь дней его останется только 1/4, через 12 дней — 1/8 и т. д. Чтобы радиоактивность снизилась до 1% исходного вещества, должно пройти примерно семь периодов полураспада.
Необходимо подчеркнуть, что половина атомов радиоактивного вещества распадается за указанное время лишь в среднем. Фактически некоторые атомы не распадаются вовсе, в то время как другие распадаются в значительно более короткие промежутки времени.
Чем интенсивнее идет радиоактивный распад, тем короче период полураспада. Сильные излучатели живут гораздо меньше, чем слабые.
Один грамм урана содержит около 2,5 -1021 атомов. Однако из этого астрономического количества в секунду распадается только около 12 тыс. атомов. Поэтому период полураспада урана исключитель но долог — около 4,5 млрд. лет. У тория он еще дольше — более 14 млрд. лет! Время полураспада радия-226 — 1617 лет, радона — 3,82 дня, полония-218 — 3,05 мин, полония-212 — 3-Ю-7 сек, некоторых элементарных частиц — миллионные и миллиардные доли секунды.
