Протонная теория кислот и оснований Бренстеда
Кислоты Бренстеда – это соединения, способные отдавать протон (доноры протона).
Основания Бренстеда – это соединения, способные присоединять протон (акцепторы протона). Для взаимодействия с протоном основание должно иметь свободную пару электронов или электроны π-связи.
Кислоты и основания образуют сопряженные кислотно-основные пары, например:
| CH3COOH | + | H2O | 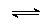 | CH3COO- | + | H3O+ |
| кислота1 | основание2 | основание1 | кислота2 |
| CH3NH2 | + | H2O | 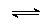 | CH3NH3+ | + | OH- |
| основание1 | кислота2 | кислота1 | основание2 |
В общем виде:
| Н-А | + | :В | 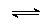 | :А | + | Н-В |
| кислота1 | основание2 | основание1 | кислота2 |
Сила кислоты НА будет зависеть от силы основания :В. Поэтому для создания единой шкалы силу кислот и оснований Бренстеда определяют относительно воды, которая является амфотерным соединением и может проявлять и кислотные, и основные свойства.
Сила кислот определяется константой равновесия их взаимодействия с водой как основанием, например:
CH3COOH + H2O = CH3COO- + H3O+

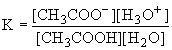
Так как в разбавленных растворах [H2O]=const, то ее можно внести в константу равновесия, которую называют константой кислотности:
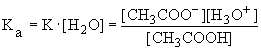
На практике чаще пользуются величинами pKa= - lg Ka. Чем меньше величина pKa, тем сильнее кислота.
Сила оснований определяется константой равновесия взаимодействия их с водой как кислотой:
RNH2 + H2O = RNH3+ + OH-
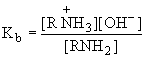 - константа основности.
- константа основности.
Для сопряженных кислоты и основания Ka Kb=KW. Таким образом, в сопряженной кислотно-основной паре, чем сильнее кислота, тем слабее основание и наоборот. Силу основания чаще выражают не константой основности, а константой кислотности сопряженной кислоты 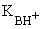 . Например, для основания RNH2 величина
. Например, для основания RNH2 величина 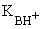 - это константа кислотности сопряженной кислоты
- это константа кислотности сопряженной кислоты 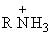 :
:
RNH3+ + H2O = RNH2 + H3О+
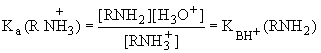
На практике чаще пользуются величиной 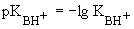 . Чем больше величина
. Чем больше величина 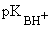 , тем сильнее основание.
, тем сильнее основание.
Классификация органических кислот и оснований
Кислоты и основания Бренстеда классифицируют по природе атома при кислотном или основном центре.
В зависимости от природы элемента, с которым связан протон, различают четыре основных типа органических кислот Бренстеда:
· O-H – кислоты - карбоновые кислоты, спирты, фенолы;
· S-H – кислоты - тиолы;
· N-H – кислоты - амины, амиды, имиды;
· C-H – кислоты - углеводороды и их производные.
В зависимости от природы атома, к неподеленной паре электронов которого присоединяется протон, основания Бренстеда делят на три основных типа:
o аммониевые основания - амины, нитрилы, азотсодержащие гетероциклические соединения;
o оксониевые основания - спирты, простые эфиры, альдегиды, кетоны, карбоновые кислоты и их функциональные производные;
o сульфониевые основания - тиолы, сульфиды.
Особый тип оснований Бренстеда представляют π-основания, в которых центром основности являются электроны π-связи (алкены, арены).
