Основные положения протолитической теории кислот и оснований Бренстеда-Лоури. Теория Льюиса.
Теория Бренстеда-Лоури: кислотой называют всякое вещество, молекулярные частицы которого(в том числе и ионы) способны отдавать протон, т.е. быть донором протонов; основанием называют всякое вещество, молекулярные частицы которого(в том числе и ионы) способны присоединить протоны, т.е. быть акцептором протонов. Например: HNO3 + H2O= H3O+ + NO3-
Молекула и ион, отличающиеся по составу на один протон, называются сопряженной кислотно-основной парой. Частицы, способные к взаимодействию как с кислотами, так и с основаниями, называются амфолитами.
Теория Льюиса: кислотой называют вещество, принимающие электронные пары, - акцептор электронов; основанием называют вещество, поставляющее электроны для образования химической связи, - донор электронов. Например: NH3 + HCI=NH4CI
14. Автопротолиз –обратимый процесс образования равного числа катионов и анионов из незаряженных молекул жидкого индивидуального вещества за счет передачи протона от одной молекулы к другой. H2O + H2O= H3O+ + OH–. Это равновесие называется равновесием автопротолиза воды. Константа автопротолиза для воды обычно называется ионным произведением воды и обозначается как Kw. Ионное произведение численно равно произведению равновесных концентраций ионов гидроксония и гидроксид-анионов. Обычно используется упрощенная запись:
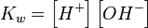
При стандартных условиях ионное произведение воды равно 10-14. Оно является постоянной не только для чистой воды, но также и для разбавленных водных растворов веществ. Автопротолиз воды объясняет, почему чистая вода, хоть и плохо, но всё же проводит электрический ток. pH — это водородный показатель— мера активности (в случае разбавленных растворов отражает концентрацию) ионов водорода в растворе, количественно выражающая его кислотность, вычисляется как отрицательный (взятый с обратным знаком) десятичный логарифм концентрации водородных ионов, выраженной в молях на литр: pH = -log[H+]. Т.е. рН определяется количественным соотношением в воде ионов Н+ и ОН-, образующихся при диссоциации воды. (Моль — единица измерения количества вещества.) Если в воде пониженное содержание свободных ионов водорода [H+] (рН > 7) по сравнению с ионами гидроксида [ОН-], то вода будет иметь щелочную реакцию, а при повышенном содержании ионов Н+ (рН < 7) - кислую. В идеально чистой дистиллированной воде эти ионы будут уравновешивать друг друга и в нейтральной воде рН=7. При растворении в воде различных химических веществ этот баланс может быть нарушен, что приводит к изменению значения рН. Когда концентрации обоих видов ионов в растворе одинаковы, говорят, что раствор имеет нейтральную реакцию. 15. Типы протолитических реакций. К протолитическим реакциям относят химические процессы, суть которых заключается в переносе протона от одних реагирующих веществ к другим.протолитическая теория кислот и оснований, в соответствии с которой кислотой считают любое вещество, отдающее протон, а основанием - вещество, способное присоединять протон, например:
CH3COOH + H2O = CH3COO- + H3O+
кислотаI основаниеI основаниеI кислотаII
NH3 + H2O = NH4+ + OH-
основаниеIкислотаII кислотаII основаниеI К протолитическим реакциям относят реакции нейтрализации и гидролиза.
Реакция 1 типа уксусная кислота с водой:  протекающая в прямом направлении,представляет ионизацию уксксной кислот,в обратном направлении-нейтрализацию какого –либо ацетета.Реакция 2 типа NH4 +H2O=NH3+H3O протекает в прямом направлении показывает гидролиз какой-либо соли аммония ,а в обратном направлении-нейтрализацию аммиака РеакциИ 3типа
протекающая в прямом направлении,представляет ионизацию уксксной кислот,в обратном направлении-нейтрализацию какого –либо ацетета.Реакция 2 типа NH4 +H2O=NH3+H3O протекает в прямом направлении показывает гидролиз какой-либо соли аммония ,а в обратном направлении-нейтрализацию аммиака РеакциИ 3типа 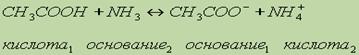 имеют место не только в воде но ив других растворителях например в жидком аммиаке.
имеют место не только в воде но ив других растворителях например в жидком аммиаке.
Гидро́лиз— один из видов химических реакций сольволиза, где при взаимодействии веществ с водой происходит разложение исходного вещества с образованием новых соединений. Механизм гидролиза соединений различных классов: соли, углеводы, белки, сложные эфиры, жиры и др. имеет существенные различия. гидролиз жиров, белков и углеводов происходит при переваривании пищи, а при гидролизе АТФ выделяется энергия, обеспечивающая нужды клетки.При гидролизе солей вода является источником протонов и электронов. Алкалиметрия и ацидиметрия — важнейшие титриметрические методы определения кислот или же оснований, основанные на реакции нейтрализации:Н+ + ОН− = Н2ОТитрование раствором щелочи называется алкалиметрией, а титрование раствором кислоты — ацидиметрией
