Химические свойства рибозы и дезоксирибозы.
1. При окислении по альдегидной группе они образуют соответствующие кислоты.
2. При восстановлении пентозы превращаются в многоатомные спирты.
3. Рибоза и дезоксирибоза имеют большое биологическое значение.4. Они входят в состав нуклеиновых кислот, которые осуществляют в клетках организмов синтез белков и передачу наследственных признаков.
Нуклеозиды и нуклеотиды.Пуриновые и пиримидиновые основания редко присутствуют в клетке в свободном состоянии, обычно они связаны с сахарами, как правило, рибозоц или дезоксирибозой, в нуклеозиды или с пентозофосфатами в нуклеотиды.Нуклеозиды. В пуриновом нуклеозиде сахар присоединен к N-9 пуринового основания β-гликоэидной связью. Если сахаром является D-рибоза, то образуются нуклеозиды аденозин и гуанозин, а если 2-дезокси-D-рибоза, то дезоксиадекозин и дезоксигуанозин. В пиримидиновых нуклеозидах β-гликозидная связь сахара с N-1 пиримидинового основания дает уридин или цитиднн, когда урацил или цитозин присоединяются к рибоэе, либо дезоксицитидин или тимидин, когда цитозин и тимин присоединяются к дезоксирибозе. Следует отметить, что урацил не встречается в виде производного дезоксирибозы, а приставка дезокси не используется применительно к тимидину, поскольку тимин редко встречается в соединении с рибозой.

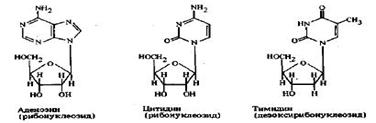
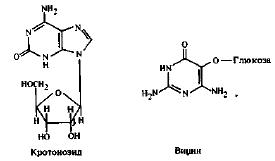
В то время как свободные основания редко присутствуют в клетках растений в заметных количествах, нуклеозиды находят в свободном состоянии наряду с другими комплексами основание - сахар, природа которых зависит or вида растений. Ткани Cmton tiglium содержат свободный нуклеозид кротонозид, образованный пурином изогуанином и сахаром рибозой, а семена видов Vicia содержат глюкоз ид вицин, в котором пиримидин дивицин соединен через кислородный заместитель с сахаром. Кроме того, показано, что зеатин встречается в растительных клетках в форме рибозида.
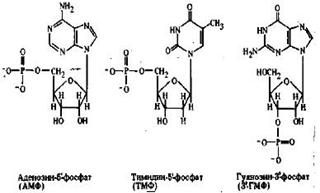 Нуклеотиды. Нуклеотид образуется путем присоединения к остатку сахара в нуклеозиде фосфатной группы. Образование сложноэфирной связи между фосфатом и сахаром может происходить по 2'-, 3'- и 5'-оксигруппам рибозы или 3'- и 5 '-оксигруппам дезоксирибозы. Значком (') обозначают атомы рибозы или дезоксирибозы, чтобы отличить их от атомов углерода в пуриновом или пиримидиновом кольце. Чаще всего этерификации подвергается гидроксил при C-5' пентозного остатка. В результате образуется нуклеозид-5'-фосфат, называемый также 5'-нуклеотидом, тип пентозы обозначают при этом приставкой: 5'-рибонуклеогид или 5'-дезоксирибонуклеотид. В результате этерификации 5'-оксигруппы аденозина образуется нуклеотид адекозин-5'-фосфат, называемый также адан иловой кислотой, или аденилатом. Термин аденилат означает, что фосфатная группа нуклеотида ионизируется при физиологических величинах pH, обычное для этого соединения сокращение - АМФ (аденозинмонофосфат). Другими важнейшими 5 '-нуклеотидами в клетке являются гуанилаг (ГМФ), цитидилат (ЦМФ) и уридилат (УМФ). 5'-Дезоксирибонуклеотиды представлены дезоксиаденилатом (дАМФ), дезоксигуанилатом (дГМФ), дезоксицитидилатом (дЦМФ) и дезокситимидилатом (дТМФ), хотя последний чаше называют тимидилатом, а реже встречающийся рибонуклеотид содержащий рибозу, фосфат и тимин, - риботимидилатом. Хотя преобладающие в природе свободные нуклеотиды - это 5'-фосфорные эфиры, при распаде в клетке нуклеиновых кислот образуются 3'-производные. Поскольку рибонуклеозиды содержат три свободные оксигруппы, помимо 3'- и 5'-эфиров, могут быть образованы 2'-фосфорные эфиры. Этого не происходит с дезоксирибсиуклеозидами, лишенными 2-оксигруппы
Нуклеотиды. Нуклеотид образуется путем присоединения к остатку сахара в нуклеозиде фосфатной группы. Образование сложноэфирной связи между фосфатом и сахаром может происходить по 2'-, 3'- и 5'-оксигруппам рибозы или 3'- и 5 '-оксигруппам дезоксирибозы. Значком (') обозначают атомы рибозы или дезоксирибозы, чтобы отличить их от атомов углерода в пуриновом или пиримидиновом кольце. Чаще всего этерификации подвергается гидроксил при C-5' пентозного остатка. В результате образуется нуклеозид-5'-фосфат, называемый также 5'-нуклеотидом, тип пентозы обозначают при этом приставкой: 5'-рибонуклеогид или 5'-дезоксирибонуклеотид. В результате этерификации 5'-оксигруппы аденозина образуется нуклеотид адекозин-5'-фосфат, называемый также адан иловой кислотой, или аденилатом. Термин аденилат означает, что фосфатная группа нуклеотида ионизируется при физиологических величинах pH, обычное для этого соединения сокращение - АМФ (аденозинмонофосфат). Другими важнейшими 5 '-нуклеотидами в клетке являются гуанилаг (ГМФ), цитидилат (ЦМФ) и уридилат (УМФ). 5'-Дезоксирибонуклеотиды представлены дезоксиаденилатом (дАМФ), дезоксигуанилатом (дГМФ), дезоксицитидилатом (дЦМФ) и дезокситимидилатом (дТМФ), хотя последний чаше называют тимидилатом, а реже встречающийся рибонуклеотид содержащий рибозу, фосфат и тимин, - риботимидилатом. Хотя преобладающие в природе свободные нуклеотиды - это 5'-фосфорные эфиры, при распаде в клетке нуклеиновых кислот образуются 3'-производные. Поскольку рибонуклеозиды содержат три свободные оксигруппы, помимо 3'- и 5'-эфиров, могут быть образованы 2'-фосфорные эфиры. Этого не происходит с дезоксирибсиуклеозидами, лишенными 2-оксигруппы
Циклические нуклеотиды.
Циклические нуклеотиды занимают центральное положение в регуляции процессов метаболизма мышечного волокна.
Являясь производными адениловой и гуаниловой кислот, эти соединения имеют рациональные химические названия —циклический 3,5-аденозинмонофосфат (цАМФ) и циклический 3,5-гуанозинмонофосфат (цГМФ);
Строение циклических нуклеотидоа:
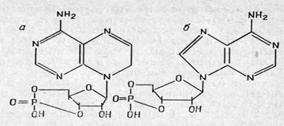 Строение циклических нуклеотидоа: а — цАМФ; б — цГМФ.
Строение циклических нуклеотидоа: а — цАМФ; б — цГМФ.
Адреналин и ацетилхолин вызывают противоположные эффекты, например, адреналин увеличивает частоту и силу сокращения сердечной мышцы,а ацетилхолин уменьшает. Образование цАМФстимулируется адренолином, а образование цГМФ ацетилхолином. Создается впечатление, что цАМФ стимулирует в основном процессы распада ( катаболизма ), а цГМФ процессы синтеза( анаболизма )Наиболее изучен циклический 3', 5'-аденозинмонофосфат (цАМФ) — белый порошок, хорошо растворимый в воде. цАМФ открыт в 1957 американским биохимиком Э. Сазерлендом с сотрудниками при исследовании механизма активации фермента фосфорилазы печени гормонами глюкагоном и адреналином. В тканях животных и человека цАМФ служит посредником в осуществлении многообразных функций различных гормонов и др. биологически активных соединений (некоторых медиаторов, токсинов, лактинов). У бактерий при недостатке в среде легкоусвояемых соединений, например глюкозы, увеличивается содержание цАМФ в клетке, что приводит к биосинтезу адаптивных (индуцируемых) ферментов, необходимых для усвоения др. источников питания. Уровень цАМФ в клетках сальмонеллы Salmonella thyphimurium определяет будущее попавшего в неё фага (при высокой концентрации цАМФ происходит лизогенизация культуры бактерий, при низкой — фаг вызывает её лизис). У миксоамёбы Dictyostelium discoideum цАМФ играет роль аттрактанта, привлекающего клетки друг к другу. У высших растений цАМФ опосредует влияние фитохрома на синтез пигментов бетационинов (у Amaranthus paniculatus).Концентрация цАМФ в тканях млекопитающих очень мала и составляет десятые доли микромоля на 1 кг сырой ткани (10-7—10-6моль). При активации аденилатциклазы, катализирующей биосинтез цАМФ, или блокировании фосфодиэстеразы, осуществляющей гидролиз этого нуклеотида, концентрация цАМФ в клетке быстро увеличивается. Т. о., содержание цАМФ в клетке определяется соотношением активностей этих двух ферментов. Связь между гормоном или др. химическим сигналом (первый «посредник») и цАМФ (второй «посредник») осуществляет т. н. аденилатциклазный комплекс, включающий рецептор, настроенный на определённый гормон (или др. биологически активное вещество) и расположенный на внешней стороне клеточной мембраны, и аденилатциклазу, расположенную на внутренней стороне мембраны. Гормон, взаимодействуя с рецептором, во многих случаях активизирует аденилатциклазу, которая катализирует биосинтез цАМФ. Концентрация цАМФ, образующегося т. о. в клетке, превышает концентрацию действующего на клетку гормона в 100 раз. В основе механизма действия цАМФ в тканях животных и человека лежит его взаимодействие с протеинкиназами — ферментами, активность которых проявляется в присутствии этого нуклеотида (см.схему). Связывание цАМФ с регуляторной субъединицей протеинкиназы приводит к диссоциации фермента и активации его каталитической субъединицы, которая, освободившись от регуляторной субъединицы, способна фосфорилировать определённые белки (в т. ч. ферменты). Изменение свойств этих макромолекул путём фосфорилирования меняет и соответствующие функции клеток. Например, при действии адреналина на клетки печени происходит фосфорилирование двух ферментов — фосфорилазы и гликогенсинтетазы. Фосфорилаза при этом активируется, что приводит к быстрому гидролизу гликогена — запасного вещества печени. Одновременно с началом гидролиза гликогена прекращается его новый синтез, т.к. фермент, участвующий в его образовании, — гликогенсинтетаза при фосфорилировании его протеинкиназами теряет свою активность. Один и тот же гормон, действуя через посредство цАМФ, в разных тканях вызывает различные функциональные ответы, зависящие от особенностей данной ткани. При стрессе, когда потребность в энергии очень велика, мозговой слой надпочечников в повышенном количестве образует гормон адреналин. В печени адреналин обусловливает активное расщепление (фосфоролиз) гликогена, образование фосфорных эфиров глюкозы и выброс в кровь большого количества глюкозы, в жировой ткани — приводит к гидролизу липидов, достигнув сердца, — увеличивает силу сокращения сердечной мышцы, усиливает кровообращение и улучшает питание тканей, осуществляя мобилизацию всех сил организма. цАМФ играет определённую роль в морфологии, подвижности, пигментации клеток, в кроветворении, клеточном иммунитете, вирусной инфекции и др. Некоторые медиаторы, например ацетилхолин, могут ускорять образование др. Ц. н. — 3',5'-гуанозинмонофосфата (цГМФ), который синтезируется в клетке из гуанозинтрифосфата при активации фермента гуанилатциклазы, входящей в гуанилатциклазный комплекс, расположенный в клеточной мембране. Характерно, что многие эффекты цГМФ прямо противоположны эффектам цАМФ. Антагонистические отношения Ц. н. проявляются чаще всего в сложных системах, когда для регуляции клеточной функции требуется разновременная модификация многих белков, осуществляемая согласованным действием попеременно активируемых цАМФ- и цГМФ-зависимых протеинкиназ.Нуклеотидные коферменты и переносчики соединений, их основные типы.
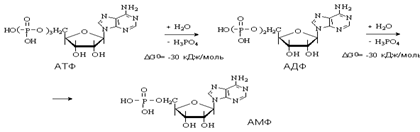
Коферменты – это органические соединения небелковой природы, которые необходимы для осуществления каталитического действия ферментов. Коферменты относятся к разным классам органических соединений. Важную группу коферментов составляют нуклеозидполифосфаты.Аденозинфосфаты – производные аденозина, содержащие остатки моно-, ди- и трифосфорных кислот. Особое место занимают аденозин-5/-моно-, ди- и трифосфаты - АМФ, АДФ и АТФ - макроэргическиевещества, которые обладают большими запасами свободной энергии в подвижной форме. Молекула АТФ содержит макроэргические связи Р-О, которые легко расщепляются в результате гидролиза. Выделяющаяся при этом свободная энергия обеспечивает протекание сопряженных с гидролизом АТФ термодинамически невыгодных анаболических процессов, например, биосинтез белка.
Кофермент А. Молекула этого кофермента состоит из трех структурных компонентов: пантотеновой кислоты, 2-аминоэтантиола и АДФ.

Кофермент А участвует в процессах ферментативного ацилирования, активируя карбоновые кислоты путем превращения их в реакционноспособные сложные эфиры тиолов.
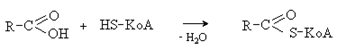
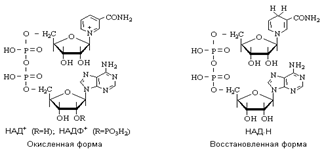
Никотинамидадениндинуклеотидные коферменты. Никотинамидадениндинуклеотид (НАД+) и его фосфат (НАДФ+) содержат в своем составе катион пиридиния в виде никотинамидного фрагмента. Пиридиниевый катион в составе этих коферментов способен обратимо присоединять гидрид-анион с образованием восстановленной формы кофермента - НАД Н.
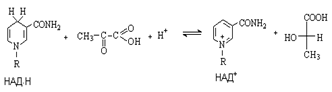
Таким образом никотинамидадениндинуклеотидные коферменты участвуют в окислительно-восстановительных процессах, связанных с переносом гидрид-аниона, например, окислении спиртовых групп в альдегидные (превращение ретинола в ретиналь), восстановительном аминировании кетокислот, восстановлении кетокислот в гидроксикислоты. В ходе этих процессов субстрат теряет (окисление) или присоединяет (восстановление) два атома водорода в виде Н+ и Н-. Кофермент служит при этом акцептором (НАД+) или донором (НАД.Н) гидрид-иона. Все процессы с участием коферментов являются стереоселективными. Так, при восстановлении пировиноградной кислоты образуется исключительно L-молочная кислота.
Олиго- и полинуклеотиды.
Если фосфатная группа одного нуклеотида взаимодействует с 3′-OH-группой другого нуклеотида, образуется динуклеотид с фосфодиэфирной связью. Такой динуклеотид несёт на 5′-конце свободную фосфатную группу, а на 3′-конце свободную OH-группу. Поэтому можно за счёт образования ещё одной фосфодиэфирной связи присоединить новый мононуклеотид. Таким путём образуются олигонуклеотиды и, наконец, полинуклеотиды.Полинуклеотиды, составленные из рибонуклеотидных звеньев, называются рибонуклеиновыми кислотами (РНК), из дезоксирибонуклеотидных мономеров — дезоксирибонуклеиновыми кислотами
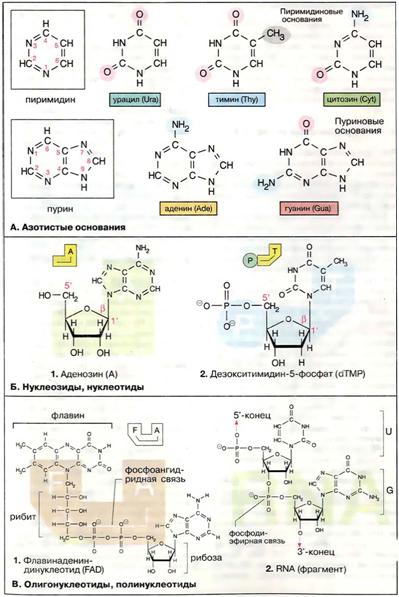 Нуклеотиды – это повторяющиеся мономерные единицыолигонуклеотидов и полинуклеотидов. Олигонуклеотиды построены из нескольких мономеров, полинуклеотиды – из многих. Нуклеиновые кислоты представляют собой полинуклеотиды, построенные из мономеров – нуклеотидов, число которых колеблется от 7 десятков до сотен миллионов.
Нуклеотиды – это повторяющиеся мономерные единицыолигонуклеотидов и полинуклеотидов. Олигонуклеотиды построены из нескольких мономеров, полинуклеотиды – из многих. Нуклеиновые кислоты представляют собой полинуклеотиды, построенные из мономеров – нуклеотидов, число которых колеблется от 7 десятков до сотен миллионов.
Молекулы нуклеиновых кислот всех типов живых организмов – линейные полимеры, не имеющие разветвлений, что доказано с помощью ряда методов (химических, ферментативных, электронной микроскопии). Наличие так называемых палиндромных шпилек, образующих своеобразные боковые отростки от линейной цепи ДНК, не следует считать нарушением ее линейности, так как в пределах каждой шпильки линейность структуры сохраняется. При суперспирализации ДНК также могут возникать своеобразные структуры, однако это тоже будут различные изгибы непрерывно продолжающейся линейной цепи. Роль мостика между нуклеотидами выполняет 3’,5’-фосфодиэфирная связь, соединяющая C-3’ D-рибозы (или 3’-дезоксирибозы) одного нуклеотида и C-5’ другого. В связи с этим полинуклеотидная цепь имеет определенное направление. На одном ее конце остается свободной 5’-OH-группа (начало цепи), на другом – 3’-OH-группа (конец цепи). Концевые гидроксильные группы могут быть этерифицированы фосфатом. Полное написание полинуклеотидных цепей сложно и громоздко, поэтому применяют схематическое изображение. Вертикальными прямыми линиями обозначают углеродные цепи сахаров с основаниями, присоединенными к C-1’ диагоналями с буквой P в середине – фосфодиэфирые связи между атомом C-3’ (вблизи середины прямой линии) и C-5’ (конец следующей линии). Используют также буквенную систему: буквами А, Г, Ц, Т, У обозначают азотистые основания, буквой ф – фосфатную группу. Если буква ф находися слева, этерифицирована группа при C-5’, справа – этерифицирована группа при C-3’ (рис. 4.1). Например, фА – аденозин-5’-фосфат, Аф – аденозин-3’-фосфат. Полинуклеотидная цепь несет множество фосфатных групп, которые легко диссоциируют, вследствие чего она приобретает отрицательный заряд. В связи с этим нуклеиновые кислоты в клетке во многих случаях связываются с основными белками, образуя нуклеопротеины. РНК входят в состав рибонуклеопротеинов (РНП), ДНК – дезоксирибонуклеопротеинов (ДНП). Олигонуклеотид (oligonucleotide) - короткий фрагмент ДНК или РНК , получаемый либо путем химического синтеза, либо расщеплением более длинных полинуклеотидов . Используются в качествезондов или праймеров.Химический синтез олигонуклеотидов наиболее эффективен в твёрдофазном варианте, основанном на фосфорамидитных строительных блоках. Синтез олигонуклеотидов в значительной степени автоматизирован. Другие методы, такие как фосфодиэфирный метод, фосфотриэфирный метод или H-фосфонатный метод, представляют в основном исторический интерес и применяются крайне редко.[1]Химический синтез олигонуклеотидов реализуется на твёрдом носителе пошаговым добавлением соответствующим образом активированных и защищённых нуклеозидных строительных блоков, до тех пор пока не будет получена заданная последовательность. Далее все защитные группы, необходимые в процессе элонгации цепи, удаляются одновременно с отсоединением олигонуклеотида от твёрдой подложки. Длина и чистота продукта определяется качеством связывания и удаления защитных групп.[1]Структурная организация ДНК: первичная, вторичная и третичная структуры.
Первичная структура молекулы ДНК Под первичной структурой нуклеиновых кислот подразумевают последовательность расположения нуклеотидов в полинуклеотидной цепи ДНК. Нуклеотиды связываются между собой при помощи фосфодиэфирных связей, которые образуются между ОН-группой в положении 5 дезоксирибозы одного нуклеотида и ОН-группой в положении 3 пентозы другого. Биологические свойства нуклеиновых кислот определяются качественным соотношением и последовательностью нуклеотидов вдоль полинуклеотидной цепи. Нуклеотидный состав ДНК у организмов разных таксономических групп специфичен и определяется отношением (Г + Ц)/(А + Т). С помощью коэффициента специфичности была определена степень гетерогенности нуклеотидного состава ДНК у организмов различного происхождения. Так, у высших растений и животных отношение (Г+Ц)/(А+Т) колеблется незначительно и имеет значение больше 1. Для микроорганизмов коэффициент специфичности изменяется в широких пределах — от 0,35 до 2,70. Вместе с тем соматические клетки данного биологического вида содержат ДНК одного и того же нуклеотидного состава, т. е. можно сказать, что по содержанию ГЦ-пар оснований ДНК одного вида идентичны. Определение гетерогенности нуклеотидного состава ДНК по коэффициенту специфичности еще не дает информации о ее биологических свойствах. Последнее обусловлено различной последовательностью отдельных нуклеотидных участков в полинуклеотидной цепи. Это значит, что генетическая информация в молекулах ДНК закодирована в специфической последовательности ее мономерных единиц. Молекула ДНК содержит нуклеотидные последовательности, предназначенные для инициации и терминации процессов синтеза ДНК (репликация), синтеза РНК (транскрипция), синтеза белка (трансляция). Имеются нуклеотидные последовательности, которые служат для связывания специфических активирующих и ингибирующих регуляторных молекул, а также нуклеотидные последовательности, не несущие какой-либо генетической информации. Существуют также модифицированные области, которые защищают молекулу от действия нуклеаз. Проблема нуклеотидной последовательности ДНК до настоящего времени полностью не разрешена. Определение нуклеотидной последовательности нуклеиновых кислот является трудоемкой процедурой, предусматривающей применение метода специфического нуклеазного расщепления молекул на отдельные фрагменты. На сегодняшний день полная нуклеотидная последовательность азотистых оснований установлена для большинства тРНК разного происхождения.
Молекула ДНК: вторичная структура Уотсон и Крик спроектировали модель двойной спирали дезоксирибонуклеиновой кислоты. Согласно данной модели две полинуклеотидных цепи обвивают друг друга, при этом образуется своеобразная спираль. Азотистые основания в них расположены внутри структуры, а фосфодиэфирный остов — снаружи.
Молекула ДНК: третичная структура Линейная ДНК в клетке имеет форму вытянутой молекулы, она упакована в компактную структуру и занимает всего 1/5 объема клетки. Например, длина ДНК хромосомы человека достигает 8 см, а упакована так, что умещается в хромосоме с длиной 5 нм. Подобная укладка возможна благодаря наличию спирализованных структур ДНК. Из этого следует, что двухцепочечная спираль ДНК в пространстве может подвергаться дальнейшей укладке в определенную третичную структуру — суперспираль. Суперспиральная конформация ДНК характерна для хромосом высших организмов. Подобная третичная структура стабилизируется за счет ковалентных связей с остатками аминокислот, входящих в состав тех белков, которые образуют нуклеопротеидный комплекс (хроматин). Следовательно, ДНК эукариотических клеток ассоциирована с белками главным образом основного характера — гистонами, а также кислыми белками и фосфопротеидами Правила Чаргаффа.Первое правило ЧаргаффаВ 1950-1952 гг. Чаргафф с сотрудниками проводил хроматографические исследования ДНК (уже было известно, что в состав ДНК входят четыре типа нуклеотида, но о спирали еще не знали). Результатом исследований стало первое правило Чаргаффа: в молекулах ДНК количество тимина (T) равно количеству аденина (A), а количество гуанина (G) равно количеству цитозина (C). Таким образом, если T и A, также как C и G, в целой молекуле ДНК идут всегда парами, то, разумеется, их количества будут одинаковы. Второе правило ЧаргаффаСуть второго правила Чаргаффа так же проста, как и первого. Собственно, второе правило и есть первое правило, только в применении к единичной нити ДНК. То есть оно гласит, что в отдельной нити ДНК количество A ≈ количеству T, количество G ≈ количеству C.На самом деле, из работы Чаргаффа следовало только то, что внутри одной нити ДНК сумма A + C равна сумме T + G. Кроме того, у него речь идет о ДНК конкретной бактерии. Первые публикации, обращающие внимание на универсальность феномена в вышеуказанном определении, появились лишь в 90-х годах, когда анализ проводился уже прямым подсчетом оснований в секвенированных последовательностях, а не хроматографически.В отличие от первого правила, в котором числа комплеменатрных оснований в двойной спирали ДНК равны точно, равенства во втором правиле приближенные. Насколько эти равенства нарушены – зависит от длины анализируемого участка. Для целой хромосомы высших эукариот ошибка в равенствах A ≈ T, G ≈ C составляет сотые доли процента, иногда еще меньше. Что касается меньших участков генома, то точность равенств держится на длинах до 70-100 тысяч пар оснований – независимо, кодирующие там области или нет, — а дальше начинает спадать. На длинах от десятков тысяч до одной тысячи правило еще держится, хотя уже с большей ошибкой, а на длинах в сотни пар оснований и меньше оно уже практически не наблюдается.Как выяснилось, правило это универсальное. Ему подчинены геномы практически всех организмов – вирусов, бактерий, архей, эукариот. Исключениями из него явились лишь геномы некоторых органелл (особенно митохондрии позвоночных), геномы вирусов с однонитевой ДНК и геномы всех РНК-вирусов. Но я коснусь этого дела подробнее позжеКомплементарность оснований открыл Чаргафф, который сформулировал такие правила: 1. Количество пуриновых оснований равно количеству пиримидиновых (А + Г = Ц + Т) 2. Количество аденина равно количеству тимина, а гуанину - цитозина (А = Т; Г = Ц).Комплементарные пары нуклеотидов.
Пара нуклеотидов - Элементарная единица двухцепочечной молекулы нуклеиновой кислоты. Парынуклеотидов в ДНК формируются по принципу комплементарности – гуанин-цитозин и аденин-тимин (в РНК или гибридных ДНК/РНК-дуплексах – аденин-урацил). Также пара нуклеотидов – единица измерения размера длины гена, сайта, хромосомы, генома.Против одной цепи нуклеотидов располагается вторая цепь. Расположение нуклеотидов в этих двух цепях не случайное, а строго определенное: против аденина одной цепи в другой цепи всегда располагается тимин, а против гуанина — всегда цитозин, между аденином и тимином возникают две водородные связи, между гуанином и цитозином — три водородные связи. Закономерность, согласно которой нуклеотиды разных цепей ДНК строго упорядоченно располагаются (аденин — тимин, гуанин — цитозин) и избирательно соединяются друг с другом, называется принципом комплементарности.Из принципа комплементарности следует, что последовательность нуклеотидов одной цепи определяет последовательность нуклеотидов другой.Цепи ДНК антипараллельны (разнонаправлены), т.е. нуклеотиды разных цепей располагаются в противоположных направлениях, и, следовательно, напротив 3'-конца одной цепи находится 5'-конец другой. Молекулу ДНК иногда сравнивают с винтовой лестницей. «Перила» этой лестницы — сахарофосфатный остов (чередующиеся остатки дезоксирибозы и фосфорной кислоты); «ступени» — комплементарные азотистые основания.Причиной комплементарности оснований является совпадение углов, по которым основания присоединяются к пентозофосфатным остаткам ДНК. Это обеспечивает максимальное сближение между собой пар – аденин-тимин и гуанин – цитозин.Формы ДНК.Исследования М. Уилкинса и Р. Франклин показали, что молекулы ДНК могут давать различную дифракционную картину в рентгеновских лучах в зависимости от содержания воды и солей. Модель, предложенная Уотсоном и Криком, соответствовала значениям параметров структуры, полученным на основе рентгенограммы В-формы ДНК, изображенной на рис. 21. В-форма характеризуется плоскопараллельным расположением пар нуклеотидных оснований внутри двойной спирали. Плоскости оснований почти перпендикулярны оси спирали и отстоят друг от друга на 0,34 нм. Этой повторяющейся единице соответствуют яркие меридиональные дуги в верхней и нижней частях рентгенограммы, изображенной на рис. Диаметр спирали почти в точности равен 2 нм, а соседние пары нуклеотидных оснований повернуты друг относительно друга на 36°. В результате на один виток спирали приходится десять пар оснований. На рис. изображена спираль с правым направлением вращения. Рентгенограмма ДНК, однако, не дает достаточной информации для того, чтобы судить, является спираль правой или левой. При построении своей модели Дж. Уотсон и Ф. Крик выбрали направление вращения произвольно.
Возможное разнообразие структур двухцепочечных молекул ДНК стало ясным относительно недавно в результате экспериментов по кристаллизации гомогенных двухцепочечных олигомеров ДНК, получаемых посредством химического синтеза. Дифракционные рентгеновские картины, полученные на таких кристаллах ДНК, более четки, чем получаемые на природной ДНК, и позволяют определить с большой точностью положения отдельных атомов. Эти исследования обнаружили, что как право-, так и левозакрученная двухцепочечная спираль ДНК может существовать в нескольких модификациях, характеризуемых различными значениями параметров. Форма спирали определяется свойствами растворителя и последовательностью нуклеотидов. Самокомплементарный тетрамер ДНК типа ЦГЦГ (5'-конец всегда пишется слева) образует при кристаллизации левозакрученную двухцепочечную структуру, получившую название Z-ДНК вследствие зигзагообразного характера фосфодиэфирного каркаса. Напротив, самокомплементарный додекамер ЦГЦГААТТЦГЦГ кристаллизуется в виде правозакрученной двухцепочечной спирали В-формы, хотя содержит на обоих концах 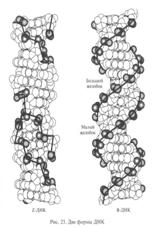 последовательность ЦГЦГ, которая сама по себе кристаллизуется в Z-форме. Обе формы ДНК изображены для сравнения рядом
последовательность ЦГЦГ, которая сама по себе кристаллизуется в Z-форме. Обе формы ДНК изображены для сравнения рядом
Исследования структуры полимера (ЦГ)n в растворе показали, что эта молекула может существовать в одной из двух альтернативных форм: в правой В-форме или левой Z-форме. Эти две формы переходят одна в другую при изменении ионной силы раствора или катионов, нейтрализующих отрицательный заряд на фосфодиэфирном каркасе. Природные молекулы ДНК в основном существуют в правой В-форме, если они не содержат последовательности типа (ЦГ)n. Однако если такие последовательности входят в состав ДНК, то эти участки при соответствующих условиях могут переходить в Z-форму. Возможность такого перехода указывает на то, что две цепи в двойной спирали ДНК находятся в динамическом состоянии и могут раскручиваться друг относительно друга, переходя из правой формы в левую и наоборот. Молекулы ДНК для этого должны быть довольно лабильны и допускать конформационные превращения.
Обработка гигантских хромосом дрозофилы в клетках слюнных желез специфичными к Z-ДНК антителами свидетельствует о том, что ДНК в хромосомах существует в обеих формах. Биологические следствия такой лабильности структуры ДНК пока не вполне понятны.
Кое-что известно о биологическом значении правозакрученной А-формы ДНК. В неблагоприятных условиях некоторые бактерии превращаются в споры. В таком неактивном состоянии они могут находиться сколь угодно долго, пока не появятся подходящие условия для размножения. В этом состоянии их ДНК окутана так называемыми споровыми белками. С.Мор (США) и его коллеги, используя оптические методы, показали, что ДНК при этом находится в А-форме.Незадолго до этого исследования было обнаружено, что ДНК в спорах гораздо устойчивее к поражающему действию ультрафиолетового излучения, чем та же ДНК в бактериях, активно размножающихся. Почти в то же самое время выяснили, что А-ДНК примерно в 10 раз более устойчива к поражающему действию ультрафиолетового излучения, чем В-ДНК. Споровые белки превращают ДНК бактерии из В- в А-форму, чтобы защитить ДНК. Это один из немногих примеров, где биологическая роль А-формы проступает особенно явно. Есть и другие примеры, когда А-ДНК была найдена в биологических структурах или процессах. Их количество все возрастает.
Палиндромы
Палиндром (palindrome) — нуклеотидная последовательность ДНК, читаемая одинаково в обоих направлениях. П. является тандемным инвертированным повтором
 Палиндромы - повторы последовательностей нуклеотидов на обоих цепях, которые читаются одинаково слева направо и справа налево (если их читать в направлении 5'>3' ). 5’- ЦТТЦГАТЦГААГ.....ЦТТЦГАТЦГААГ-3’ 3’- ГААГЦТАГЦТТЦ.....ГААГЦТАГЦТТЦ-5’
Палиндромы - повторы последовательностей нуклеотидов на обоих цепях, которые читаются одинаково слева направо и справа налево (если их читать в направлении 5'>3' ). 5’- ЦТТЦГАТЦГААГ.....ЦТТЦГАТЦГААГ-3’ 3’- ГААГЦТАГЦТТЦ.....ГААГЦТАГЦТТЦ-5’
